Ультразвуковая диагностика в оценке состояния детей при муковисцидозе
Москва, Россия.
Рубрика: Эхография в педиатрии
УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Муковисцидоз - это частое моногенное заболевание, обусловленное мутацией гена трансмембранного регулятора белка, характеризующееся поражением всех экзокринных желез жизненно важных органов и имеющее обычно тяжелое течение и неблагоприятный прогноз. Заболевание наследуется по аутосомно-рецессивному типу и рано приводит к стойкой инвалидизации, снижению продолжительности жизни больных, необходимости постоянного диспансерного наблюдения и проведения лечебных мероприятий. Распространенность муковисцидоза в нашей стране составляет 1 из 5000 новорожденных. Проблема своевременной диагностики муковисцидоза, раннего начала терапии и активной реабилитации больных актуальна не только с медицинской, но и социальной точки зрения [1, 2].
В начальной стадии патологического процесса болезнь проявляется в 43 % случаев респираторным синдромом, в 12 - кишечным и в 45 % - их сочетанием. Патогенез поражения аппарата внешнего дыхания при муковисцидозе сходен с механизмами, нарушающими деятельность пищеварительных желез, хотя и имеет свои особенности. Вязкий секрет слизистых желез бронхиального дерева закупоривает мельчайшие бронхи с последующим развитием участков эмфиземы, нарушением равномерности вентиляции легких и артериальной гипоксии. Обструктивные изменения сосудов малого круга кровообращения приводят к легочной гипертензии, правожелудочковой недостаточности и формированию хронического легочного сердца. Характер и степень поражения легких являются определяющими для жизни больного, поскольку от легочных осложнений погибает до 90 % больных муковисцидозом [3]. Немаловажная роль в патогенезе заболевания отводится поражениям системы пищеварения и прежде всего - поджелудочной железы и печени. Однако изменениям желудочно-кишечного тракта, к сожалению, уделяется незначительное внимание, что приводит подчас к серьезным ошибкам в терапии больных муковисцидозом и развитию у них тяжелых осложнений, требующих иногда хирургического лечения [4].
В настоящее время произошел значительный прогресс в решении проблемы муковисцидоза: открыт ген муковисцидоза, разработаны современные принципы терапии и реабилитации больных, что значительно повышает качество жизни пациентов и увеличивает ее продолжительность. Актуальным остается вопрос о своевременной диагностике муковисцидоза. Несмотря на манифестный характер этого заболевания, муковисцидоз отличается многообразием клинической картины, что представляет значительные трудности в диагностике, требует дифференциации со многими заболеваниями и создает условия для диагностических ошибок. Муковисцидоз часто ошибочно принимают за хроническую пневмонию, бронхиальную астму, рецидивирующий или обструктивный бронхит, острую кишечную инфекцию и кишечную непроходимость [5]. Полисиндромность смешанной формы муковисцидоза проявляется в сочетании бронхообструкции с кишечными нарушениями и дефицитом массы тела, т.е. классической триадой клинических симптомов муковисцидоза, что должно нацеливать клиницистов на проведение лабораторных методов: определение хлоридов пота и ДНК-диагностику. Только совокупность характерных анамнестических, клинических, рентгенологических сведений и повышение показателей хлоридов в поте позволяют верифицировать диагноз "муковисцидоз". Диагностические ошибки влекут за собой ошибочные терапевтические мероприятия, что, в свою очередь, усугубляет тяжесть заболевания и его прогноз. С целью предотвращения развития таких осложнений, как кровотечение из верхних отделов пищеварительного тракта в результате цирроза печени (ЦП) и портальной гипертензии, используются визуальные методы диагностики, в частности, ультразвуковой.
Внедрение новейших высокоинформативных технологий, в том числе допплерографических методик, дают возможность оценить не только состояние желудочно-кишечного тракта, поджелудочной железы и гепатобилиарной системы у больных муковисцидозом, но и состояние кровотока в сосудах системы воротной вены и чревного ствола, позволяют расширить диагностический диапазон и выработать дополнительные критерии диагностики. На современном этапе эти вопросы остаются актуальными, поскольку все еще у значительной части больных диагноз уточняется в поздние сроки [5].
Цель настоящего исследования - сопоставление клинико-лабораторных и ультразвуковых данных для выявления дополнительных критериев диагностики муковисцидоза у детей.
Материалы и методы
В НЦЗД РАМН за период с 2001 по 2005 г. было обследовано 38 детей в возрасте от 1 месяца до 17 лет со смешанной формой муковисцидоза. Диагноз муковисцидоза базировался на наличии хронического бронхолегочного процесса, типичного кишечного синдрома, случаев муковисцидоза у сибсов, положительного потового теста и данных генетического исследования.
Всем больным проводилось полное клинико-лабораторное обследование с анализом анамнестических данных. Клинические и биохимические исследования включали: общий анализ крови, протеинограмму, определение билирубина и его фракций, АЛТ и АСТ, липазы, амилазы, щелочной фосфатазы, гамма-глютамилтрансферазы, иммунологическое обследование, общий анализ мочи, копрограмму, посев мокроты на микрофлору и чувствительность к антибиотикам, рентгенографию грудной клетки и придаточных пазух носа, исследование функции внешнего дыхания, электрокардиографию, потовую пробу, ДНК-диагностику, исследования показателей липидного и углеводного обменов. Определялись маркеры гепатита В, С, Д. Правильный направляющий диагноз был поставлен лишь у половины детей, несмотря на то, что в 80 % случаев первые симптомы заболевания появились уже на первом году жизни пациентов, но это можно объяснить полиморфностью клинических симптомов муковисцидоза [4].
Пациенты с муковисцидозом были разделены на две группы по степени тяжести заболевания в соответствии со шкалой Швахмана-Брасфильда в модификации С.В. Рачинского и Н.И. Капранова. Первую группу составили 22 ребенка с течением заболевания средней тяжести (оценка по шкале Швахмана-Брасфильда составила 54,2±0,4 балла) и вторую группу - 16 детей с тяжелым течением муковисцидоза (38,1±0,2 балла). Диагноз муковисцидоза у больных подтверждался положительным потовым тестом, который проводился неоднократно классическим методом пилокарпинового электрофореза по Гибсону-Куку титрованием хлором в лаборатории НЦЗД РАМН и РДКБ. У всех обследованных детей концентрация хлоридов в потовой жидкости составляла в среднем 81,5±1,4 ммоль/л (при норме менее 60 ммоль/л) и достаточной навеске пота более 150 мг. Всем детям проводилась ДНК-диагностика с определением генотипа.
Респираторный синдром клинически характеризовался приступообразным кашлем с вязкой, трудноотделяемой мокротой, одышкой. Симптомы "барабанные пальцы" и "часовые стекла" наблюдались у 9 детей с тяжелым течением заболевания.
Нарушения со стороны желудочно-кишечного тракта в основном проявлялись в виде характерного синдрома мальабсорбции: вздутие и увеличение размеров живота, учащение стула, полифекалия, резко зловонный, блестящий замазкообразный стул, иногда с видимой стеатореей, плохая прибавка массы тела часто при повышенном аппетите, снижение мышечного тонуса и тургора тканей. Лишь у небольшого числа больных отмечалась склонность к запорам, но у этих детей при ультразвуковом исследовании кишечника имело место расширение ампулы прямой кишки.
Всем пациентам проводилось ультразвуковое исследование органов брюшной полости, забрюшинного пространства и сердца (ЭхоКГ) с помощью современных ультразвуковых диагностических аппаратов с использованием датчиков с частотами 3,5-5 и 6-8 МГц по общепринятым методикам. Допплерографические методики исследования включали оценку кровотока (линейные и объемная скорости) по сосудам портальной системы (воротная и селезеночная вены) и сосудам чревного ствола (индексы резистентности общей печеночной и селезеночной артерий). Определялась форма кривой кровотока по средней печеночной вене. Проводилось исследование центральной и внутрисердечной гемодинамики, оценивалось давление в легочной артерии. Эндоскопическое исследование верхних отделов желудочно-кишечного тракта было проведено 12 больным.
При статистической обработке полученных результатов вычисляли процентные отличия показателей у больных детей от показателей контрольной группы (соответственно возрасту пациентов), которую составили 80 здоровых сверстников. В связи с небольшим количеством пациентов деление на возрастные группы не представлялось возможным из-за малочисленности подгрупп. В группу сравнения вошли 100 больных с хроническими гепатитами В и С и 60 больных с циррозом печени в исходе хронических гепатитов В и С и билиарным циррозом печени. Достоверными считались различия при р<0,05.
Результаты и обсуждение
По данным ЭхоКГ у больных со средней тяжестью течения муковисцидоза отмечалось умеренное параллельное развитие дилатации полости правого желудочка (Дд ПЖ) и утолщение миокарда его стенок (Тм ПЖ), что в среднем составило 29,4±4,8 и 18,8±3,3 % соответственно (табл. 1). Такие факторы, как увеличение сроков заболевания, тяжесть его течения, степень нарушения показателей функции внешнего дыхания, уровень гипоксемии и гиперкапнии в большей степени влияют на величину объема полости ПЖ, чем на толщину миокарда. Изменения со стороны левого желудочка выражались в уменьшении его размеров (Дд ЛЖ) в среднем на 9,6±5,8 %, снижении насосной функции сердца (УО) на 19,6±3,3 % от должного, а также сократительной способности миокарда: ФИ понижалась до 0,56±0,04 (при норме 0,65±0,04), что, возможно, было связано с дистрофическими процессами в сердечной мышце [6]. Толщина миокарда левого желудочка (Тм ЛЖ) у детей этой группы была в пределах нормы. Внутрисердечная гемодинамика характеризовалась наличием умеренной недостаточности трикуспидального клапана (+/++) при максимальной скорости регургитации 2,2±0,4м/с и градиентом давления 19,5 мм рт.ст. Это свидетельствовало об умеренном повышении давления в системе легочной артерии, которое, в среднем по группе, составило 24,6 мм рт.ст. (при норме 15 мм рт.ст.).
| Показатель | Течение муковисцидоза | |
|---|---|---|
| средней тяжести (n=22) | тяжелое (n=16) | |
| Дд ПЖ | +29,4±4,8* | +46,8±6,4*ˆ |
| Тм ПЖ | +18,8±3,3* | +30,8±5,4*ˆ |
| Дд ЛЖ | -9,6±5,8 | -21,4±5,6*ˆ |
| Тм ЛЖ | +2,3±5,8 | +30,4±4,9*ˆ |
| УО | -19,6±3,3* | -27,4±5,3*ˆ |
| ФИ (усл. ед) | 0,56±0,04 | 0,52±0,03* |
| Регургитация на ТК | +/++ | ++/+++ |
| V max рег. на ТК (м/с) | 2,2±0,4 | 3,2±0,26 ˆ |
| Давление в ЛА (мм рт. ст.) | 24,6±1,4 | 46,4±2,6*ˆ |
В группе детей с тяжелым течением муковисцидоза выраженность эксцентрической гипертрофии ПЖ была достоверно выше, чем у больных с течением муковисцидоза средней тяжести. Дилатация полости ПЖ преобладала над гипертрофией миокарда. Параметры ЛЖ изменялись разнонаправлено: диаметр полости был, как правило, уменьшен, в то время как толщина миокарда увеличена, т.е. возникала так называемая концентрическая гипертрофия ЛЖ. Согласно данным Н.И. Капранова [6], утолщение миокарда ЛЖ можно объяснить не только включением артериоло-артериолярных анастомозов при высокой легочной гипертензии, увеличивающим "постнагрузку" на ЛЖ, но и выраженным межуточным отеком и лимфоидноклеточной инфильтрацией миокарда. На отсутствие истинной гипертрофии указывало значительное нарушение насосной функции сердца: УО был снижен на 27,4±4,4 % от должного, а ФИ была уменьшена до 0,52±0,05. Изменения транстрикуспидального кровотока выражались в довольно значительной регургитации (++/+++) при максимальной скорости около 3 м/с, что свидетельствовало о существенной легочной гипертензии - в среднем по группе 46,4 мм рт.ст.
Анализ результатов полученных данных показал, что у детей с муковисцидозом изменения морфометрических и функциональных параметров сердца, а также показателей внутрисердечной гемодинамики зависят от тяжести течения заболевания. У больных муковисцидозом по мере прогрессирования процесса происходит повышение давления в системе легочной артерии, причиной которого может быть нарастание гипоксемии, гиперкапнии, снижения вентиляционной способности легких. У детей с тяжелым течением муковисцидоза ультразвуковые признаки бивентрикулярной недостаточности, выражающейся в эксцентрической гипертрофии правого желудочка, концентрической гипертрофии левого желудочка, нарушении насосной функции сердца и контрактильной способности миокарда, были достоверно выше, чем у детей со средней тяжестью течения муковисцидоза.
При ультразвуковом исследовании гепатобилиарной системы у всех детей с течением муковисцидоза средней тяжести отмечались различные изменения желчного пузыря: у 8 пациентов его размеры были увеличены, у 4 детей - уменьшены, у 3 - желчный пузырь не визуализировался, у 2 детей на эхограмме в области проекции желчного пузыря определялся гиперэхогенный тяж, что могло быть связано с его склерозированием (рис. 1а). В группе детей с тяжелым течением муковисцидоза увеличение размеров желчного пузыря отмечено лишь у 3 детей, уменьшение его размеров - у 6 больных, не визуализировался - у 3 детей и у 3 пациентов имели место признаки его склерозирования.
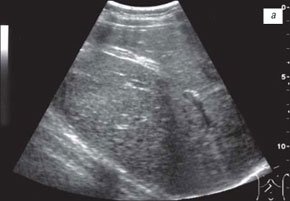
а) При муковисцидозе средней тяжести (склерозированный пузырь).
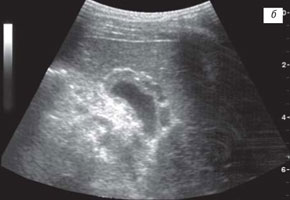
б) При тяжелым течении муковисцидоза.
Независимо от тяжести течения муковисцидоза аномалии развития желчного пузыря в виде различных перегибов: в области дна, тела, воронки, а также "S-образная" форма наблюдались у 18 детей. У 14 пациентов в просвете пузыря определялась "взвесь", у 3 детей - неполные перегородки в области шейки пузыря, у 3 детей старшего возраста имели место множественные конкременты размером от 6 до 12 мм. Стенки желчного пузыря были утолщены до 4 мм у 6 детей старшего возраста и до 2 мм - у 10 пациентов. У 5 детей с тяжелым течением муковисцидоза утолщение стенок желчного пузыря составило от 6 до 14 мм и у 2 из них определялся варикоз сосудов его стенок (рис. 1 б).
При ультразвуковом исследовании поджелудочной железы у 16 из 22 детей с течением муковисцидоза средней тяжести (68 %) и у всех детей с тяжелым течением заболевания (100 %) отмечалось ее увеличение, которое, как правило, сочеталось с повышением эхогенности паренхимы и ее неоднородностью вследствие чередования изо. и гиперэхогенных участков. Возможно, разрешающая способность ультразвуковых приборов даже такого класса, на которых выполнялась работа, все еще не позволяет дифференцировать гиперэхогенные участки как очень мелкие кисты. У 4 детей первой группы и у 3 пациентов второй группы (21 %) на фоне гиперэхогенной неоднородной паренхимы по переднему контуру поджелудочной железы определялись анэхогенные участки с беспорядочным расположением, размером от 4 до 11 мм, что расценивалось как кисты поджелудочной железы (рис. 2). По данным других авторов, кисты поджелудочной железы наблюдались в 9 % случаев и представляли собой аневризматически расширенные участки вирсунгова протока [7]. У 18 пациентов обеих групп наблюдались гиперэхогенные параллельные эхо-сигналы, чаще в паренхиме хвоста поджелудочной железы, что оценивалось как уплотнение стенок сосудов в этой области. У 6 больных младшего возраста с течением муковисцидоза средней тяжести изменений поджелудочной железы не было. Панкреатическая недостаточность, определяемая по уровню эластазы-1 в стуле, выявлена у 4 пациентов с течением муковисцидоза средней тяжести и у 7 детей - с тяжелым течением муковисцидоза. По данным некоторых авторов, поджелудочная железа вовлекается в процесс в 80 % случаев и ее дисфункция является вторичной, вызванной механической закупоркой выводных протоков вязким слизистым секретом [4, 8]. Выделение энзимов поджелудочной железой бывает нарушено полностью или частично, и секреторная недостаточность обнаруживается уже на самых ранних этапах периода новорожденности. В результате изменений панкреатической секреции нарушается двигательная функция кишечника, возникают поносы или запоры. Нормальное всасывание жиров становится невозможным, что приводит к появлению обильного, зловонного, "вязкого стула сального вида". Эти симптомы появляются в возрасте 1-3 месяцев, но могут развиваться и позднее [8]. Тяжелое течение муковисцидоза может приводить к тотальному перерождению поджелудочной железы, когда эхографически она определяется как гиперэхогенный тяж небольших размеров с кальцинатами в паренхиме. В наших наблюдениях таких изменений поджелудочной железы не отмечалось. При современном лечении адекватными дозами панкреатических ферментов кальцинаты в паренхиме поджелудочной железы практически не встречаются [1, 4].
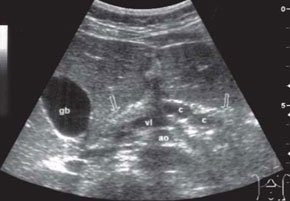
Рис. 2. Эхограмма поджелудочной железы ребенка с тяжелым течением муковисцидоза.
У всех детей при ультразвуковом исследовании печени наблюдалось достоверное увеличение обеих ее долей различной степени выраженности (табл. 2).
| Показатель | Течение муковисцидоза | |
|---|---|---|
| средней тяжести (n=22) | тяжелое (n=16) | |
| Размеры печени: правая доля левая доля |
+12,8±0,4* +19,3±0,5* |
+18,6±0,9*ˆ +25,5±1,8* |
| Размеры селезенки: продольный поперечный |
+1,5±0,4 +0,5±0,1 |
+28,2±2,6*ˆ +20,1±2,2*ˆ |
Так, в первой группе пациентов со средней тяжестью течения муковисцидоза увеличение верхненижнего размера для левой доли в среднем по группе составило 19,3±0,5 % и для правой доли - 12,8±0,4 % по сравнению с контрольной группой. Во второй группе с тяжелым течением муковисцидоза отмечалось увеличение левой доли на 25,5±0,8 % и правой - на 18,6±0,3 %. У 18 детей первой группы и у всех детей второй группы паренхима печени была гиперэхогенной и неоднородной. У 4 детей с течением муковисцидоза средней тяжести ультразвуковая картина печени соответствовала возрастной норме. Изменения структуры печени отличались большим разнообразием - от мелкоочаговой диффузной до крупноочаговой неоднородности (табл. 3).
| Тип неоднородности паренхимы | Течение муковисцидоза | |
|---|---|---|
| средней тяжести (n=22) | тяжелое (n=16) | |
| Мелкоочаговая | 3 | 2 |
| Среднеочаговая | 12 | - |
| "Тяжистость" | 3 | 6 |
| Крупноочаговая | - | 8 |
Так, у 5 детей из обеих групп имела место мелкоочаговая диффузная неоднородность паренхимы печени (рис. 3), что эхографически соответствовало признакам ее жировой инфильтрации [9-11]. Ведущая роль в оценке состояния паренхимы печени отводится морфологическим исследованиям, которые считаются "золотым стандартом" диагностики [9, 12]. Однако, несмотря на высокую информативность биопсии, она не может быть включена в алгоритм обследования больных муковисцидозом из-за своей травматичности и опасности осложнений. В наших исследованиях биопсия печени не проводилась, но по данным других авторов у всех больных муковисцидозом без клинических признаков цирроза печени отмечалась жировая дистрофия гепатоцитов [11, 12].
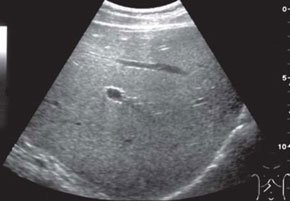
Рис. 3. Эхограмма печени ребенка с тяжелым течением муковисцидоза.
У детей с мелкоочаговой диффузной неоднородностью паренхимы печени (5 пациентов) изменений со стороны размеров и структуры паренхимы селезенки не наблюдалось. Допплерографические показатели кровотока как по сосудам портальной системы, так и сосудам чревного ствола были в пределах нормальных значений соответственно возрасту пациентов. Кровоток по средней печеночной вене имел нормальную трехфазную форму.
Помимо увеличения печени и мелкоочаговой диффузной неоднородности ее паренхимы у этих же детей определялось увеличение размеров и гиперэхогенность паренхимы поджелудочной железы. Такое сочетание эхо-признаков обычно наблюдается у больных сахарным диабетом. Клинико-лабораторных подтверждений признаков так называемого муковисцидозозависимого сахарного диабета выявлено не было, но у этих детей имело место нарушение толерантности глюкозы. Так, по данным Н.Ю. Каширской [10], у больных муковисцидозом отмечается хорошее всасывание углеводов, но метаболизм их может быть нарушен вплоть до развития сахарного диабета. Автор наблюдала нарушение толерантности глюкозы у 53 % больных, а инсулинозависимый сахарный диабет (муковисцидозозависимый тип) как манифестную форму эндокринного поражения поджелудочной железы - у 1 % больных.
У 12 пациентов первой группы паренхима печени характеризовалась среднеочаговой диффузной неоднородностью, причем у 8 из них визуализировался просвет внутрипеченочных желчных протоков (1-2 мм), стенки их были гиперэхогенными. Желчный пузырь у этих больных был деформирован, увеличен, сократительная функция пузыря в пробе с желчегонным завтраком была снижена, стенки пузыря утолщены до 2-3 мм. Ультразвуковые размеры селезенки, ее паренхима, диаметр селезеночной вены и допплерографические параметры кровотока в среднем по группе были в пределах возрастной нормы. Такая эхографическая картина могла соответствовать как признакам дискинезии желчевыводящих путей, так и хронического гепатита В, возникновение которого нельзя исключить у детей с муковисцидозом [9]. Однако, учитывая клинико-лабораторные данные: отсутствие маркера хронического гепатита В, нормальные уровни АЛТ и АСТ, повышение щелочной фосфотазы в среднем до 460 ед/л, такое состояние было расценено как дискинезия желчевыводящих путей с явлениями холестаза. По данным Н.Ю. Каширской [10], у 3 % детей с муковисцидозом выявлялись маркеры хронического гепатита В и хронического гепатита С. Автор считает, что больным муковисцидозом как группе риска по инфицированию вирусными гепатитами, передающимися преимущественно парентеральным путем, показано проведение профилактической вакцинации.
У 9 из 12 пациентов на фоне среднеочаговой диффузной неоднородности паренхимы печени определялись гиперэхогенные тяжи по ходу ветвей воротной вены равномерно и неравномерно утолщенные (рис. 4), что указывало на наличие фиброза различной степени выраженности.
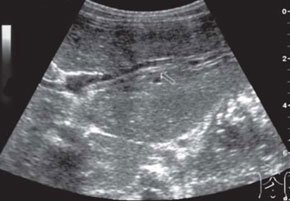
Рис. 4. Эхограмма печени ребенка с течением муковисцидоза средней тяжести.
В наших предыдущих исследованиях проводилось сопоставление ультразвуковых и морфологических данных у детей с хроническим гепатитом различной этиологии и было установлено, что равномерно утолщенные тяжи соответствуют минимально выраженному фиброзу и неравномерно утолщенные - признакам тяжелого фиброза [9]. Увеличение продольного размера селезенки у 9 детей с признаками фиброза в среднем составило 10 % по сравнению с данными контрольной группы, отмечалось достоверное увеличение объемного кровотока по воротной вене и повышение индекса резистентности в общей печеночной артерии. Изменения допплерографических параметров в селезеночных сосудах не были достоверными (табл. 4). Кровоток по средней печеночной вене был трехфазным у 4 пациентов и двухфазным - у 5 детей с признаками фиброза.
| Показатель | Течение муковисцидоза | ||
|---|---|---|---|
| средней тяжести (n=22) | тяжелое (n=16) | ||
| без признаков фиброза (n=13) | с признаками фиброза (n=9) | ||
| Объемный кровоток: воротная вена селезеночная вена |
+4,3±1,8 +2,5±0,8 |
+12,6±2,2* +8,3±1,6 |
+32,5±3*ˆ +20,4±2,4*ˆ |
| Индекс резистентности: общая печеночная артерия селезеночная артерия |
+4,8±1,6 +3,2±1 |
+9,2±1,5* +6,8±1,4 |
+16,1±1,9*ˆ +22,4±2,9*ˆ |
Выраженная "тяжистость" печеночного рисунка вследствие множественных гипоэхогенных участков паренхимы, размер которых составил от 7 до 15 мм, между гиперэхогенными тяжами по ходу сегментарных ветвей воротной вены неравномерно утолщенных (рис. 5 а) определялась у 9 пациентов обеих групп (см. выше). Эти изменения паренхимы печени напоминали эхографическую картину при аутоиммунном гепатите и соответствовали морфологической картине выраженного фиброза [13, 14]. У этих детей отмечалось увеличение продольного размера селезенки в среднем на 15 %, расширение ствола воротной и селезеночной вены. Допплерографические показатели достоверно отличались от должных величин, что косвенно подтверждало их зависимость от степени выраженности фиброза.
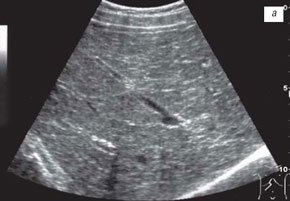
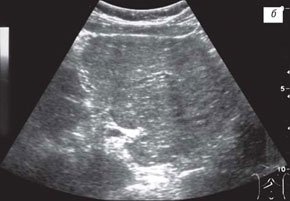
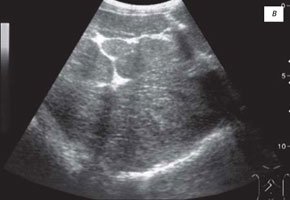
Рис. 5. Эхограммы печени ребенка с тяжелым течением муковисцидоза.
У 8 детей второй группы с тяжелым течением муковисцидоза паренхима печени имела крупноочаговую неоднородность. Контур печени был неровный из.за дольчатости, которая была связана с выраженной гиперэхогенностью межсегментарных перегородок. В паренхиме печени определялись единичные и множественные изоэхогенные узлы размером от 8 до 32 мм на фоне неравномерно утолщенных тяжей по ходу сегментарных ветвей воротной вены (рис. 5 в). Продольный размер селезенки у всех детей этой группы был увеличен и в среднем составил 28,2±2,6 % по сравнению с контрольной группой (см. табл. 2). У 3 из 8 пациентов селезенка имела округлую форму, т.е. продольный и поперечный размеры были равныПаренхима селезенки характеризовалась выраженной неоднородностью и гиперэхогенностью. Визуализировались множественные внутриорганные ветви селезеночной вены с гиперэхогенными стенками. Дополнительные дольки селезенки диаметром 5 и 11 мм в области ее нижнего полюса определялись у 2 детей. Допплерографические показатели косвенно свидетельствовали о развитии портальной гипертензии: увеличение объемного кровотока по сосудам портальной системы в основном за счет расширения диаметра стволов воротной и селезеночной вены, наличие кровотока по пупочной вене (у 2 детей), повышение индекса резистентности в сосудах чревного ствола (см. табл. 3). Кровоток по средней печеночной вене имел двухфазную и линейную формы. Желчный пузырь при этом у 2 пациентов был небольших размеров с утолщенными стенками до 8-14 мм и варикозным расширением их сосудов (см. рис. 1б). Одновременно определялось утолщение стенок пилорического отдела желудка, их слоистость и варикоз сосудов в них, что подтверждалось данными гастроскопии. Все это также свидетельствовало о признаках портальной гипертензии. Учитывая клинико-лабораторные и ультразвуковые данные у 8 (50 %) детей с тяжелым течением муковисцидоза, был диагностирован цирроз печени с признаками портальной гипертензии. Полученные результаты согласуются с данными других авторов, которые отмечали цирроз печени у 4 (53 %) больных с муковисцидозом [4, 7, 10, 11, 14, 15].
Исследования показали, что выявленные изменения гепатобилиарной системы, поджелудочной железы и сердца отражают механизмы патогенеза и динамику течения муковисцидоза у детей. Респираторный синдром влечет за собой гипоксемию, гиперкапнию, снижение вентиляционной способности легких и как следствие этих процессов развивается хроническое легочное сердце. Степень выраженности бивентрикулярной недостаточности отражает динамику течения муковисцидоза.
Изменения поджелудочной железы (увеличение размеров, неоднородность и гиперэхогенность паренхимы) имели место у 68 % детей с течением муковисцидоза средней тяжести и у 100 % детей с тяжелым течением муковисцидоза. Эти изменения можно объяснить нарушениями образования и выделения электролитной фракции панкреатического сока, который приобретает вязкую консистенцию за счет высокой концентрации макромолекулярных веществ. Все остальные процессы в поджелудочной железе вторичны и связаны с замедлением оттока секрета, действием мощных протеаз, что влечет за собой сначала ее увеличение с повышением эхогенности и появлением неоднородности паренхимы, а затем уменьшение размеров и образованием кист и кальцинатов.
Недостаточное образование электролитной фракции желчи вызывает сгущение органических веществ в ней с развитием холестаза в печеночных протоках и образованием склерозированного желчного пузыря, утолщением и уплотнением его стенок, уменьшением его размера и конкрементами в просвете пузыря [8, 10-12]. По данным ряда авторов, холестаз может привести к возникновению гепатита с последующим развитием фиброза и цирроза печени. Считают, что очаговый билиарный фиброз является патогномоничным поражением печени при муковисцидозе [8, 10, 11, 15].
Результаты нашего исследования показали, что неоднородность паренхимы печени у детей с муковисцидозом менялась по мере прогрессирования заболевания. Мелкоочаговая и среднеочаговая диффузная неоднородность с минимально выраженным фиброзом наблюдалась у 68 % больных со средней тяжестью течения муковисцидоза. "Тяжистость" печеночного рисунка и крупноочаговая неоднородность вплоть до развития цирроза печени имела место у 87 % детей с тяжелым течением муковисцидоза. Распространение фиброза вызывает одно из ранних осложнений - мультинодулярный цирроз печени с последующей портальной гипертензией. Это осложнение следует диагностировать как можно раньше, чтобы по возможности избежать значительного варикозного расширения вен пищевода: определение уровня щелочной фосфотазы гамма-глютамилтранферазы, проведение УЗИ и фиброэндоскопии [16]. По результатам нашего исследования фиброз различной степени выраженности наблюдался у 67 % детей с муковисцидозом и у 50 % из них сформировался цирроз печени. По данным других авторов, признаки фиброза встречаются практически у всех больных муковисцидозом, и у 4 (53 %) пациентов они приводят к развитию цирроза печени с синдромом портальной гипертензии, когда единственным радикальным методом лечения может быть трансплантация печени [4, 7, 11, 12, 14-16]. Морфологические данные подтверждают признаки биларного цирроза печени: белковая и белковолипоидная дистрофия гепатоцитов, расширение и фиброз портальных трактов, нарушение балочного строения печеночной дольки, пролиферация желчных протоков, образование ложных долек, умеренно выраженная воспалительная инфильтрация [10, 11].
Поражение гепатобилиарной системы отражает тяжесть течения муковисцидоза, но клинические проявления встречаются относительно редко. Нарушения функции печени умеренные, так как сохраняется достаточное количество неповрежденных печеночных клеток. По данным Т.Е. Гембицкой [17], наиболее частым симптомом поражения печени является гепатомегалия, которая отмечалась у 30 % больных с муковисцидозом, но при этом автор предостерегает, что не следует забывать о гепатоптозе, обусловленном эмфиземой легких. В наших исследованиях измерение верхненижнего размера долей печени исключает это. Учитывая бессимптомность или субклиническое течение поражений печени у больных муковисцидозом, диагностический поиск этой патологии должен быть активным и с целью раннего выявления этих изменений большое значение приобретают лабораторные исследования и, в частности, ультразвуковое исследование и сцинтиграфия печени с 99mТс [17].
Выводы
Таким образом, комплексная ультразвуковая оценка состояния паренхимы печени и кровотока по сосудам портальной системы и сосудам чревного ствола позволяет уточнить степень выраженности фиброза в ткани печени и выявить начальные признаки портальной гипертензии. Допплерографические и ЭхоКГ параметры могут быть использованы как дополнительные критерии диагностики тяжести течения муковисцидоза. У всех больных муковисцидозом независимо от тяжести и длительности заболевания рекомендуется регулярно, не менее 1 раза в 6 мес, проводить полное клинико-лабораторное обследование, включающее ультразвуковое исследование сердца, гепатобилиарной системы, поджелудочной железы и допплерографическое исследование сосудов портальной системы и чревного ствола с целью коррекции проводимой терапии.
Литература
- Капранов Н.И., Каширская Н.Ю., Воронкова А.Ю. и др. Муковисцидоз. Современные достижения и актуальные проблемы // Методические рекомендации. - М., 2005. - C. 110.
- Симонова О.И. Кинезитерапия в комплексном лечении больных муковисцидозом // Автореф.дисс. … д.ра мед. наук. - М., 2001. - 43 с.
- Капранов Н.И., Рачинский С.В. Муковисцидоз. - М.: Медицина, 1995. - 187 с.
- Каширская Н.Ю., Капранов Н.И. Состояние системы пищеварения при муковисцидозе // Сб. ст. и тезисов. 6-й Национальный конгресс по муковисцидозу. - Санкт.Петербург, 2003.- С. 15.19.
- Неретина А.Ф., Ульянова Л.В., Клокова В.М. и др. Ошибки диагностики муковисцидоза у детей // Сб. ст. и тезисов XII конгресса по болезням органов дыхания. - М., 2002. - С. 20.24.
- Капранов Н.И. Течение и исход муковисцидоза у детей при современных методах лечения и реабилитации // Автореф. дисс. … д.ра мед. наук. - М., 1986. - 53 с.
- Vaughn D.D, Jabra A.A., Fishman E.K. Pancreatic disease in children and young adult // Radiographics. - 1998. - (Vol. 18. (5): 1171.87.
- Делягин В.М., Капранов Н.И., Каширская Н.Ю. и др. Лучевая диагностика поражений печени, желчного пузыря и поджелудочной железы при муковисцидозе у детей // SonoAce International. 2003. - N 11. - С. 48.53.
- Дворяковская Г.М., Якушенко С.М., Дворяковский И.В и др. Сравнительный анализ данных ультразвукового и морфологического исследований печени при хронических гепатитах у детей // Ультразвуковая и функциональная диагностика. - 2005. - N 1. - С. 39.48.
- Каширская Н.Ю. Состояние желудочно-кишечного тракта, поджелудочной железы и гепатобилиарной системы у больных муковисцидозом // Автореф. дисс. … д.ра мед. наук.-М., 2001. - 46 с.
- Akata D., Akhan O., Ozselic U. et al. Hepatobiliary manifestation of cystic fibrosis in children // Eur.J.Radiol. - 2002. - Vol. 41. - N 1: 26.33.
- Cadranel J.F., Rufat P., Degos F. Practices of liver byopsy in Franse: result of prospective nationwide survey // Hepatology. - 2000. - Vol. 32.- N3.- P. 477.481.
- Дворяковская Г.М., Гундобина О.С., Дворяковский И.В., Каганов Б.С. Ультразвуковая оценка эффективности терапии при аутоиммунном гепатите у детей // Ультразвуковая и функциональная диагностика. - 2005. - N 4. - С. 44.51.
- Patricuin H., Lenaerts C., Smith L. et al. Liver disease in children with cystic fibrosis // Radiology. - 1999. - Vol.211. - N 4.- Р. 229.32.
- Капустина Т.Ю. Изменения печени и их коррекция при муковисцидозе у детей на современном этапе // Автореф. дисс. … канд. мед. наук. - М., 2001. - 22 с.
- Жан Фейжельсон, Ж..П. Шазалетт, Иветт Пеко и др. Билиарный мультинодулярный цирроз печени при муковисцидозе // Сб. ст. и тезисов. 6.й Национальный конгресс по муковисцидозу. - СПб, 2003. - 63 с.
- Гембицкая Т.Е., Усенко О.В., Шабров А.В. Клинико-лабораторные особенности билиарного цирроза печени у взрослых больных муковисцидозом, методы лечения // Сб. ст. и тезисов. 6.й Национальный конгресс по муковисцидозу. - СПб, 2003.- С. 19.22.

УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Публикации по теме
- Ультразвуковой контроль при катетеризации центральных вен у детей - Быков М.В.
- Ультразвуковая диагностика щитовидной железы и надпочечников у детей с кардиомиопатиями - Дворяковская Г.М.
- Ультразвуковая диагностика в оценке состояния детей при муковисцидозе - Дворяковская Г.М.
- Клинико-эхографические особенности воспалительных процессов внутренних половых органов у девочек - Мартыш Н.С.
- Ультразвуковая оценка полиорганных изменений у детей с почечной недостаточностью - Ольхова Е.Б.

