Эхография и допплерометрия для оценки эффективности лечения женщин с преждевременной недостаточностью яичников
Рубрика: Эхография в гинекологии
УЗИ сканер RS80
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Введение
Преждевременное угасание функции яичников - сложный, многофакторный и продолжительный процесс. Термином "преждевременная недостаточность яичников" (ПНЯ) обозначают комплекс симптомов, формирующийся у женщин моложе 40 лет и включающий аменорею, признаки выраженного эстрогендефицита и бесплодие при повышенном уровне гонадотропинов (ФСГ, ЛГ) [1, 20]. В литературе обсуждается возрастной диапазон, который делает правомерным установление диагноза преждевременная недостаточность яичников. Возрастом формирования ПНЯ считают 35-43 года [8, 18, 19, 22], но большинство исследователей указывают на возраст до 40 лет [6].
В основе данной патологии, независимо от этиологического фактора, лежит несвойственное этому возрастному периоду уменьшение запаса примордиальных фолликулов вплоть до его полного истощения и формирования афолликулярного типа ПНЯ. Это состояние описывается как "многофакторный синдром", обусловленный хромосомными аномалиями, генетическими нарушениями, ферментопатиями, инфекционными и ятрогенными факторами [14, 18]. Только в 5-10% случаев и лишь при наличии фолликулярного типа патологии, когда в яичниках обнаруживаются отдельные фолликулы, женщины с ПНЯ могут забеременеть [23, 28]. Согласно данным литературы у пациенток с ПНЯ беременности могут наступать на фоне приема эстрогенов и в циклах отмены КОК [27]. Так, Alper [5] описал беременности у 6 пациенток с ПНЯ: 2 пациентки забеременели на фоне приема конъюгированных эстрогенов, 2-на фоне отмены оральных контрацептивов и 2 пациентки забеременели спонтанно. Возможно, что частота наступления беременности зависит от возраста начала заболевания. Экзогенное введение эстрогенов сенсибилизирует клетки гранулезы, что по механизму обратной связи блокирует ФСГ и приводит к овуляции [6]. Комбинированные оральные контрацептивы действуют по механизму обратной связи на ЛГ- и ФСГ-рецепторы [11]. Однако исследования, посвященные использованию КОК для подавления гонадотропинов, показали, что эти препараты на фолликулярную активность не влияют [9].
Существует прямо пропорциональная зависимость между пулом примордиальных и числом растущих фолликулов, поэтому при снижении числа первых уменьшается размер когорты фолликулов, ежемесячно отбираемых в овуляторном цикле. Прижизненно объективно оценить овариальный пул невозможно, поэтому необходимы косвенные методы его определения. По мнению некоторых авторов [24, 29] наряду с гормональными методами основным методом является эхография, включающая определение объема яичника и числа антральных фолликулов и дополненная цветовым допплеровским картированием яичникового кровотока (ЦДК). Установлено, что объем яичника менее 3 см3 [29] и наличие в яичнике менее 5 антральных фолликулов являются неблагоприятным прогностическим признаком овариального резерва [24]. Число антральных фолликулов, обнаруженных с помощью трансвагинальной эхографии, отражает оставшийся пул "отдыхающих" примордиальных фолликулов, что подтверждается рядом работ, основанных на гистологических исследованиях, в которых была доказана прямая зависимость между числом примордиальных и растущих фолликулов [24, 29].
Репродуктивная система женщины уникальна тем, что в гормонально зависимых органах синхронно с гормональными фазами происходят выраженные колебания сосудистоготонуса. Адекватное кровоснабжение крайне необходимо для нормального функционирования яичников [3, 4]. Изменение кровотока в них связано с системным и локальным колебаниями уровней гормонов. Питание малых примордиальных фолликулов происходит за счет близко расположенных стромальных сосудов. Снижение овариального кровотока, выявленное с помощью цветового допплеровского картирования, а не повышение уровня ФСГ, является более ранним маркером сниженного овариального резерва. Сниженное кровоснабжение яичника в свою очередь может приводить к резистентности яичника на гормональную стимуляцию и формирование яичниковой недостаточности.
В настоящее время для коррекции ранних, средневременных и поздних обменных нарушений, свойственных ПНЯ [1], назначают заместительную гормонотерапию. При этом используют препараты, в состав которых входят натуральные эстрогены в дозировках, временно обеспечивающих поддержание их концентрации в плазме крови на уровне ранней фолликулярной фазы менструального цикла.
Цель данного исследования - оценка изменения кровоснабжения яичников с помощью цветового допплеровского картирования кровотока в яичниковой артерии и ее стромальных ветвях и эхографическая характеристика органов малого таза у пациенток с ПНЯ, принимающих заместительную гормонотерапию.
Материалы и методы
Были обследованы 78 женщин с преждевременной недостаточностью яичников в возрасте от 18 до 40 лет (средний возраст 34,8±3,25) до и после 12 месяцев приема заместительной гормонотерапии. В контрольную группу вошли 10 женщин репродуктивного возраста с сохраненным ритмом менструации, которым эхография органов малого таза проводилась на 3-й день цикла. Уровни гормонов (ФСГ, ЛГ, Е2 и Т) определяли методом ИФА с помощью соответствующих тест-систем на автоматическом анализаторе "Cobar Core II". Трансвагинальное ультразвуковое исследование органов малого таза с ЦДК яичникового кровотока проводилось на аппарате экспертного класса с использованием мультичастотного трансвагинального датчика с частотой 8 - 6 - 4 МГц в режиме сканирования двумерной серой шкалы (B-mode), цветового допплеровского картирования (C-mode) и импульсного спектрального допплеровского режима (D-mode). При трансвагинальной эхографии органов малого таза вычисляли объем яичников и проводили подсчет антральных фолликулов в них, кроме того, измеряли размеры тела матки и изучали состояние эндометрия. При ЦДК визуализировали цветовые локусы, соответствующие расположению сосудов, и оценивали особенности их васкуляризации. Для получения допплеровской кривой выбирали локусы, размер и окно цветового допплеровского картирования, которые строго соответствовали обследуемой зоне. Угол цветового картирования был менее 60°С. Базовая линия устанавливалась по центру скоростной шкалы. Мощность выбирали максимальной, при которой не было артефактов. Для подавления возникающих шумов (цветовых артефактов) использовали частотный фильтр.
Анализ кривой скорости кровотока (КСК) проводили на протяжении не менее двух последовательных сердечных циклов. Полученные данные затем усредняли. При исследовании доллеровской кривой обращали внимание на особенности ее формы: тип А - диастолический кровоток присутствует на протяжении всего сердечного цикла, тип В - отсутствует поздний диастолический кровоток, тип С - отсутствует ранний диастолический кровоток, тип D - диастолический кровоток отсутствует в раннюю диастолу, присутствует в среднюю и отсутствует в позднюю диастолу, тип 0 - диастолический кротовок полностью отсутствует [3].
Для количественной интерпретации спектральных кривых скоростей кровотока использовали индекс резистентности (ИР), пульсационный индекс (ПИ) и пиковую систолическую скорость кровотока (ПСС).
Заместительная гормонотерапия пациенткам с преждевременной недостаточностью яичников проводилась трехфазным препаратом дивисек (фирма Орион Фарма, Финляндия). Эстрогенный компонент в нем представлен эстрадиолом валеаратом, а гестагенный - медроксипрогестероном ацетатом (МПА). Выбор данного препарата обусловлен тем, что в его состав входит гестаген с частичной андрогенной активностью. Согласно проведенному ранее исследованию [16] у пациенток, получающих в качестве эстрогена эфир эстрадиола (в данном случае эстрадиол валерат), расстройства аффективного спектра регрессируют быстрее, чем у пациенток, принимавших конъюгированные эстрогены. Трехфазный режим приема дивисека позволяет избежать возобновления симптомов недостатка половых гормонов, возникающих в дни ожидаемых менструальноподобных реакций при двухфазном режиме. Препарат также активно предупреждает потерю костной ткани, которая сопровождает эстрогендефицитные состояния.
Мы назначали препарат дивисек в непрерывном режиме в течение 12 месяцев.
Статистическая обработка данных выполнена на компьютере с помощью электронных таблиц "Microsoft Excel" и пакета прикладных программ "Statistica for Windows" v. 7.0, StatSoft Inc. (США).
Результаты
Проведено проспективное клинико-лабораторное обследование 78 пациенток с ПНЯ (средний возраст 34,8±3,25 года). К моменту проведения исследования длительность заболевания составила 5,5±1,4 года, а возраст начала заболевания - 29,1±3,3 года. Начало нарушений ритма менструаций пришелся на возраст 27,3±1,1 года.
Среди причин, приведших к развитию ПНЯ, пациентки наиболее часто отмечали стрессовые факторы (26,92%), хотя у большинства больных (53,85%) непосредственную причину возникновения ПНЯ установить не удалось.
Начало заболевания по типу олигоаменореи выявлено у большинства пациенток (92,3%), только у 7,7% было внезапное прекращение менструаций по типу стойкой аменореи.
Все больные с ПНЯ предъявляли жалобы на вторичную аменорею, 58 (74,35%) - на повышенную утомляемость, 56 (71,8%) - на приливы, 53 (67,9%) - на бесплодие, 34 (43,6%) - на снижение либидо, 15 (19,23%) - на сухость во влагалище, 13 (16,67%) - на головокружение, 5 (6,41%) - на частое мочеиспускание, 5 (6,41%) - на прибавку в весе, 4 (5,13%) - на повышение артериального давления.
Выраженность симптомов дефицита половых гормонов по индексу Куппермана (15,75±1,4 балла) расценивалась как средне-тяжелая.
Средний уровень ЛГ и ФСГ у больных с ПНЯ значительно превышал нормативные показатели для женщин репродуктивного возраста, составляя 90,8±5,4 и 115,8±5,2 МЕ/л соответственно. Концентрация эстрадиола (76,7±10,7 пмоль/л) у женщин с ПНЯ была значительно ниже нормативных показателей ранней фолликулиновой фазы у женщин с регулярными менструациями, при этом у 54 (69,23%) пациенток уровень эстрадиола не превышал 70 пмоль/л и в среднем составил 52,9±14,6 пмоль/л. Интересно отметить, что в среднем по группе у женщин с ПНЯ уровень тестостерона составил 0,9±0,09 нмоль/л, а у 60,3% больных находился в пределах 0,2-0,9 нмоль/л и составил 0,61±0,1 нмоль/л, что расценивается как стойкое гипоандрогенное состояние.
Для изучения размеров и внутренней структуры яичников 78 женщинам с ПНЯ была осуществлена трансвагинальная эхография органов малого таза (табл. 1) (рис. 1).
| Показатель | Основная группа (78 пациенток) |
Контрольная группа (10 пациенток) |
|---|---|---|
| Визуализация яичников с обеих сторон | 67 (85,9%) | 10 (100%) |
| Визуализация яичников только справа | 5 (6,4%) | - |
| Визуализация яичников только слева | 5 (6,4%) | - |
| Яичники не визуализируются с обеих сторон | 1 (1,28%) | - |
| Объем правого яичника, см3 | 1,82+0,21* | 5,8+1,7 |
| Объем левого яичника, см3 | 1,81+0,26* | 6,1+1,4 |
| Фолликулярный тип ПНЯ | 41 (53,3%)* | 10(100%) |
| До 5 антральных фолликулов | 31 (75,6%) | - |
| 5-10 антральных фолликулов | 10(24,4%)* | 10(100%) |
| Среднее число антральных фолликулов на яичник | 3,6+1,1* | 6,5+1,9 |
| Афолликулярный тип ПНЯ | 36 (46,7%) | - |
| Объем тела матки, см3 | 24,8+2,27* | 47,1+2,1 |
| М-эхо, см | 0,3+0,07 | 0,4+0,01 |
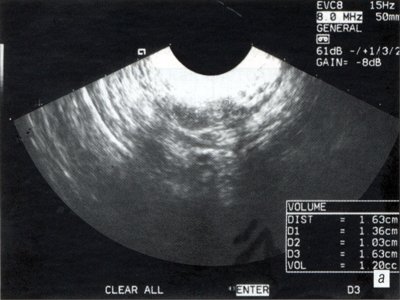
а) До лечения.
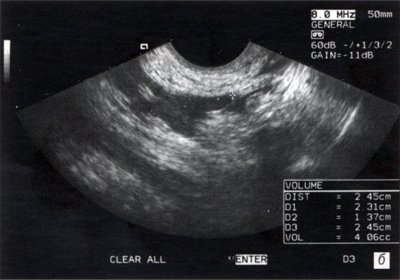
б) После 12 месяцев приема заместительной гормонотерапии.
Нужно отметить, что у 50 (64,5%) пациенток с ПНЯ объемы правых яичников, а у 52 (67,5%) объемы левых яичников не превышали 2 см3, составляя 1,14±0,09 и 1,08±0,05 см3 соответственно.
ЦДК кровотока в воротах и строме яичников выполнено 77 (98,7%) пациенткам, так как у одной пациентки не удалось визуализировать оба яичника. У 7 (9,1%) пациенток при проведении цветового допплеровского картирования не удалось обнаружить кровоток в воротах, а, следовательно, и в строме обоих яичников (т.е. отсутствовал как систолический, так и диастолический компонент - тип кривой N). У 3 (3,9%) пациенток кровоток в воротах яичников не визуализировался справа, а у 15 (19,5%) пациенток - слева. Таким образом, кровоток в воротах яичников удалось обнаружить у 67 (87%) женщин с ПНЯ справа и у 55 (71,4%) пациенток с ПНЯ слева. У 8 (10,25%) пациенток кровоток в стромальных ветвях яичниковой артерии не визуализировался с обеих сторон, у 4 (5,1%) пациенток - справа, а у 10 (10,28%) - слева. Следовательно, визуализировать кровоток в строме яичников удалось у 55 (71,4%) пациенток справа и у 37 (48%) пациенток слева.
В 33% случаев имело место полное отсутствие диастолического кровотока (тип кривой 0), в 43% случаев отсутствовал ранний диастолический кровоток (тип кривой А), что свидетельствовало о возможных ишемических процессах ткани яичника. В 8% случаев отсутствовал поздний диастолический кровоток (форма кривой В) и в 16% случаев диастолический кровоток присутствовал на протяжении всего сердечного цикла (тип кривой С).
При ЦДК было выявлено достоверное повышение индексов сосудистого сопротивления (ПИ и ИР) в яичниковой артерии и в ее стромальных ветвях в основной группе по сравнению с контрольной группой (табл. 2).
| Показатель | Пациентки с ПНЯ | Контрольная группа | ||
|---|---|---|---|---|
| Правый яичник | Левый яичник | Правый яичник | Левый яичник | |
| Ворота яичников | ||||
| n=67 | n=55 | n=10 | n=10 | |
| ПИ | 2,31+0,3* | 2,8+0,7* | 1,1+0,09 | 1,0+0,08 |
| ИР | 1,46+0,2* | 0,81+0,1* | 0,71 ±0,1 | 0,67±0,1 |
| ПСС, м/с | 0,09+0,01 | 0,08+0,02 | 0,15+0,02 | 0,13+0,01 |
| Строма яичников | ||||
| n=55 | n=37 | n=8 | n=9 | |
| ПИ | 3,49+0,2* | 2,9+0,13* | 0,8+0,2 | 0,9+0,22 |
| ИР | 1,3+0,09* | 0,88+0,08* | 0,53+0,09 | 0,55+0,07 |
| ПСС, м/с | 0,09+0,01 | 0,1+0,02 | 0,15+0,02 | 0,14±0,01 |
Наравне с повышением индексов сопротивления сосудистого русла у пациенток с ПНЯ недостоверно снижено ПСС по сравнению с ПСС у женщин с регулярным менструальным циклом.
Во время цветового допплеровского картирования было установлено, что в группе с афолликулярным типом ПНЯ отмечается более существенное снижение кровотока в яичниковой артерии. Это, по-видимому, обусловлено более выраженной эстрогенной недостаточностью (табл. 3).
| Показатель | Фолликулярный тип ПНЯ (41 пациентка) |
Афолликулярный тип ПНЯ (36 пациенток) |
|---|---|---|
| Уровень Е2, пмоль/л | 107,6+23,61* | 62,3+5,98 |
| Уровень ФСГ, МЕ/л | 101+13,5 | 112+11,5 |
| ПИ стромы правого яичника | 2,99+0,53* | 3,5+0,67 |
| ИР стромы правого яичника | 0,89+0,03* | 1 ,38+0,03 |
| ПИ стромы левого яичника | 3,38+0, 34* | 2,71+0,37 |
| ИР стромы левого яичника | 0,87+0,03 | 0,9+0,03 |
| ПИ ворот правого яичника | 1,63+0,13 | 2,3+0,5 |
| ИР ворот правого яичника | 1 ,2+0,05* | 1 ,88+0,07 |
| ПИ ворот левого яичника | 2,5+0,47* | 2,9+0,54 |
| ИР ворот левого яичника | 1 ,02+0,06* | 1,34+0,09 |
Всем 78 пациенткам с ПНЯ для купирования ранних (а в ряде случаев и поздних) симптомов дефицита половых гормонов была рекомендована заместительная гормонотерапия. Во время приема препарата у всех пациенток наступала закономерная менструальноподобная ответная реакция, ациклических кровянистых выделений не наблюдалось.
Через 12 месяцев приема дивисека у пациенток определяли индекс Куппермана. Он составил 5,1±1,3 балла, что говорит о восполнении недостающих половых гормонов. Это было также подтверждено гормональными исследованиями (табл. 4).
| Показатель | Среднее значение | Р | |
|---|---|---|---|
| до лечения | после лечения | ||
| ФСГ, МЕ/л | 116+41,8 | 47,4+10,14 | <0,05 |
| ЛГ, МЕ/л | 90,8+36,8 | 51,15+7,17 | <0,05 |
| Е2, пмоль/л | 76,7+10,7 | 252,3+31,7 | <0,05 |
| Т, нмол/л | 0,9+0,28 | 1,1+0,16 | <0,05 |
Как видно из табл.4, после 12 месяцев приема дивисека уровень ЛГ снизился почти в 2 раза и составил 51,15±11,4 МЕ/л, ФСГ - более, чем в 2 раза (47,4±9,8 МЕ/л).
Одновременно с падением уровня гонадотропинов уровень Е2 вырос в 2,2 раза (252,3±31,7 пмоль/л). На фоне терапии мы добились также повышения уровня тестостерона примерно на 20% (с 0,9±0,28 до 1,1 ±0,16 нмоль/л).
После заместительной гормонотерапии 42 пациенткам с ПНЯ проведена динамическая трансвагинальная эхография органов малого таза в сочетании с ЦДК яичникового кровотока. При этом было выявлено увеличение объемов яичников на 32-80%, тела матки - на 35%, а также относительное улучшение показателей овариального резерва (табл. 5).
| Показатель | Исходные данные (78 пациенток) |
Через 12 месяцев проведения ЗГТ (42 пациентки) |
|---|---|---|
| Объем правого яичника, см3 | 1,82+0,21* | 2,37+0,75 |
| Объем левого яичника, см3 | 1,81+0,26* | 3,22+0,63 |
| Фолликулярный тип ПНЯ | 41 (53,3%)* | 31 (73,8%) |
| До 5 антральных фолликулов | 35 (85,4%) | 35 (83,3%) |
| 5-10 антральных фолликулов | 10(24,4%)* | 6(14,2%) |
| Среднее число антральных фолликулов на яичник | 3,6+1,1* | 5,1+1,1 |
| Афолликулярный тип ПНЯ | 36 (46,7%) | 11 (26,2%) |
| Объем тела матки, см3 | 24,8+2,27* | 33,4+3,34 |
| М-эхо, см | 0,3+0,07 | 0,5+0,09 |
ЦДК кровотока в воротах и строме яичников выполнено 42 пациенткам. У 3 (7,1%) пациенток при проведении цветового допплеровского картирования не удалось обнаружить кровоток в воротах, а следовательно, и в строме обоих яичников (т.е. отсутствовал как систолический, так и диастолический компонент (тип кривой N). У одной (2,3%) пациентки кровоток не визуализировался в воротах правого яичника, а у 4 пациенток (9,5%) - в воротах левых яичников. Таким образом, кровоток в воротах удалось обнаружить у 38 (90,4%) женщин с ПНЯ справа, у 35 (83,3%) - слева. У 3 (7,1%) пациенток не визуализировался кровоток в строме обоих яичников, у 2 (4,7%) - справа, а у 4 (9,5%) - слева. Следовательно, визуализировать кровоток в строме яичников удалось у 33 (78,5%) пациенток справа и у 30 (71,5%) - слева.
В15% случаев отсутствовал поздний диастолический кровоток (тип кривой В) и в 26% диастолический кровоток присутствовал на протяжении всего сердечного цикла (тип кривой С). Форма кривой кровотока в большинстве случаев (29%) соответствовала типу 0 (полное отсутствие диастолического кровотока), в 30% - типу А (отсутствует ранний диастолический кровоток), что свидетельствовало об улучшении кровотока (в строме и воротах яичников) на фоне заместительной гормонотерапии.
В ходе исследования на фоне терапии было выявлено достоверное снижение показателей сосудистого сопротивления в воротах и в строме яичников (рис. 2, 3).
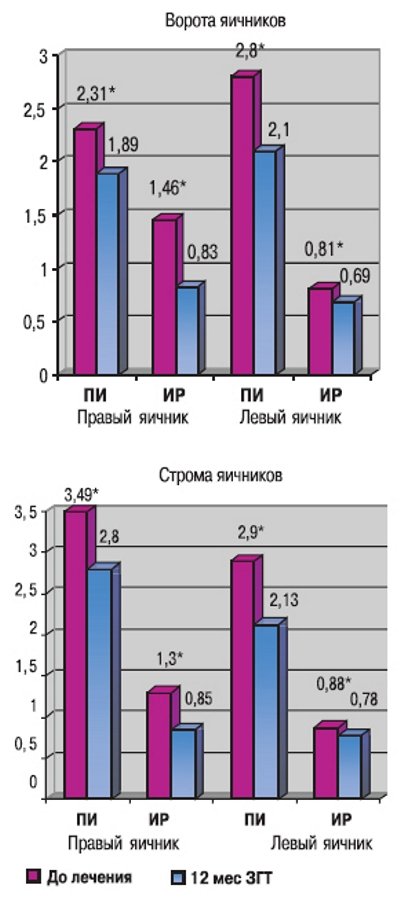
Рис. 2. Динамика показателей ЦДК после 12 месяцев приема заместительной гормонотерапии; * р<0,05.
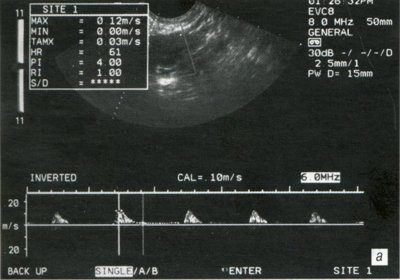
а) До лечения.
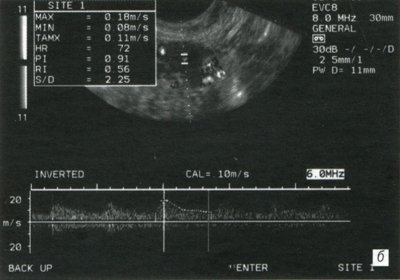
б) После 12 месяцев приема заместительной гормонотерапии.
При оценке показателей кровотока было установлено, что в группе женщин с фолликулярным типом ПНЯ на фоне ЗГТ происходит более существенное снижение показателей сосудистого сопротивления (табл. 6).
| Показатель | Тип ПНЯ | |
|---|---|---|
| фолликулярный | афолликулярный | |
| Уровень Е2, пмоль/л | 352,6+37,5* | 157,3+15,6 |
| Уровень ФСГ, МЕ/л | 40,7+11,3* | 54,3+8,9 |
| ПИ стромы правого яичника | 2,99+0,53* | 3,5+0,67 |
| ПИ стромы левого яичника | 2,25+0,33 | 2,57+0,32 |
| ИР стромы правого яичника | 0,89+0,03* | 1,38+0,03 |
| ИР стромы левого яичника | 0,77+0,08 | 0,79+0,13 |
| ПИ ворот правого яичника | 1 ,55+0,27* | 2,23+0,43 |
| ПИ ворот левого яичника | 2,5+0,47* | 2,9+0,54 |
| ИР ворот правого яичника | 0,82+0,19* | 0,98+0,27* |
| ИР ворот левого яичника | 1 ,02+0,06* | 1,34+0,09 |
Обсуждение
Результаты исследования показывают снижение объема овариального резерва у женщин с ПНЯ (до 1,82±0,21 и 1,81±0,26 см3 для правого и левого яичников соответственно) и числа антральных фолликулов (до 3,6±1,1 фолликулов на яичник). Они согласуются с данными, полученными раннее [17]. G.S. Conway [14] установил, что при ПНЯ фолликулярный тип патологии выявляется в 60% случаев. Мы обнаружили фолликулы у 53,3% женщин с ПНЯ, что свидетельствует о значительном снижении овариального резерва у обследованных больных.
Повышение индексов сопротивления сосудистого русла (ПИ, ИР) у женщин с ПНЯ в яичниковой артерии, а также в ее стромальных ветвях не противоречит данным L. Valentin [30]. В этой работе установлено, что при эстрогендефицитных состояниях, к которым относится ПНЯ, локусы кровотока обнаруживаются лишь в 61% случаев, при этом в 81% случаев выявляется повышение ПИ. Согласно данным Т.Н. Burne [10] у женщин в постменопаузе ПИ колеблется в пределах 3,1-6,6, что существенно превышает значения этого показателя у женщин репродуктивного возраста с сохраненной функцией яичников. В то же время Т. Dada и др. [15] считают, что косвенно состояние овариального резерва отражает другой индекс сопротивления сосудистого русла - ИР, так как при его повышении частота наступления беременности в программах ЭКО значительно снижается. Согласно данным X. Xiao [32], у женщин, страдающих бесплодием (при исключении трубного фактора), индекс ИР также повышен. Наравне с повышением индексов сопротивления сосудистого русла у наших пациенток с ПНЯ недостоверно снижен ПСС, что согласуется с данными работы [26].
У больных с ПНЯ на фоне проведения заместительной гормонотерапии препаратами, в состав которых входит гестаген с частичным андрогенным эффектом, было отмечено увеличение объемов яичников на 32-80%. Средний объем матки на фоне терапии увеличился на 35%. Полученные данные обусловлены ростом уровня Е2 (76,7±10,7 до 252,3±31,7 пмоль/л) и снижением ФСГ (с 116±41,8 до 47,4±10,14 МЕ/л), а также улучшением кровоснабжения органов малого таза, что подтверждается достоверным снижением показателей сосудистого сопротивления в воротах и в строме яичников, выявленным с помощью цветового допплеровского картирования. Наши данные согласуются с результатами исследования Н.А. Pan [25], который с помощью энергетического допплера выявил достоверное увеличение яичникового кровотока у женщин в постменопаузе после 3 мес назначения ЗГТ. С нашей точки зрения полученные результаты можно объяснить тем, что эстрогены являются эндогенными регуляторами ангиогенеза [7]. Как известно, ангиогенез не характерен для неповрежденных тканей организма взрослого человека в физиологических условиях и активизируется при патологическом росте тканей при опухолях, остром или хроническом воспалительном процессе, диабетической ретинопатии. Эндометрий и ткань яичника являются уникальным исключением из этого правила, так как процессы циклического ангиогенеза в них происходят ежемесячно. Эстрадиол, являясь эндогенным регулятором ангиогенеза, регулирует синтез NO, потенциального вазодилятатора, а также сосудисто-эндотелиального фактора роста, который стимулирует сосудистый рост в яичнике и обеспечивает быстрый рост капиллярной сети в процессе роста и селекции фолликулов.
Так, в период постменопаузы экспрессия сосудисто-эндотелиального фактора роста обнаруживается лишь в кистах, содержащих эпителий, и в серозных цистаденомах [21]. Следует отметить, что на местномуровне эстрадиол регулирует также и синтез эритропоэтина [31]. При улучшении кровоснабжения яичников улучшается питание фолликулов, благодаря чему они начинают расти. Так, фолликулярный тип ПНЯ был выявлен у 73,8% пациенток по сравнению с 53,3% до лечения, при этом у 35 (84,4%) пациенток визуализировалось до 5 антральных фолликулов, у 6 (15,5%) пациенток - до 10 антральных фолликулов, что свидетельствует об относительном улучшении показателей овариального резерва.
Вывод
Таким образом, трансвагинальная эхография в сочетании с цветовым допплеровским картированием является неинвазивной высокоинформативной методикой, позволяющей осуществлять динамический контроль за пациентками с ПНЯ, принимающими заместительную гормонотерапию.
Литература
- Сметник В.П., Кулаков В.И. Руководство по климактерию МИА.-2001. - С. 345-346, 368.
- Сметник В.П., Тумилович А.Г. Неоперативная гинекология.-М.: Медицинское информацион ное агентство.-2003.
- Федорова Е.В., Аипман А.Д. Применение цветового допплеровского картирования и допплерометрии в гинекологии.-М., 2002.
- Abulafia О., Sherer D. Angiogenesis of the ovary. Am. J.//Obstet. Gynecol.-2000.-Vol 182.-N1.-' P. 240-246.
- Alper MM., Jolly E.E. and Garner P.R. Pregnancies after premature ovarian failure // Obstet Gynecol.-1986.-P. 59-62, 67.
- Aubard, et al. Early menopause //Journal Clin Gynecoljgic Obstetrique et Biologic de la Reproduction.-1997. - Vol.26.-P. 231-237.
- AugustinH.G. Antiangiogenesic tumor therapy: will it work?-TiPS.-1998.-Vol.l9.-P. 216-222.
- Bjoro K. Amenorrhea: a study with particular attention to the problems of ovarian failure//Acta Obstetrica et Gynecologica Scandinavica.-1966. - Vol. 45.-P. 69.
- Buckler H.M., Healy D.L. and Burger H.G. Does gonadotropin suppression result in follicular development in premature ovarian failure? // Gynecol Endocrinol.-1993.-Vol. 7.-P. 123-128.
- Burne Т.Н., Campbell S., Collins W.P., WhiteheadM.I. Transvaginal color flow imaging: a possible new screening technique for ovarian cancer//Br Med J.-1989.-Vol. 299.-P. 1367-1370.
- Check J.H., Chase J.S. andSpenceM. Pregnancy in premature ovarian failure after therapy with oral contraceptives despite resistance to previous human menopausal gonadotropin therapy//Am J Obstet Gynecol.-1989.-Vol.160.-P. 114-115.
- Chianuzzi V., Gigorrarga S., Escobar M.E., et al. Inhibition of follicle-stimulating hormone receptor binding circulating immunoglobulen //J. Clin Endocrinolog Metab.-1982.-Vol. 54.-P. 1221-1228.
- Conway G.S. Premature ovarian failure//British Medical Bulletin-2000.-Vol. 56(3).-P. 643-649, Fenichel P., Sosset C., et al. Premature ovarian failure: An autoimmune disease //Hum. Reprod.-2000. - P. 143-149.
- Conway G.S. Characterization of idiopathic premature ovarian failure Fertil Steril.-1996.-Vol. Feb.65(2).-P. 337-341
- Dada Т., Salha O., Allgar V., Sharma V. Utero-ovarian blood flow characteristics of pituitary desensitization//Hum Reprod.-2001.- Vol. Aug.l6(8).-P.1663-1670.
- DeLingerere , DennersteinL., Backstom T. Influence of route of administration on progesterone metabolism//Maturitas.-1995.-Vol. 21.-P. 251-257 17. Falsetti L., Scalchi S et al. Premature Ovarian Failure //Gynecol Endocrinol-1999.-Vol. Jun 13(3).- P. 189-195.
- Fenichel P., Sosset C., et al. Premature ovarian failure: An autoimmune disease.//Hum. Reproad.- 2000 - P. 143-149.
- Jones G.S., de Morales-Ruehsen M. A new syndrome of amenorrhea in association with hypogonadotropism and apparently normal follicular apharatus//Am. J. Obstet Gynecol.-1969. - Vol.104.-P.597.
- Krauss CM, Turksoy RN, Atkins L, et al. Familial premature ovarian failure menopause due to an interstitial deletion of the long arm of the X-chromosome //N Engl J. Med .-1987.-Vol.317.-P.125-131.
- Losordo W, IsnerM. Estrogen and Angiogenesis Arterioscler Thromb Vase Biol.-2001.-Vol. 21.-P. 6-12 22. Luisetto G., Zangari M, Bottega F. Different rates of forearm bone loss in healthy women with early or late menopause//Osteoporosis International.- 1995. - Vol.5(l) - P. 54-62.
- Menashe Y., Pearlstone, A.C. and Surrey, E.S. Spontaneous pregnancies despite failed attempts at ovulation induction in a women with iatrogenic premature ovarian failure// J Reprod. Med.-Vol.41.-P. 207-210.
- Ming-Yang Chang et al. Use of the antral follicle count to predict the outcome of assisted reproduc tive technologies. Fertil. Steril.-1998.-Vol. 69.- P. 505-510.
- Pan H.A., Li C.H., WuM.H., Chang P.M. Qualification of ovarian stromal Doppler signals in postmenopausal women receiving hormone replace ment therapy Menopause.-2003.-Vol. Jul-Aug 10 (4).-P. 366-372.
- Pellizzari P., Esposito C., et al. Color Doppler analysis of ovarian and uterine arteries in women with hypoestrogenic amenorrhoea//Hum. Reprod.- 2002.-Vol. 17.-N12.-P. 3208-3212.
- Polansky S. and De Papp E. W. Pregnancy associated with hypergonadotropic hypogonadism // Obstet Gynecol.-1976.-Vol. 47.-P. 47-51.
- SheuB.C., HoH.N., Yang Y.S. Spontanouse pregnancy after pregnancy by oocyte donation due to premature ovarian failure//Hum Reprod.-1996.- Vol. ll.-P. 1359-1360.
- Syrop, C.H., Willhoite, A. Ovarian volume: a novel outcome predictor for assisted reproduction// Fertil. Steril- 1995.-Vol. 64.-P. 1167-1171.
- Valentin L. Use of color and Spectral Doppler ultra sound examination in genaecology // European Journal of Ultasound.-1997.-Vol. 6.-P. 143-163.
- von Lindern M., BoerL., Wessely O., Parker M., Beug H. The transaction domain AF-2 but not the DNA-binding domain of the estrogen receptor is required to inhibit differenceation of avian erythroid progenitors//Mol Endocrinol.-1998.-Vol. 12.-P. 263-277.
- Xiao X., Le G., Zhang Y., Li C. The study of ovarian artery hemodynamics in patients with infertility by color Doppler energy//J Tongji Med Univ.- 2001-Vol. 21(1).-P. 42-43.

УЗИ сканер RS80
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Публикации по теме
- Ультразвуковая диагностика несостоятельного рубца на матке в отдаленном послеоперационном периоде - Чечнева М.А.
- Эхографические особенности лютеиновой фазы менструального цикла - Кузьмина С.А.
- Эхография и допплерометрия для оценки эффективности лечения женщин с преждевременной недостаточностью яичников - Александрова Н.В.
- Ультразвуковая диагностика однорогой матки - Демидов В.Н.
- Необычная ультразвуковая визуализация зрелой тератомы яичника - Селиванов В.И.
