Ультразвуковая диагностика венозного тромбоза в амбулаторных условиях
Москва, Россия.
Рубрика: Функциональная диагностика

УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Введение
Острый венозный тромбоз - распространенное и опасное заболевание. Согласно статистическим данным, его частота в общей популяции составляет около 160 на 100 000 населения [1]. Тромбоз в системе нижней полой вены (НПВ) представляет собой наиболее частую и опасную разновидность этого патологического процесса и является основным источником эмболии легочных сосудов (84,5%). Система верхней полой вены дает 0,4-0,7% тромбоэмболий легочной артерии (ТЭЛА), правые отделы сердца - 10,4%. На долю тромбозов вен нижних конечностей приходится до 95% случаев всех тромбозов в системе НПВ. Диагноз острого венозного тромбоза прижизненно диагностируется у 19,2% больных [2]. В долгосрочной перспективе тромбоз глубоких вен (ТГВ) ведет к формированию посттромбофлебитической болезни, проявляющейся хронической венозной недостаточностью вплоть до развития трофических язв, что существенно снижает трудоспособность и качество жизни пациентов.
Основными механизмами внутрисосудистого образования тромбов, известными со времен R.Virchow, являются замедление тока крови (стаз), гиперкоагуляция, травма стенки сосуда (повреждение эндотелия). Острый венозный тромбоз достаточно часто развивается на фоне различных онкологических заболеваний (злокачественные опухоли желудочнокишечного тракта, женской половой сферы и др.) в силу того, что раковая интоксикация вызывает развитие гиперкоагуляционных изменений и угнетение фибринолиза, а также из-за механического сдавления вен опухолью и прорастания ее в сосудистую стенку. Предрасполагающими факторами ТГВ считаются также ожирение, беременность, прием оральных гормональных контрацептивов, наследственные тромбофилии (дефицит антитромбина III, протеина C и S, лейденовская мутация и др.), системные заболевания соединительной ткани, хронические гнойные инфекции, аллергические реакции [3, 4]. Наибольшему риску развития ТГВ подвержены больные пожилого и старческого возраста и лица, страдающие хронической венозной недостаточностью нижних конечностей, а также пациенты с инфарктом миокарда, декомпенсированной сердечной недостаточностью, инсультом, пролежнями, гангреной нижних конечностей. Особую тревогу вызывают травматологические больные, так как переломы бедренной кости в основном встречаются у лиц пожилого и старческого возраста, наиболее отягощенных соматическими заболеваниями [5]. Тромбозы у травматологических больных могут возникнуть при любой травме нижних конечностей, так как при этом имеют место все этиологические факторы тромбоза (повреждение сосуда, венозный застой и изменения свертывающих свойств крови) [6].
Надежная диагностика флеботромбоза является одной из актуальных клинических задач. Физикальные методы обследования позволяют поставить правильный диагноз лишь в типичных случаях заболевания, при этом частота диагностических ошибок достигает 50% [7]. Так, например, тромбоз вен икроножных мышц при сохраненной проходимости остальных вен нередко протекает бессимптомно. Из-за опасности пропустить острый ТГВ голеней клиницисты зачастую ставят этот диагноз в каждом случае появления болей в икроножных мышцах [8]. Особое внимание заслуживают "травматологические" больные, у которых наличие боли, отека и изменения окраски конечности могут быть следствием самой травмы, а не ТГВ. Иногда первым и единственным проявлением подобного тромбоза служит массивная ТЭЛА.
В задачи инструментального обследования входят не только подтверждение или опровержение наличия тромба, но также определение его протяженности и степени эмбологенности. Выделение эмболоопасных тромбов в отдельную группу и изучение их морфологической структуры имеют большое практическое значение, так как без этого невозможны разработка эффективной профилактики легочной эмболии и выбор оптимальной тактики лечения. Тромбоэмболические осложнения чаще наблюдаются при наличии флотирующего тромба с гетерогенной структурой, неровным гипо- или изоэхогенным контуром в отличие от тромбов, имеющих гиперэхогенный контур и гомогенную структуру. Важным критерием эмбологенности тромба является степень его подвижности в просвете сосуда. Эмболические осложнения чаще отмечаются при выраженной и умеренной подвижности тромбомасс [9, 10].
Венозный тромбоз - достаточно динамичный процесс. С течением времени процессы ретракции, гуморального и клеточного лизиса способствуют уменьшению размеров тромба. Одновременно с этим идут процессы его организации и реканализации. В большинстве случаев проходимость сосудов постепенно восстанавливается, клапанный аппарат вен разрушается, а остатки тромбов в виде пристеночных наложений деформируют сосудистую стенку. Затруднения в диагностике могут быть при возникновении повторного острого тромбоза на фоне частично реканализованных вен у больных с посттромбофлебитической болезнью. В этом случае достаточно надежным критерием является различие вен в диаметре: у пациентов с признаками реканализации тромбомасс происходит уменьшение вены в диаметре вследствие стихания острого процесса; при развитии ретромбоза вновь происходит достоверное увеличение диаметра вены с нечеткими ("размытыми") контурами стенок и окружающих тканей [9]. Этими же критериями пользуются при дифференциальной диагностике острого пристеночного тромбоза с посттромботическими изменениями вен.
Из всех неинвазивных методов, применяемых для диагностики тромбоза, в последнее время все чаще используется ультразвуковое сканирование венозной системы. Метод триплексного ангиосканирования, предложенный Barber в 1974 г., включает исследование сосудов в В-режиме, анализ допплеровского сдвига частот в виде классического спектрального анализа и цветового картирования потока (в скоростном и энергетическом режимах). Использование спектральной допплерографии позволило точно измерять кровоток внутри просвета вен. Применение метода цветового допплеровского картирования (ЦДК) обеспечило возможность быстро отличать окклюзирующий тромбоз от неокклюзирующего, выявлять начальные стадии реканализации тромбов, а также определять местоположение и размер венозных коллатералей. При исследованиях в динамике ультразвуковой метод позволяет обеспечить достаточно точный контроль за эффективностью тромболитической терапии. Кроме того, с помощью ультразвукового исследования можно установить причины появления клинической симптоматики, сходной с таковой при патологии вен, например выявить кисту Бейкера, межмышечную гематому или опухоль. Внедрение в практику ультразвуковых приборов экспертного класса с датчиками частотой от 2,5 до 14 МГц позволило достичь практически 99% точности диагностики.
Материал и методы
Обследование включало осмотр пациентов с клиническими признаками венозного тромбоза и ТЭЛА. Больные предъявляли жалобы на отек и боль в нижней (верхней) конечности, боль в икроножной мышце (чаще распирающего характера), "тянущую" боль в подколенной области, боль и уплотнение по ходу подкожных вен. При осмотре выявлялись умеренный цианоз голени и стопы, плотный отек, болезненность при пальпации мышц голени, у большинства пациентов - положительные симптомы Хоманса и Мозеса.
Всем обследуемым проводилось триплексное сканирование венозной системы на современных ультразвуковых аппаратах линейным датчиком с частотой 7 МГц. При этом оценивалось состояние вен бедра, подколенной вены, вен голени, а также большой и малой подкожных вен. Для визуализации подвздошных вен и НПВ использовался конвексный датчик с частотой 3,5 МГц. При сканировании НПВ, подвздошных, большой подкожной вены, бедренных вен и вен голени в дистальном отделе нижних конечностей пациент находился в положении лежа на спине. Исследование подколенных вен, вен верхней трети голени и малой подкожной вены проводилось в положении пациента лежа на животе с валиком, подложенным под область голеностопных суставов. Затруднения в диагностике возникали при визуализации дистального отдела поверхностной бедренной вены у тучных пациентов, визуализации вен голени при выраженных трофических и индуральных изменениях тканей. В этих случаях также использовался конвексный датчик. Глубину сканирования, усиление эхо-сигнала и другие параметры исследования подбирали индивидуально для каждого пациента и сохраняли неизменными во время всего обследования, включая наблюдения в динамике.
Сканирование начинали в поперечном сечении для исключения наличия флотирующей верхушки тромба, о чем свидетельствовало полное соприкосновение венозных стенок во время легкой компрессии датчиком. Убедившись в отсутствии свободно флотирующей верхушки тромба, компрессионную пробу датчиком проводили от сегмента к сегменту, от проксимальных отделов к дистальным. Предлагаемая методика является наиболее точной не только для выявления тромбоза, но и для определения его протяженности (исключая подвздошные вены и НПВ, где проходимость вен определялась в режиме ЦДК). Продольное сканирование вен подтверждало наличие и характеристики венозного тромбоза. Кроме того, продольное сечение использовалось для локации анатомического слияния вен. Во время обследования оценивались состояние стенок, просвет вен, локализация тромба, его протяженность, степень фиксации к сосудистой стенке.
Ультразвуковая характеристика венозных тромбов проводилась по отношению к просвету сосуда: они различались как пристеночные, окклюзирующие и флотирующие тромбы. Признаками пристеночного тромбоза считались визуализация тромба с наличием свободного кровотока в просвете вены, отсутствие полного спадения стенок при компрессии вены датчиком, наличие дефекта заполнения при ЦДК, наличие спонтанного кровотока при спектральной допплерографии (рис.1).
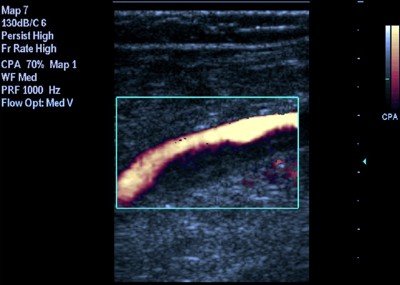
Рис. 1. Неокклюзирующий тромбоз подколенной вены. Продольное сканирование вены. Огибающий кровоток в режиме энергетического кодирования потока.
Ультразвуковыми критериями флотирующих тромбов считали: визуализацию тромба как эхогенной структуры, расположенной в просвете вены с наличием свободного пространства, колебательные движения верхушки тромба, отсутствие соприкосновения стенок вены при компрессии датчиком, наличие свободного пространства при выполнении дыхательных проб, огибающий тип кровотока при ЦДК, наличие спонтанного кровотока при спектральной допплерографии. При выявлении флотирующего тромба оценивалась степень его подвижности: выраженная - при наличии спонтанных движений тромба при спокойном дыхании и/или задержке дыхания; умеренная - при обнаружении колебательных движений тромба в ходе проведения функциональных проб (кашлевая проба); незначительная - при минимальной подвижности тромба в ответ на функциональные пробы.
Результаты исследования
С 2003 по 2006 г. были обследованы 236 пациентов в возрасте от 20 до 78 лет, из них 214 с клиникой острого тромбоза и 22 с клиникой ТЭЛА.
В первой группе в 82 (38,3%) случаях проходимость глубоких и поверхностных вен не была нарушена и клиническая симптоматика обусловлена иными причинами (табл. 1).
| Патология | Количество больных | |
|---|---|---|
| абс. | % | |
| Травма | 33 | 40,2 |
| Заболевания суставов | 18 | 22,0 |
| Лимфовенозная недостаточность | 12 | 14,6 |
| Киста Бейкера больших размеров | 6 | 7,3 |
| Лимфаденит | 5 | 6,1 |
| Внутримышечная гематома | 4 | 4,9 |
| Экстравазальная компрессия | 4 | 4,9 |
Диагноз тромбоза был подтвержден у 132 (61,7%) больных, при этом в большинстве случаев (94%) тромбоз выявлялся в системе НПВ. ТГВ был обнаружен в 47% случаев, поверхностных вен - в 39%, поражение как глубокой, так и поверхностной венозной системы наблюдалось в 14%, в том числе у 5 больных с вовлечением перфорантных вен.
Вероятные причины (факторы риска) развития венозного тромбоза представлены в табл. 2.
| Фактор риска | Количество больных | |
|---|---|---|
| абс. | % | |
| Травма (в том числе длительная гипсовая иммобилизация) | 41 | 31,0 |
| Варикозная болезнь | 26 | 19,7 |
| Злокачественные новообразования | 23 | 17,4 |
| Операции | 16 | 12,1 |
| Прием гормональных препаратов | 9 | 6,8 |
| Тромбофилии | 6 | 4,5 |
| Хроническая ишемия конечностей | 6 | 4,5 |
| Ятрогенные причины | 5 | 4,0 |
В наших наблюдениях наиболее часто выявлялись распространенная форма тромбоза, а также поражение вен на уровне подколенно-берцового и бедренно-подколенного сегментов (табл. 3).
| Локализация | Количество больных | |
|---|---|---|
| абс. | % | |
| Вены голени | 19 | 14,4 |
| Подколенная вена | 8 | 6,0 |
| Подколенно-берцовый сегмент | 34 | 25,8 |
| Бедренно-подколенный сегмент | 21 | 15,9 |
| Илеофеморальный сегмент | 5 | 3,8 |
| Бедренно-подколенно-берцовый сегмент | 38 | 38,8 |
| Подвздошно-бедренно-подколенно-берцовый сегмент | 7 | 5,3 |
Чаще (63%) имели место тромбозы, полностью окклюзирующие просвет сосуда, на втором месте по частоте (30,2%) были пристеночные тромбы. Флотирующие тромбы диагностированы в 6,8% случаев: у 1 пациента - в сафенофеморальном соустье при восходящем тромбозе ствола большой подкожной вены, у 1 - илеофеморальный тромбоз с флотирующей верхушкой в общей подвздошной вене, у 5 - в общей бедренной вене при тромбозе бедренно-подколенного сегмента и у 2 - в подколенной вене при ТГВ голени.
Протяженность нефиксированной (флотирующей) части тромба, по ультразвуковым данным, варьировала от 2 до 8 см. Чаще выявлялась умеренная подвижность тромботических масс (5 больных), в 3 случаях подвижность тромба была минимальной. У 1 пациента при спокойном дыхании визуализировались спонтанные движения тромба в просвете сосуда (высокая степень подвижности). В наших наблюдениях чаще выявлялись флотирующие тромбы с неоднородной эхоструктурой (7 человек), при этом в дистальном отделе преобладал гиперэхогенный компонент, а в области головки тромба - гипоэхогенный (рис. 2).
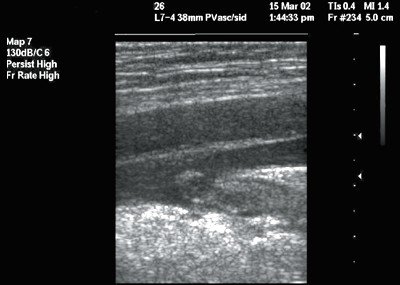
Рис. 2. Флотирующий тромб в общей бедренной вене. В-режим, продольное сканирование вены. Тромб гетероэхогенной структуры с четким гиперэхогенным контуром.
В первом случае зафиксирован изоэхогенный тромб с гиперэхогенным контуром (рис. 3), во втором - гомогенный "организованный" тромб с четким контуром (рис. 4).
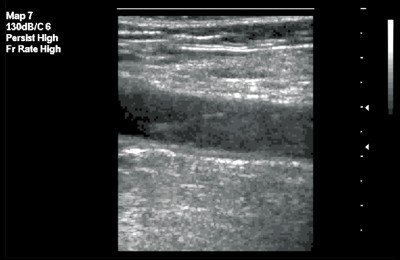
Рис. 3. Флотирующий тромб в поверхностной бедренной вене. В-режим, продольное сканирование вены. Тромб изоэхогенной структуры с гиперэхогенным контуром.
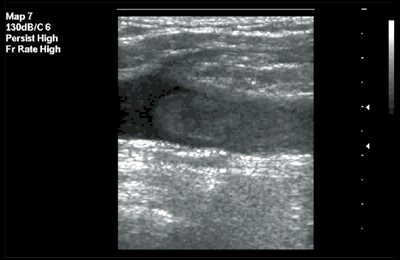
Рис. 4. Флотирующий тромб в поверхностной бедренной вене. В-режим, продольное сканирование вены. Тромб гомогенной эхоструктуры с четким контуром.
В группе пациентов с клиникой ТЭЛА у 5 (22,7%) больных имел место ТГВ различных стадий развития (преимущественно бедренно-подколенный сегмент).
В динамике для оценки течения тромботического процесса были обследованы 82 пациента, из них у 63 (76,8%) отмечалась частичная реканализация тромботических масс. В этой группе у 28 (44,4%) больных наблюдался центральный тип реканализации (при продольном и поперечном сканировании в режиме ЦДК реканализационный канал визуализировался в центре сосуда); у 23 (35%) пациентов диагностирована пристеночная реканализация тромботических масс (чаще кровоток определялся вдоль стенки вены, непосредственно прилежащей к одноименной артерии); у 13 (20,6%) больных выявлялась неполная реканализация с фрагментарным асимметричным окрашиванием в режиме ЦДК. Тромботическая окклюзия просвета вены наблюдалась у 5 (6,1%) больных, в 6 (7,3%) случаях отмечалось восстановление просвета вены. Признаки ретромбоза сохранялись у 8 (9,8%) обследованных.
Выводы
Комплексное ультразвуковое исследование, включающее ангиосканирование с использованием спектрального, цветового и энергетического допплеровских режимов и эхографию мягких тканей, является высокоинформативным и безопасным методом, позволяющим наиболее достоверно и быстро решать вопросы дифференциальной диагностики и лечебной тактики в амбулаторной флебологической практике. Это исследование целесообразно проводить на амбулаторном этапе для более раннего выявления пациентов, которым не показана (а иногда и противопоказана) тромболитическая терапия, и направления их в профильные отделения; при подтверждении наличия венозного тромбоза необходимо выявлять лиц с высоким риском развития тромбоэмболических осложнений; наблюдать в динамике за течением тромботического процесса и тем самым корректировать лечебную тактику.
Литература
- Lindblad, Sternby N.H., Bergqvist D. Incidence of venous thromboembolism verified by necropsy over 30 years. // Br.Med.J. 1991. V. 302. P. 709-711.
- Савельев В.С. Тромбоэмболия легочной артерии - классификация, прогноз и хирургическая тактика. // Грудная и сердечно-сосудистая хирургия 1985. N°5. С. 10-12.
- Баркаган З.С. Геморрагические заболевания и синдромы. Изд. 2-е, перераб. и доп. М.:Медицина 1988; 525 с.
- Bergqvist D. Postoperative thromboembolism. // New York 1983. P. 234.
- Савельев В.С. Флебология. М.: Медицина 2001; 664 с.
- Кохан Е.П., Заварина И.К. Избранные лекции по ангиологии. М.: Наука 2000. С. 210, 218.
- Hull R., Hirsh J., Sackett D.L. et al. Combined use of leg scenning and impedance plethysmography in suspected venous thrombosis. An alternative to venography. // N.Engl.J.Med. 1977. N° 296. P. 1497-1500.
- Савельев В.С., Думпе Э.П., Яблоков Е.Г. Болезни магистральных вен. М., 1972. С. 144-150.
- Альбицкий А.В., Богачев В.Ю., Леонтьев С.Г. и др. Ультразвуковое дуплексное ангиосканирование в диагностике ретромбозов глубоких вен нижних конечностей. // Кремлевская медицина 2006. N°1. С. 60-67.
- Харченко В.П., Зубарев А.Р., Котляров П.М. Ультразвуковая флебология. М.: ЗОА "Эники". 176 с.

УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Публикации по теме
- Возможности ультразвукового исследования с цветовым допплеровским картированием в диагностике тромбоза в системе воротной вены - Курзанцева О.М.
- Абсцессы легкого - многообразие ультразвуковой семиотики - Сафонов Д.В.
- Ультразвуковая диагностика венозного тромбоза в амбулаторных условиях - Раптанова Т.А.
- Возможности динамической ультразвуковой допплерографии в определении функциональной полноценности сосудистого анастомоза после реконструктивных хирургических вмешательств - Берестень Н.Ф.
- Кардиосовместимая доплерография кавального кровообращения печени - Берестень Н.Ф.

