Возможности ультразвукового метода исследования в диагностике и лечении ложных аневризм висцеральных сосудов
кафедра лучевой диагностики ФППОв I МГМУ им. И.М. Сеченова, Москва.
Рубрика: Функциональная диагностика

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Хронический панкреатит в 21-25% случаев сопровождается развитием постнекротических кист [1]. В отличие от острых кист поджелудочной железы, кисты при хроническом панкреатите никогда не подвергаются рассасыванию и самоизлечению. Существование больших (более 5 см) кист при хроническом панкреатите свыше 7 нед, как правило, сопровождается развитием различных осложнений [2, 3]:
- нагноение в 1-4%;
- кровотечение в полость кисты;
- сдавление органов желудочно-кишечного тракта, воротной, нижней полой вен, мочевыводящих и желчных путей;
- прорыв кисты в желудочно-кишечный тракт, брюшную, грудную полость, в мочевыводящие пути и воротную вену;
- перфорация в общий желчный проток.
Псевдокисты содержат панкреатические энзимы, которые вызывают периартериальное воспаление, некроз стенки сосуда, расположенного рядом со стенкой кисты, и разрушают ее. Когда артерия "прорывается" в кисту, она формирует ложную аневризму или кровотечение в псевдокисту [4, 5]. Ложная аневризма - не частое осложнение, оно наблюдается у 2-10% таких больных [6]. Как правило, в литературе описаны единичные наблюдения подобных осложнений. В табл. 1 представлена частота ложной аневризмы висцеральных артерий (АВА) по данным литературы [5, 7-13].
| N | Авторы | Клиника | Количество наблюдений ложной аневризмы | Год |
|---|---|---|---|---|
| 1 | H. Boschman и соавт. [7] | Potsdam Germany, Ernst-von-Bergmann-Klinikum | 1 селезеночная артерия | 2001 |
| 2 | A. Urakami и соавт. [8] | Okayama, Japan, Kawasaki Medical School | 1 селезеночная артерия | 2002 |
| 3 | K. Ido и соавт. [5] | Aichi, Japan, Nagoya Tokushukai General Hospital | 1 поджелудочно- двенадцатиперстная артерия | 2004 |
| 4 | L. Kaman и соавт. [9] | Chandigarh, India, Postgraduate Institute of Medical Education and Reseаrch | 1 верхняя панкреатодуоденальная артерия | 2004 |
| 5 | J.M. Alamo и соавт. [10] | Seville. Spain, Hospital del Rocio | 1 печеночная артерия | 2005 |
| 6 | D. Lagana и соавт. [11] | Rochestr, Great Britain, University of Rochester Medical Center | 1 селезеночная артерия; 2 желудочнодвенадцатиперстные артерии; 1 панкреатодуоденальная артерия | 2006 |
| 7 | П.Г. Таразов и соавт. [12] | Санкт-Петербург, Россия, Российский научный центр радиологии и хирургических технологий Росмедтехнологий | 1 селезеночная артерия | 2009 |
| 8 | М.В. Вишнякова и соавт. [13] | Москва, Россия, отделение лучевой диагностики, Московского областного научноисследовательского клинического института им. М.Ф. Владимирского | 1 селезеночная артерия | 2010 |
Из табл. 1 следует, что ложная аневризма висцеральных артерий - весьма редкая патология. Необходимо отметить, что развитие кровотечения в постнекротическую кисту является грозным осложнением и до недавнего времени сопровождалось летальностью от 40 до 80% [2].
Клинические проявления неосложненной ложной аневризмы висцеральных артерий неспецифичны. Пациенты отмечают абдоминальный дискомфорт, боли в животе различной локализации, интенсивности и характера, не зависящие от приема пищи. При пальпации живота в большинстве случаев определяется болезненность в эпигастрии, очень редко - пульсирующее образование. При аускультации в проекции аневризмы выслушивается систолический шум. Также могут иметь место симптомы, обусловленные компрессией соседних структур [6, 14, 15].
Ложные аневризмы характеризуются, как правило, преобладанием симптомов панкреатита и его осложнений. Редко, при наличии постнекротической кисты больших размеров, пациенты могут ощущать наличие объемного образования в брюшной полости.
В настоящее время для диагностики ложной аневризмы висцеральных артерий применяют ультразвуковое, компьютерно-томографическое и магнитно-резонансное исследование, а также ангиографию. Каждое из этих исследований позволяет выявить аневризму, определить ее локализацию, питающую артерию и взаимоотношение с окружающими органами и сосудистыми структурами [2, 16]. Однако при ультразвуковом исследовании (УЗИ) отсутствует лучевая нагрузка, вследствие чего его можно применять и как метод диагностики, и как метод, позволяющий мониторировать состояние пациента во время и после хирургического (мини-инвазивного и/или открытого) лечения больных.
Лечение как симптомных, так и асимптомных ложных аневризм висцеральных артерий обязательно. Оно, как правило, включает хирургическое вмешательство, направленное также на коррекцию проявлений хронического панкреатита. С развитием интервенционной радиологии началось активное внедрение в практику эндоваскулярных методов лечения аневризм висцеральных артерий. Ряд авторов при угрозе или развитии аррозионного кровотечения операцией выбора считают перевязку артерии с последующей декомпрессией кисты, а рентгеноэндоваскулярную окклюзию рассматривают как вариант подготовки больного к радикальному оперативному лечению. Но с развитием и совершенствованием эндоваскулярных лечебных методик все чаще стали появляться описания успешного транскатетерного рентгеноэндоваскулярного лечения аррозионных кровотечений в псевдокисту поджелудочной железы [4].
Целью настоящей работы явилась оценка возможности ультразвукового метода исследования в диагностике и лечении ложных аневризм (ЛА) висцеральных сосудов.
Материалы и методы
За период с 1995 по 2011 г. в Институте хирургии проходили обследование и лечение 25 пациентов с ложными аневризмами висцеральных сосудов в возрасте от 34 до 74 лет (средий возраст 50,1±3,28 года). В исследование вошли 17 (68,0%) мужчин и 8 (32,0%) женщин. В дооперационном периоде всем пациентам выполняли УЗИ в объеме: исследование в В-режиме, дуплексное сканирование в режимах цветового допплеровского картирования (ЦДК), отражения допплеровского сигнала (ЭОДС) и импульсной допплерографии, при необходимости проводили трехмерную реконструкцию ультразвукового изображения. Ангиографическое исследование выполнили в 68,0% случаев.
Оценку образований проводили по следующим критериям:
- локализация аневризмы;
- определение сосуда, являющегося источником аневризмы, с оценкой диаметра;
- форма аневризмы;
- размер;
- состояние просвета сосуда и характер кровотока;
- состояние полости и ее взаимоотношения с окружающими структурами.
По результатам ангиографии и интраоперационным данным во всех случаях верифицировали ложные аневризмы.
Результаты
На основании данных УЗИ у 25 пациентов был диагностирован хронический панкреатит с постнекротической кистой и сформировавшейся в ее полости ЛА прилежащего магистрального висцерального сосуда. Локализация постнекротических кист, в полости которых развилась ЛА, была представлена следующим образом: головка поджелудочной железы - у 9 (36,0%) больных, тело - у 3 (12,0%), тело-хвост - у 5 (20,0%) и хвост - у 8 (32,0%). В 5 случаях в паренхиме поджелудочной железы локализовались и другие постнекротические кисты.
При анализе данных об особенностях течения хронического панкреатита было выявлено: наличие конкрементов в паренхиме железы - у 17 (68,0%) больных, панкреатическая гипертензия - у 17 (68,0%) (в том числе с наличием вирсунголитиаза у 4), увеличение селезенки - у 18 (72,0%) пациентов. У 7 (28,0%) пациентов диагностировали увеличение регионарных лимфатических узлов. Оценка состояния вен системы воротной вены показала, что портальная гипертензия с развитием венозных коллатералей (от 2 до 11 мм) имела место у 15 (60,0%) больных, тромбоз вен - у 7 (28,0%), экстравазальная компрессия - у 8 (32,0%).
Распределение аневризм по сосудамисточникам аневризмы - в проведенном исследовании представлено в табл. 2. У3 (12,0%) пациентов были выявлены два источника ложных аневризм.
| Сосуд-источник аневризмы | Число* | % |
|---|---|---|
| Селезеночная артерия | 15 | 53,5 |
| Общая печеночная | 2 | 7,1 |
| Верхняя брыжеечная артерия | 1 | 3,6 |
| Желудочно-двенадцатиперстная | 5 | 17,9 |
| Поджелудочно-двенадцатиперстная | 2 | 7,1 |
| Левая желудочная | 1 | 3,6 |
| Желудочно-сальниковая | 1 | 3,6 |
| Тощекишечная | 1 | 3,6 |
Диагностированные ложных аневризм во всех наблюдениях имели одну и ту же этиологию и, следовательно, одинаковую клиническую картину. Аналогичными были и их диагностические признаки.
Диаметр постнекротической кисты составил от 73,0 до 143,0 мм. Размер полости ЛА варьировал от 20,0х16,0 до 44,6х52,0 мм. Во всех случаях в полости постнекротической кисты определяли циркулярно расположенные тромботические массы толщиной от 4,0 до 27,7 мм. Размер дефекта сосуда составлял от 4,9 до 7,1 мм.
При комплексном УЗИ в В-режиме визуализировали округлое образование в капсуле различной степени выраженности, неоднородное по структуре, по периферии преимущественно эхоплотное с наличием анэхогенной полости, интимно прилежащей к одной из стенок с нарушением ее целостности. При дуплексном сканировании отмечено спонтанное контрастирование полости аневризмы (аналогично и в режиме Sie-flow) с регистрацией артериального кровотока. В режиме импульсной допплерографии линейная скорость кровотока на входе в аневризму была повышена на 18,9-37,8% по сравнению с нормальными значениями с высокой диастолической составляющей. В 18 случаях полость аневризмы окрашивалась не полностью, имелись пристеночные неокрашиваемые участки, которые соответствовали "свежим" тромботическим массам (рис. 1).
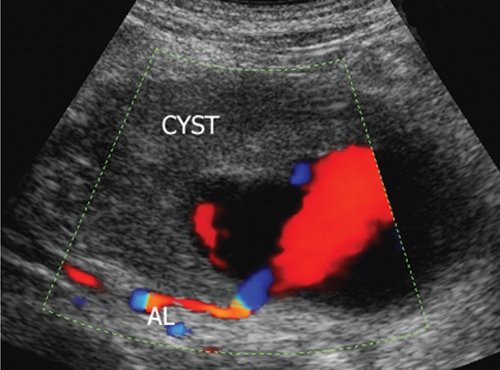
Режим ЦДК: AL - селезеночная артерия, CYST - постнекротическая киста.
Трехмерная реконструкция УЗ-изображения помогает диагностировать саму ЛА и определить ее взаимоотношение с сосудом-источником, а также более четко проследить ход сосуда.
Анализ данных обследования пациентов показал, что при выборе тактики ведения этой категории больных необходимо учитывать следующие параметры:
- размеры аневризмы;
- связь полости аневризмы с протоковой системой поджелудочной железы;
- наличие осложнений течения хронического панкреатита (панкреатическая гипертензия, кальциноз паренхимы поджелудочной железы, портальная гипертензия).
Так, в нашем исследовании в 7 (28,0%) случаях ЛА были размером менее 50,0 мм в диаметре, пять из них имели достаточно выраженные пристеночные тромботические массы. Связь полости этих аневризм с главным панкреатическим протоком (ГПП) отсутствовала. В 7 (28,0%) случаях установлена связь ЛА с протоковой системой поджелудочной железы, во всех этих наблюдениях размеры аневризмы превышали 60,0 мм в диаметре. Следует отметить, что связь ЛА с протоковой системой поджелудочной железы по данным УЗИ выявили только в 3 случаях. Методом выбора для диагностики этого состояния является магнитно-резонансная холангиопанкреатография, позволяющая четко проследить характер взаимоотношения ЛА с ГПП. Осложненное течение хронического панкреатита с большей степенью выраженности выявляли при значительных размерах аневризмы и наличии ее связи с ГПП.
Полученные в ходе исследования данные свидетельствуют о том, что при небольших ложных аневризмах, не связанных с протоковой системой поджелудочной железы, эффективно рентгеноэндоваскулярное лечение, позволяющее добиться "выключения" ЛА из кровотока.
При ложных аневризмах, полость которых связана с протоковой системой поджелудочной железы, а также при наличии панкреатической гипертензии, калькулеза паренхимы поджелудочной железы и вирсунголитиаза, портальной гипертензии целесообразно проводить хирургическое лечение, направленное на устранение ЛА и других осложнений хронического панкреатита. Для уменьшения риска профузного кровотечения при последующем открытом оперативном вмешательстве рентгеноэндоваскулярное лечение эффективно в качестве I этапа лечения.
Таким образом, данные УЗИ непосредственно влияют на выбор тактики лечения пациентов с ложными аневризмами висцеральных сосудов.
В 17 (68,0%) наблюдениях проводили полипроекционную ангиографию брюшного отдела аорты и ее ветвей для уточнения локализации ЛА, ее взаимоотношений с соседними структурами и оценки возможности использования методов эндоваскулярного лечения. При ангиографии определяли дефект артерии с заполнением полости ЛА.
По результатам предоперационного обследования, с учетом клинических данных о состоянии паренхимы поджелудочной железы и состоянии органов желудочно-кишечного тракта, была выбрана следующая тактика лечения пациентов:
- эндоваскулярная окклюзия полости аневризмы - в 8 (32,0%) наблюдениях;
- в качестве I этапа лечения выполнено эндоваскулярное вмешательство (окклюзия полости артерии, ствола артерии на проксимальном участке, эндопротезирование), II этап - открытое оперативное вмешательство - в 5 (20,0%) наблюдениях (рис. 2-5);
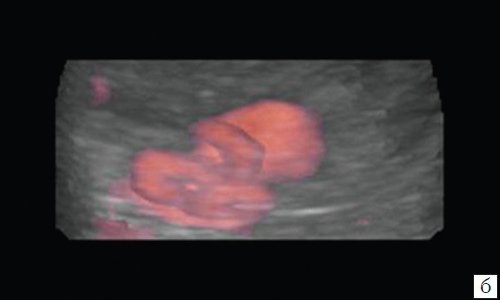
- изогнутость ствола артерии не позволила выполнить эндоваскулярное вмешательство, вследствие чего была произведена открытая операция - в 1 (4,0%) случае (рис. 6);
- ангиографическое исследование носило диагностический характер, так как при проведении консервативной терапии по данным УЗ-мониторирования в динамике было отмечено постепенное "закрытие" полости аневризмы, подтвердившееся и при ангиографии - в 3 (12,0%) случаях;
- при выраженном болевом синдроме и/или угрозе разрыва кисты выполнили экстренное открытое оперативное вмешательство - в 8 (32,0%) наблюдениях.
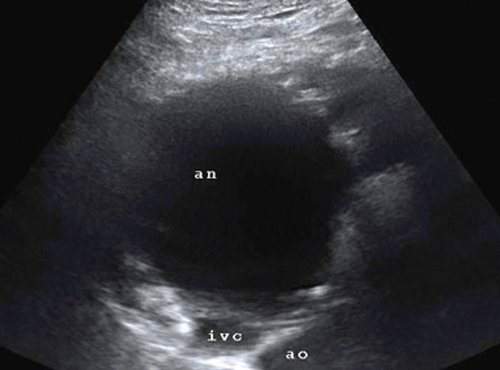
В-режим: an - аневризма, ivc - нижняя полая вена, ao - аорта.
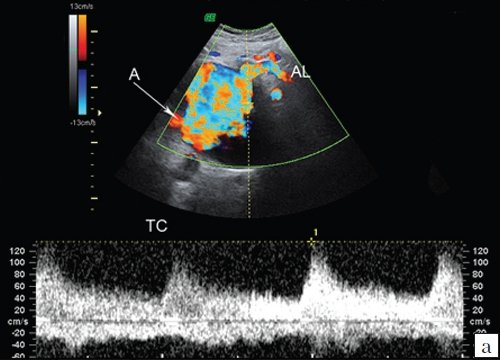
а) Эхограмма полости ложной аневризмы, окрашиваемой в режиме ЦДК, с регистрацией спектра допплеровских частот по чревному стволу, прослеживаемому по медиальному контуру аневризмы (A - аневризма, TC - чревный ствол, AL - селезеночная артерия).
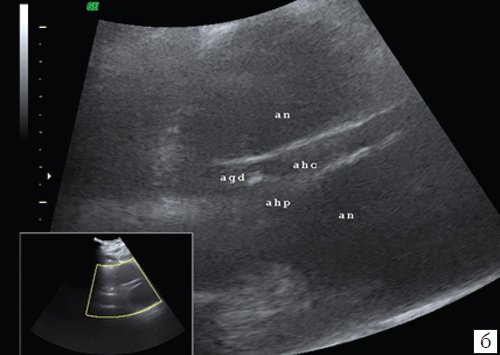
б) Эхограмма общей печеночной артерии и ее ветвей, распластанной на аневризме (an - аневризма, ahc - общая печеночная артерия, agd - желудочно-двенадцатиперстная артерия, ahp - собственная печеночная артерия) .
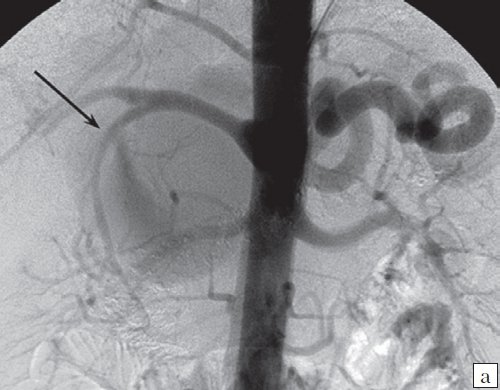
а) Ангиография брюшного отдела аорты, аневризма желудочно-двенадцатиперстной артерии отмечена черной стрелкой.
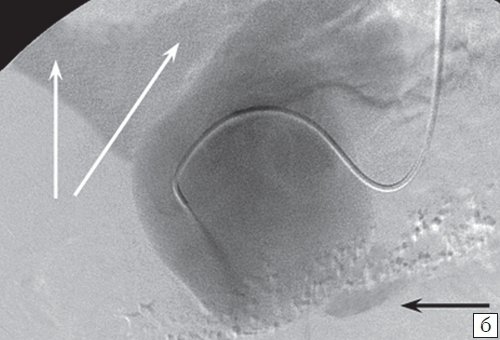
б) Ангиография после катетеризации аневризмы желудочнодвенадцатиперстной артерии. При введении контрастного вещества, сразу после заполнения полости аневризмы, контрастируются: верхняя брыжеечная вена (отмечена черной стрелкой) и ветви воротной вены (отмечены белыми стрелками).
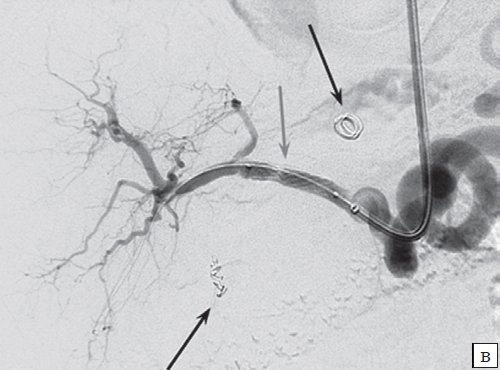
в) Целиакография после имплантации в общую и собственную печеночные артерии стент-графтов (отмечены серой стрелкой), визуализируются спирали в дистальной части желудочно-двенадцатиперстной артерии и спираль большего диаметра в полости аневризмы (отмечены черными стрелками).
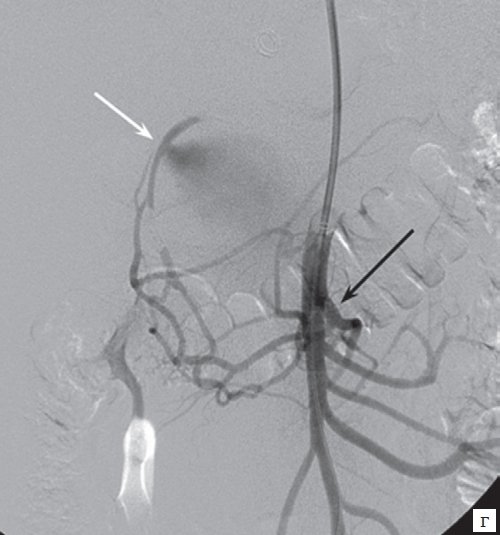
г) Верхняя мезентерикография, визуализируются множественные коллатерали между бассейнами желудочно-двенадцатиперстной и поджелудочно-двенадцатиперстной (отмечена черной стрелкой) артерий со сбросом контрастного вещества в полость аневризмы (отмечена белой стрелкой).
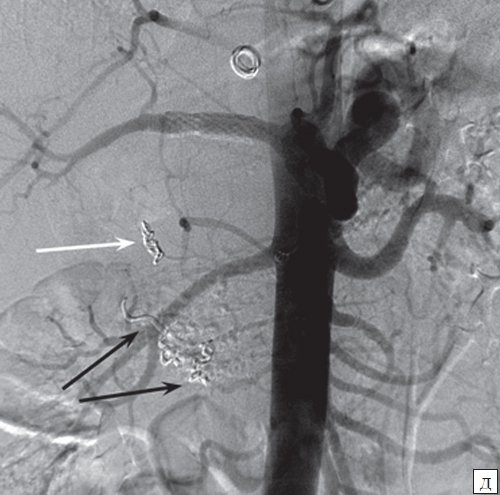
д) Ангиография брюшного отдела аорты, полость ЛА не контрастируется, общая и собственная печеночные артерии проходимы, визуализируются эмболизационные спирали в желудочно-двенадцатиперстной артерии (отмечены белой стрелкой) и в ветвях поджелудочно-двенадцатиперстной артерии (отмечены черными стрелками).
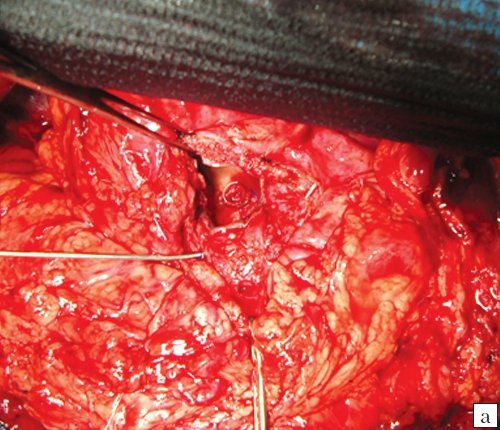
а) Изображение полости ЛА с наличием спирали в её полости.
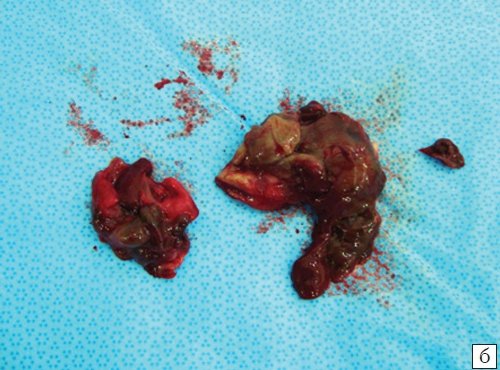
б) Макропрепарат.
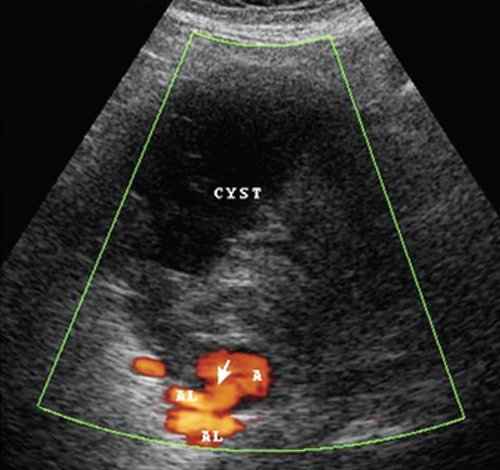
а) В режиме энергии отраженного допплеровского сигнала (AL - селезеночная артерия, CYST - постнекротическая киста).
б) В режиме трехмерной ультразвуковой ангиографии.
Следует отметить, что в 3 (12,0%) наблюдениях рентгеноэндоваскулярное вмешательство как окончательный метод лечения проводили под контролем УЗИ. Интраоперационный УЗ-мониторинг включал исследование полости аневризмы непосредственно перед вмешательством и сразу после него для оценки его эффективности. При этом в 2 случаях после окклюзии артерии и эмболизации полости ЛА сразу после манипуляции полость аневризмы не окрашивалась в режимах ЦДК и ЭОДС. У одного пациента с наличием ЛА желудочно-двенадцатиперстной артерии после окклюзии артерии в режимах ЦДК и ЭОДС полость аневризмы незначительно окрашивалась в проекции контралатерального полюса, в связи с чем было проведено дополнительное исследование, выявившее еще одни источник аррозионного кровотечения, который был устранен. В качестве иллюстрации приводим клиническое наблюдение.
Клиническое наблюдение
При комплексном УЗИ, включавшем исследование в В-режиме и дуплексное сканирование висцеральных сосудов и образования, в проекции головки железы определялось образование округлой формы размером 37,6х40,8х54,9 мм, с нечеткими, ровными контурами, по структуре неоднородное, с наличием эхоплотной неравномерно выраженной периферии, преимущественно по переднему и медиальному контурам (тромботические массы) и анэхогенной (жидкостной) полостью по латеральному контуру размером 23,0х15,4 мм. В режиме ЦДК и ЭОДС полость полностью окрашивалась (рис. 7), регистрировали двунаправленный артериальный кровоток (ЛСК до 0,5-0,6 м/с).
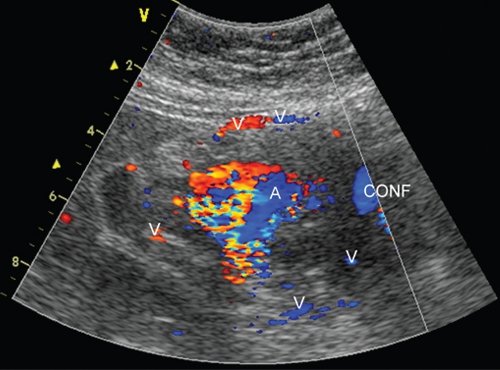
Режим ЦДК: A - аневризма, CONF - конфлюенс воротной вены, V - венозные коллатерали.
При дооперационном обследовании (включавшем также компьютерную и магнитно-резонансную томографию) источником ЛА была определена желудочно-двенадцатиперстная артерия. Пациентке выполнили рентгеноэндоваскулярную эмболизацию желудочнодвенадцатиперстной артерии от полости аневризмы до ее устья спиралями Gianturco MReye® (COOK). При контрольном интраоперационном УЗИ в режимах ЦДК и ЭОДС просвет образования окрашивался в проекции нижнего полюса, в режиме импульсной допплерографии регистрировался редуцированный, по сравнению с предыдущим исследованием, артериальный кровоток (рис. 8).
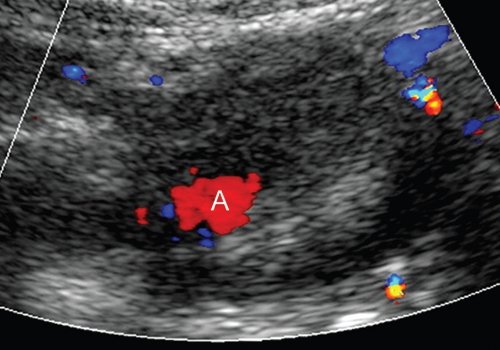
Полость аневризмы (А) в режиме ЦДК окрашивается менее интенсивно, по сравнению с дооперационным исследованием.
После чего выполнили рентгеноэндоваскулярную эмболизацию устий нижних поджелудочно-двенадцатиперстных артерий взвесью частиц PVA. При контрольном интраоперационном УЗИ в режимах ЦДК и ЭОДС просвет образования не окрашивался, кровоток внутри аневризмы в режиме импульсной допплерографии не регистрировался (рис. 9).
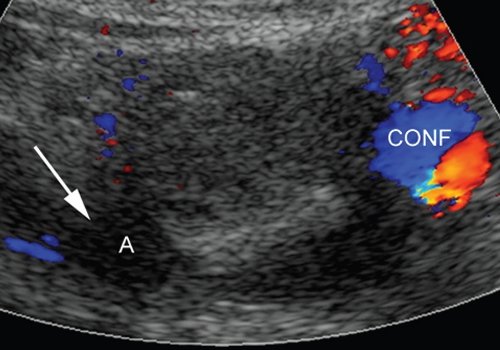
Полость аневризмы (А) в режиме ЦДК не окрашивается (CONF - конфлюенс воротной вены).
Далее был проведен УЗ-мониторинг полости аневризмы в 1-е, 3-и (рис. 10) и 7-е и сутки. В режимах ЦДК и ЭОДС полость аневризмы не окрашивалась.
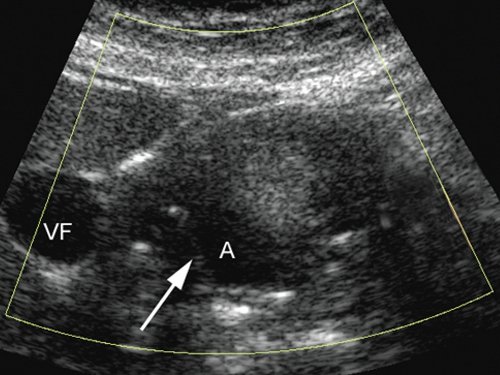
Полость аневризмы (А) в режиме ЦДК не окрашивается, в ней определяются линейные гиперэхогенные структуры. Контуры кисты нечеткие, ровные (VF - желчный пузырь).
Контрольное УЗИ также было проведено через 45 дней после эндоваскулярного вмешательства. В режимах ЦДК и ЭОДС просвет данной полости не окрашивался (рис. 11).
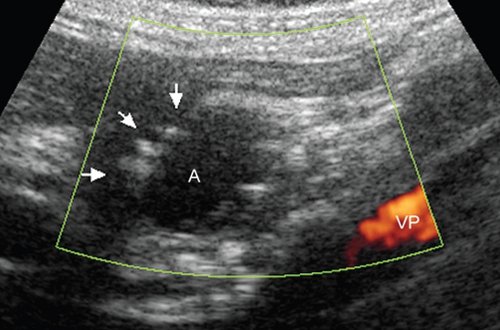
Полость аневризмы (А) в режиме энергии отраженного допплеровского сигнала не окрашивается. По внутреннему латеральному контуру полости определяются округлые гиперэхогенные структуры (указаны стрелками), контуры кисты четкие, ровные (продольное сканирование, VP - воротная вена).
Во всех случаях при проведении эндоваскулярного лечения в раннем послеоперационном периоде пациентам проводили регулярное ультразвуковое мониторирование состояния полости аневризмы (через 1, 3, 5 дней после вмешательства, в случае окончания лечения - при выписке). При выполнении эмболизации полости аневризмы окклюзирующими спиралями, окклюдером и спиралями, а также после эмболизации артерииисточника полное выключение аневризмы из кровотока при проведении УЗ-мониторирования отмечали через 3-7 дней после оперативного вмешательства.
Целью послеоперационного мониторирования после рентгеноэндоваскулярных вмешательств также являлась оценка состояния селезенки. Так, в одном наблюдении после рентгеноэндоваскулярной окклюзии селезеночной артерии спиралями у пациентки при проведении УЗИ был диагностирован инфаркт селезенки. Динамическое наблюдение за зоной инфаркта на фоне плохо купирующихся признаков хронического панкреатита по данным УЗИ выявило абсцедирование этой зоны. Пациентке была выполнена дистальная резекция поджелудочной железы со спленэктомией.
Результаты проведенного оперативного лечения свидетельствуют о том, что при выполнении в качестве I этапа эндоваскулярной окклюзии заинтересованной в патологическом процессе артерии кровопотеря составила 750,0 мл, в то время как при открытом оперативном вмешательстве без предварительной эмболизации она варьировала от 3500 до 7000 мл.
При выполнении открытого оперативного вмешательства в 1 (4,0%) случае было проведено интраоперационное УЗИ, данные которого позволили четко определить локализацию ЛА селезеночной артерии, входящей в воспалительный инфильтрат.
Заключение
При наличии ЛА ультразвуковое исследование позволяет без лучевой нагрузки на пациента диагностировать аневризму, оценить сосуд, являющийся ее источником, и изменения, вызванные хроническим панкреатитом. Таким образом, проведение комплексного УЗИ позволяет на первом этапе диагностики получить практически все необходимые данные для определения тактики лечения пациента.
"Слабым" местом ультразвукового метода исследования является диагностика связи полости ЛА с ГПП. Учитывая выявление этой связи при размере ЛА более 60,0 мм, всем пациентам с такими размерами ЛА целесообразно дополнять исследование магнитно-резонансной холангиопанкреатографией, которая позволяет более точно оценить состояние панкреатического и билиарного протокового "дерева".
В доступной нам литературе отсутствуют сведения об использовании интраоперационного УЗ-мониторирования на этапах рентгеноэндоваскулярного вмешательства при мини-инвазивном лечении. Однако наш опыт свидетельствует о том, что УЗ-мониторирование эффективно в интраоперационной оценке качества манипуляции и дает возможность корректировать тактику оперативного вмешательства. Интраоперационное УЗИ позволило без дополнительного введения контрастного вещества выявить не диагностированный до операции второй источник аневризмы и тем самым скорректировать ход лечебной манипуляции.
Следует отметить, что ЛА - серьезное осложнение течения хронического панкреатита. Лечение таких больных затрудняется их общим соматическим состоянием. Так, несмотря на все усилия, 3 больных умерли, это составило 12,0% от общего числа пациентов в группе. Результаты нашего наблюдения за пациентами с ложными аневризмами, развившимися на фоне хронического панкреатита, свидетельствуют о том, что тактика лечения в каждом случае должна пределяться индивидуально, с учетом клинических данных конкретного больного и наличия у него осложнений.
Литература
- Hanyu F., Imaizumi T., Pancreas et. al. editors. Rinsho Gekagaku 3, Shoukakigekagaku. Tokyo: Asakura, 1999. P. 389-432.
- Степанова Ю.А. Лучевые методы диагностики кистозных образований поджелудочной железы и парапанкреатической зоны на этапах хирургического лечения. Дис. ... докт. мед. наук. М., 2009. 398 с.
- Буриев И.М., Корняк Б.С., Азимов Р.Х., Панова Н.В. Редкое осложнение постнекротической кисты поджелудочной железы (случай из практики) // Анналы хирургической гепатологии. 2000. N1. С. 77-80.
- Покровский А.В. "Клиническая ангиология". Руководство в 2 томах. М.: "Медицина", 2004. Т. 2. С. 117-128.
- Ido K., Isobe K., Kimura K. et al. Case of hemorrhagic pancreatic pseudocyst in which ultrasound imaging was useful // J Med Ultrasonics. 2004. 31:41-45.
- Данилов М.В., Федоров В.Д. Хирургия поджелудочной железы: руководство для врачей. М.: Медицина, 1995. 512 с.
- Boschmann H., Zimmermann H-B., Wiechmann T. et al. Rupturiertes Milzarterienaneurysma - eine seltene Ursache rezidivierender gastrointestinaler // Blutungen Med Klin. 2001. 96: 351-354 (Nr. 6).
- Urakami A., Tsunoda T., Kubozoe T. et al. Rupture of a bleeding pancreatic pseudocyst into the stomach // J Hepatobiliary Pancreat Surg. 2002. 9:383-385.
- Kaman L., Sanyal S., Menakuru S.R. et al. Pseudoaneurysm of the pancreaticoduodenal artery, a rare cause of hemosuccus pancreaticus: report of a case // Surg Today. 2004. 34(2): 181-184.
- Alamo J.M., Gomes M.A., Tamayo M.J. et al. Mycotic pseudoaneurysms after liver transplatation // Transplant Proc. 2005. 37(3): 1512-1514.
- Lagana D., Carrafiello G., Mangini M. et al. Multimodal approach to endovascular treatment of visceral artery aneurysms and pseudoaneurysms // Eur J Radiol 2006. 59(1): 104-111.
- Таразов П.Г., Розенгауз Е.В., Павловский А.В., Попов С.А. Псевдоаневризма селезеночной артерии - осложнений хронического панкреатита (наблюдение из практики) // Медицинская визуализация. 2009. N3. С. 31-36.
- Вишнякова М.В., Лерман А.В., Сташук Г.А. и др. Диагностика и эндоваскулярное лечение псевдоаневризмы селезеночной артерии (клиническое наблюдение) // Диагностическая и интервенционная радиология. 2010. N4. С. 97.
- Pulcini G., D`Adda F., Lanzi S. et. al. Aneurysms of the superior mesenteric artery // Ann. Ital. Chir. 2002. 73(2): 129-136.
- Seriki D.M., Abidia A., Butterfield J.S. et al. Endovascular stent graft: treatment of pseudoaneurysm of the superior mesenteric artery // Cardiovasc. Interv. Radiol. 2004. 27: 271-273.
- Gabelman A., Gorich J., Merkle E.M. Endovascular treatment of a visceral artery aneurysms // J Endovasc Ther. 2002. 9(1): 38-34.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Публикации по теме
- Ультразвуковая диагностика мальформации селезеночной вены - Бычкова Е.В.
- Ультразвуковая диагностика бедренной и седалищной нейропатии в неврологической практике - Кислякова М.В.
- Возможности ультразвукового метода исследования в диагностике и лечении ложных аневризм висцеральных сосудов - Степанова Ю.А.
- Цветовое дуплексное сканирование в диагностике патологической извитости внутренних сонных артерий - Кузьмичева И.Н.
- Применение алгоритма комплексного ультразвукового исследования сосудистой системы головного мозга при гипертонической энцефалопатии - Белова Л.А.

