Сравнительный анализ данных импульсно-волновой эластографии и эластометрии объемных образований печени in vivo и на макропрепарате
Рубрика: Технологии, методики и стандарты

УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Введение
Внедрение в клиническую практику новых технологий ультразвуковых исследований (эластографии и эластометрии) позволяет детально изучить состояние органов и тканей. Однако диагностическая ценность различных эхографических методик в дифференциальной диагностике новообразований печени изучена недостаточно. Нет четких дифференциальных признаков новообразований печени по данным ультразвуковой томографии, отсутствует сравнительный анализ как качественных, так и количественных методик. Диагностика и оценка характера очаговых изменений печени сопряжены с большими трудностями: необходимостью учета большого разнообразия заболеваний, сопровождающихся очаговыми изменениями печени; возможным сочетанием доброкачественных и злокачественных изменений, отсутствием высокоспецифичных признаков. Необходимость повышения эффективности диагностики опухолевых поражений печени обусловливает актуальность разработки новых методик и оценку их эффективности [1-3].
Цель эксперимента заключалась в сопоставлении данных эластографии и эластометрии объемных образований печени в дооперационном периоде in vivo и на макропрепарате ex vivo. При этом оценивалась структура опухоли, ее эластичность по отношению к окружающей паренхиме и к опухолям другого генеза.
Материал и методы
В исследование макропрепарата печени ex vivo было включено 36 наблюдений. Всем 36 пациентам проводилось хирургическое лечение по поводу опухолевого поражения печени. Характер оперативных вмешательств зависел от распространенности опухолевого процесса. В 47,2% случаев была выполнена правосторонняя гемигепатэктомия, в 25,0% - резекции печени, в 11,1% - левосторонняя гемигепатэктомия, в 8,3% - расширенная правосторонняя гемигепатэктомия. В 5,6% выполнены атипичные резекции и в 2,8% - расширенная левосторонняя гемигепатэктомия.
По данным гистологического исследования: в 61,1% случаев у 22 больных был выявлен гепатоцеллюлярный рак, в 27,8% (10) - метастазы колоректального рака, у 3 пациентов (8,3%) - фокальная нодулярная гиперплазия и в одном случае (2,8%) - гепатоцеллюлярная аденома. В дооперационном периоде у данной группы пациентов оценивался размер опухоли и глубина расположения ее от поверхности кожи. У пациентов с первичными опухолями печени в 11 (42,3%) случаях размеры опухолей были более 5 см, в 10 (38,5%) - до 3 см, а в 5 (19,2%) - от 3 до 5 см. У пациентов с метастазами колоректального рака в 4 (40%) наблюдениях очаги были размером до 3 см, в трех и трех наблюдениях - от 3 до 5 см и более 5 см соответственно.
Распределение опухолевых узлов по глубине залегания в паренхиме печени от поверхности кожи: у пациентов с первичными опухолями печени в 57,7% (15) случаев опухоли располагались на глубине от 4 до 6 см, в 34,6% (9) - на глубине от 2 до 4 см, у 2 (7,7%) - на глубине более 6 см. У больных с метастазами колоректального рака в 60% (6) наблюдений очаги располагались на глубине от 4 до 6 см, в 3 (30%) - от 2 до 4 см, в одном (10%) - более 6 см.
Для проведения эластографии и эластометрии самыми оптимальными считались опухоли размерами от 2 до 5 см, располагавшиеся на глубине от 2 до 6 см. В исследованиях на макропрепарате печени оптимальными оказались размеры опухолей от 0,5 до 5 см. При проведении эластографии с ручной компрессией на макропрепарате печени предпочтительными считались размеры опухолей от 1 до 5 см, с учетом того, что неизмененная паренхима вокруг опухоли должна быть не менее 0,5 см толщиной, что согласуется с мнением других исследователей [4].
Результаты
По данным эластографии с ручной компрессией, как на дооперационном этапе, так и в эксперименте на макропрепарате, было выделено 6 вариантов эластограмм с разной степенью жесткости опухолевой ткани. Варианты: В1- мягкой консистенции, В2 - мягкий центр и плотный ободок по периферии, В3 - мягкой консистенции с жесткими включениями, В4 - жесткой консистенции с мягкими включениями, В5 - жесткой консистенции, В6 - жесткий центр и мягкий по краю [5].
В группе пациентов с первичной опухолью печени в 12 (46,2%) случаях структура опухоли была мягкой в центральных отделах и жесткой по периферии. В 26,9% (7) наблюдений опухоль имела жесткую структуру с мягкими включениями. У 5 пациентов (19,2%) опухоль была мягкой консистенции с плотными включениями и у 2 (7,7%) - мягкой консистенции. В группе пациентов с метастазами колоректального рака в печень в 8 (80,0%) наблюдениях очаги были жесткими, в одном (10%) очаги имели жесткий центр и мягкий край, еще в одном случае - мягкий центр и жесткий край.
При исследованиях макропрепарата печени с первичной опухолью в 13 (50,0%) случаях структура опухоли была мягкой в центральных отделах и жесткой по периферии. В 6 наблюдениях (23,1%) опухоль имела жесткую структуру с мягкими включениями, в 5 (19,2%) - опухоль была мягкой консистенции с плотными включениями и в 2 (7,7%) - мягкой консистенции. В группе с метастазами колоректального рака в печень в 7 (70,0%) наблюдениях очаги были жесткими, в 3 (30%) случаях очаги имели жесткий центр и мягкий край.
По данным эластографии с методикой ARFI, как в дооперационном периоде, так и в эксперименте на макропрепарате, было выделено 3 варианта эластограмм с разной степенью жесткости опухолевой ткани по отношению к неизмененной паренхиме печени [5]. Варианты: В1 - мягкой консистенции, В2 - жесткой консистенции, В3 - смешанной консистенции. При исследовании в режиме ARFI в группе пациентов с первичными опухолями печени в 13 (50,0%) наблюдениях опухоли имели смешанную консистенцию, в 10 (38,5%) - мягкую и у 3 пациентов (11,5%) - жесткую консистенцию. В группе с метастазами колоректального рака у 7 (70,0%) больных очаги были жесткими, в 3 наблюдениях (30,0%) - смешанной консистенции. При исследовании в режиме ARFI макропрепарата печени с первичными опухолями в 14 (53,9%) случаях опухоли имели смешанную консистенцию, в 9 (34,6%) наблюдениях были мягкой консистенции и в 3 (11,5%) - жесткой. В группе с метастазами колоректального рака в 9 случаях (90,0%) очаги были жесткими, в одном (10,0%) - смешанной консистенции.
По данным эластометрии с методикой SWV (Shear wave velocity) оценивался скоростной показатель жесткости опухолевой ткани и неизмененной паренхимы печени, у пациентов в дооперационном периоде и на макропрепарате печени.
У пациентов с метастазами колоректального рака в печень были зафиксированы самые низкие скоростные показатели СРПВ в неизмененной паренхиме печени. Значения их варьировали в пределах от 1,06 (min) до 3,02 (max) м/с, средние - 1,78 м/с и медиана - 1,75 м/с. У пациентов с первичными опухолями печени показатели СРПВ в неизмененной паренхиме были самыми высокими, в пределах от 1,21 (min) до 3,94 (max) м/с, средние значения - 2,28 м/с, медиана - 1,95 м/с, за счет наличия выраженных дистрофических изменений. Низкие скоростные показатели СРПВ в неизмененной паренхиме печени были в макропрепарате с метастазами колоректального рака. Значения их варьировали в пределах от 1,27 (min) до 2,52 (max) м/с, средние - 1,91 м/с и медиана - 1,98 м/с. В макропрепарате с первичной опухолью печени показатель СРПВ в неизмененной паренхиме был высоким, в пределах от 1,06 (min) до 4,01 (max) м/с, средние значения - 2,36 м/с, медиана - 2,16 м/с, в большинстве случаев за счет фиброзных и цирротических изменений паренхимы печени у пациентов с вирусными гепатитами.
В группе пациентов с метастазами колоректального рака скоростной показатель СРПВ в опухолевой ткани был высоким, в диапазоне от 3,12 до 4,22 м/с, средний скоростной показатель был 3,60 м/с, медиана среднего скоростного показате- ля - 3,62 м/с. В группе пациентов с первичными опухолями печени скоростной показатель СРПВ был ниже и варьировал от 1,12 до 3,68 м/с, средний скоростной показа- тель - 2,14 м/с, медиана - 2,05 м/с. В макропрепарате печени с метастазами колоректального рака скоростной показатель СРПВ в опухолевой ткани был высоким, в диапазоне от 2,76 до 4,66 м/с, средний скоростной показатель был 3,63 м/с, медиана среднего скоростного показателя - 3,51 м/с. В макропрепаратах с первичными опухолями печени скоростной показатель СРПВ был ниже и варьировал от 1,1 до 3,47 м/с, где средний скоростной показатель - 2,08 м/с, медиана - 1,97 м/с.
Заключение
При проведении эластометрии печени и сопоставлении с данными морфологического исследования нами было отмечено, что при вирусном поражении паренхимы печени (при нарастании фиброза) средние показатели СРПВ опухоли печени в большинстве случаев всегда ниже средних показателей СРПВ неизмененной паренхимы печени, что является критерием дифференциальной диагностики гепатоцеллюлярного рака, и согласуются с данными других авторов [6-7]. При гепатоцеллюлярном раке показатель СРПВ в большинстве случаев увеличивался от центра опухоли к ее периферии, а при фокальной нодулярной гиперплазии, наоборот, - от периферии к ее центру.
При исследовании опухоли печени на дооперационном этапе показатели эластометрии и эластографии совпадали с показателями эластографии и эластометрии при исследовании опухоли печени на макропрепарате. Средние показатели СРПВ опухолевой ткани in vivo между группами пациентов с первичными опухолями печени и метастазами колоректального рака в печень были достоверными (р < 0,05), а в неизмененной паренхиме печени отмечалась тенденция к достоверности (р = 0,089). Средние показатели СРПВ опухолевой ткани in vitro между группами пациентов с первичными опухолями печени и метастазами колоректального рака в печень были достоверными (р < 0,05).
Показатели информативности эластографии с ручной компрессией для первичных опухолей печени (n = 26): чувствительность - 31,82%, специфичность - 100%, точность - 42,31%, прогностическая ценность положительного результата - 100%, прогностическая ценность отрицательного результата - 21,05%. Показатели информативности эластографии с ручной компрессией для метастазов в печень колоректального рака (n = 10): чувствительность - 90%, точность - 90%, прогностическая ценность положительного результата - 100%, прогностическая ценность отрицательного результата - 0%. Показатели информативности эластографии с технологией ARFI для первичных опухолей печени (n = 26): чувствительность - 40,91%, специфичность - 100%, точность - 50%, прогностическая ценность положительного результата - 100%, прогностическая ценность отрицательного результата - 23,53%. Показатели информативности элас- тографии с технологией ARFI для метастазов в печень колоректального рака (n = 10): чувствительность - 100%, точность - 100%, прогностическая ценность положительного результата - 100%.
Для расчета информативности показателей эластометрии в дифференциальной диагностике новообразований печени, в эксперименте с макропрепаратом, нами были выбраны пороговые значения СРПВ - 2,0 и 1,5 м/с. Наиболее информативными были показатели при пороговом значении 1,5 м/с, где точность - 75%, чувствительность - 81%, специфичность - 25%, прогностическая ценность положительного результата - 90%, прогностическая ценность отрицательного результата - 14%. В качестве иллюстрации приводим одно из наших клинических наблюдений.
Клиническое наблюдение
Пациентка В., 37 лет, находилась на стационарном лечении в отделении опухолей печени и поджелудочной железы с диагнозом: "опухоль печени". По данным МРТ (рис. 1-5) (исследование было выполнено с контрастным веществом примавист) имело место опухолевое образование печени, возможно, вторичного характера?
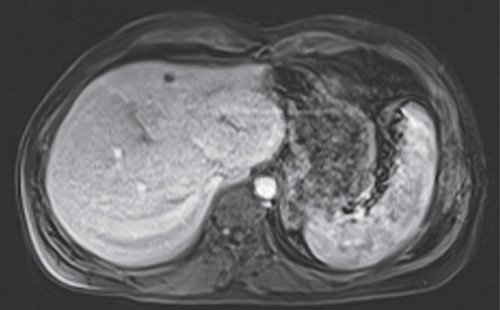
Рис. 1. МРТ печени с контрастным веществом примавист. Артериальная фаза.
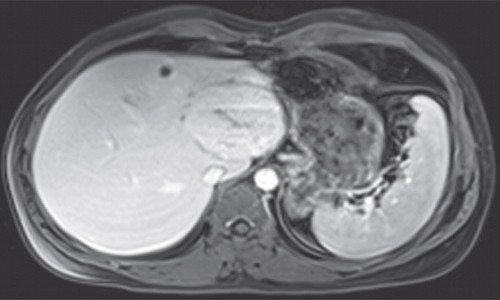
Рис. 2. МРТ печени. Венозная фаза.
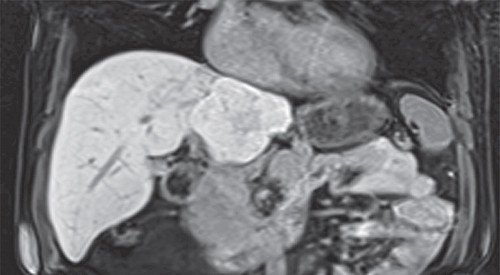
Рис. 3. МРТ печени. Корональная проекция.
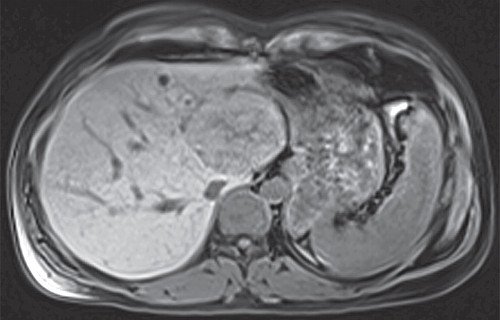
Рис. 4. МРТ печени, Т1ви. Натив.
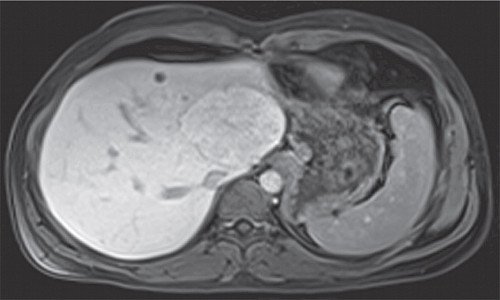
Рис. 5. МРТ печени. Отсроченная фаза.
По данным комплексного ультразвукового исследования (рис. 6-11) (с эластографией и эластометрией): печень увеличена (КВР правой доли = 16,5 см), контур правой доли ровный, контур левой доли бугристый. Структура с дистрофическими изменениями (показатель СРПВ варьировал от 1,71 до 1,96 м/с). На этом фоне в С2-3 определяется изоэхогенное образование размером 6,5 х 5,7 см (по данным эластографии и ARFI, мягкой консистенции с плотными участками, показатель СРПВ в центральных отделах варьировал от 3,09 до 4,14 м/с). В других сегментах печени - без очаговых изменений. В С4 определялась киста до 0,8 см. Внутрипеченочные желчные протоки не расширены. Заключение: УЗ-картина объемного образования в левой доле печени больше соответствует фокальной нодулярной гиперплазии.
Комплексное УЗТ (эластография и эластометрия) in vivo
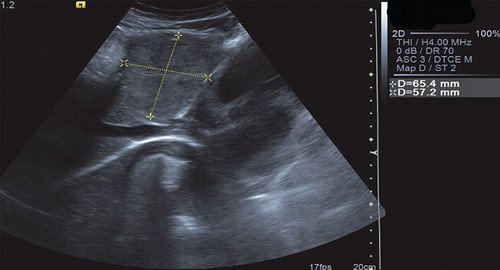
Рис. 6. В-режим. Объемное образование в левой доле печени.
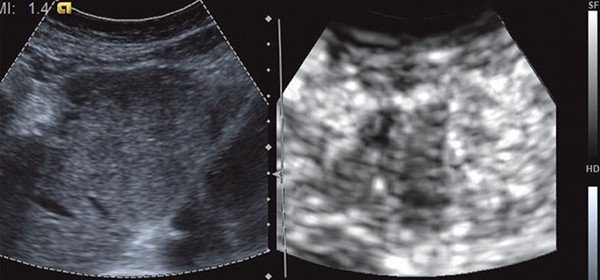
Рис. 7. Эластография с ручной компрессией (в режиме серошкального кодирования). По жесткости объемное образование в левой доле печени имеет такую же консистенцию, как и неизмененная паренхима печени. В центральных отделах опухоли определяются жесткие включения.
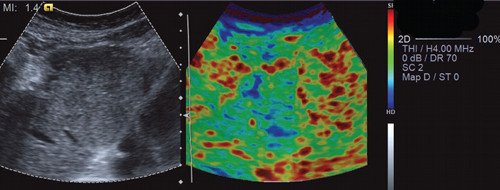
Рис. 8. Элатография с ручной компрессией (в режиме цветового кодирования). На эластограмме видно, что объемное образование в левой доле печени - мягкой консистенции с жесткими включениями (вариант эластограммы № 3).
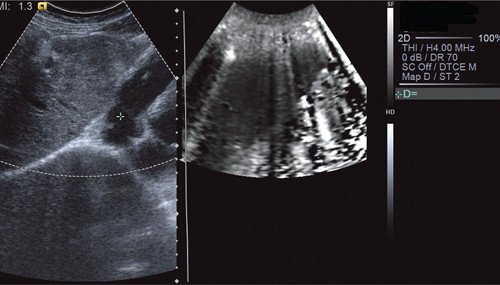
Рис. 9. Эластография с методикой ARFI. Объемное образование в левой доле печени по периферии - мягкой консистенции, в центральных отделах - жесткой консистенции (вариант эластограммы № 3).
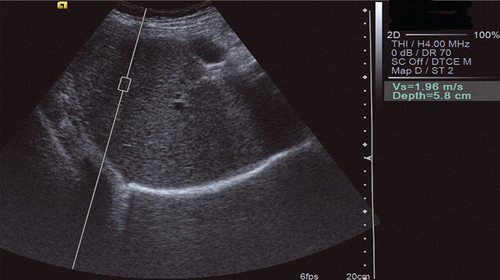
Рис. 10. Эластометрия неизмененной паренхимы печени. Показатель СРПВ (скорость распространения поперечной волны) варьировал от 1,71 до 1,96 м/с - дистрофические изменения паренхимы печени.
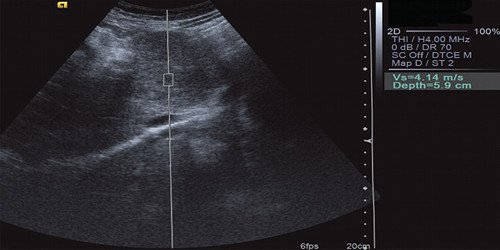
Рис. 11. Эластометрия объемного образования в левой доле печени. Показатель СРПВ (скорость распространения поперечной волны) в центральных отделах опухоли был высоким (от 3,09 до 4,14 м/с) за счет фиброзных изменений в центральных отделах ФНГ.
Проведено оперативное лечение: сегментэктомия печени 2-3 (при ревизии в брюшной полости в левой доле печени в проекции 2-3-сегментов определяется опухолевый узел размером до 6 см, плотно-эластичной консистенции).
Ход операции
Срединная лапаротомия. При ревизии в брюшной полости в левой доле печени в проекции 2-3-сегментов определяется опухолевый узел до 6 см в диаметре, плотно-эластичной консистенции. Дополнительная левая печеночная артерия отходит от левой желудочной артерии. Других изменений в печени не выявляется. Другой патологии в брюшной полости нет. Мобилизована левая доля печени. Левая печеночная вена выделена и перевязана. Электроножом, с отступом от опухоли на 0,5 см, намечена линия резекции. Гепатодуоденальная связка пережата. Парциально, с предварительной перевязкой паренхимы печени, выполнена сегментэктомия 2-3 печени. Культя печени дополнительно прошита, перитонизирована остатками серповидной связки. Гепатодуоденальная связка пережималась на 13 минут. Брюшная полость дренирована 2 дренажами. Гемостаз. Рана ушита послойно. Кровопотеря: 300 мл (рис. 17).
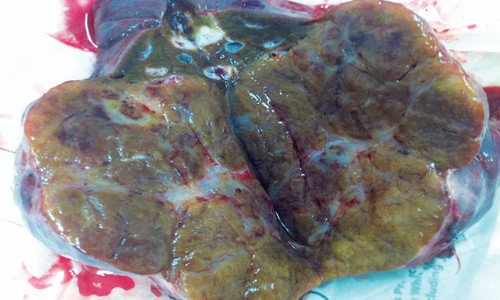
Рис. 17. Макропрепарат печени. Нодулярная гиперплазия печени с участками фиброза в центральных отделах.
Исследование макропрепарата печени: по данным эластографии и ARFI объемное образование печени мягкой консистенции с жесткими включениями; по данным эластометрии показатель СРПВ в центральных отделах опухоли был от 3,38 до 3,96 м/с, в периферических отделах - от 2,41 до 2,90 м/с. Показатель СРПВ неизмененной паренхимы печени варьировал от 1,74 до 1,80 м/с (рис. 12-16).
Комплексное УЗТ (эластография и эластометрия) на макропрепарате печени ex vivo
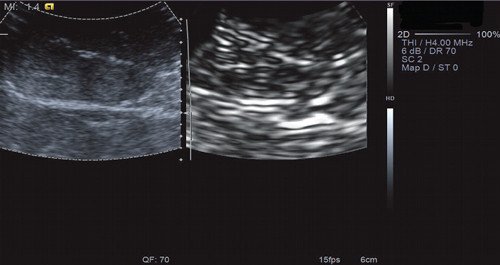
Рис. 12. Эластография с ручной компрессией (в режиме серошкального кодирования). Объемное образование печени - мягкой консистенции и не отличалось от неизмененной паренхимы печени. Коэффициент компрессии QF = 70.
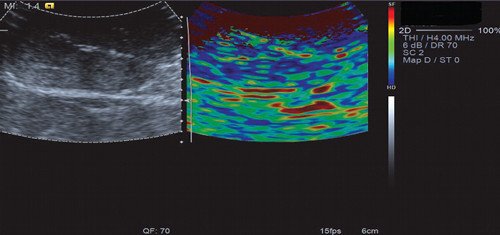
Рис. 13. Эластография с ручной компрессией (в режиме цветового кодирования). На эластограмме видно, что объемное образование печени - мягкое с жесткими включениями (вариант эластограммы № 3).
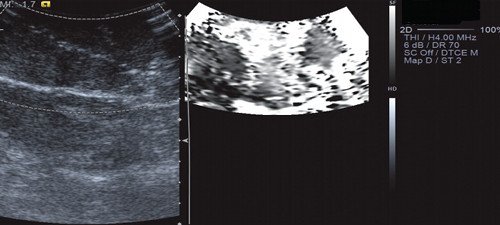
Рис. 14. Эластография с методикой ARFI. Объемное образование печени мягкой консистенции с жесткими включениями (вариант эластограммы № 3).
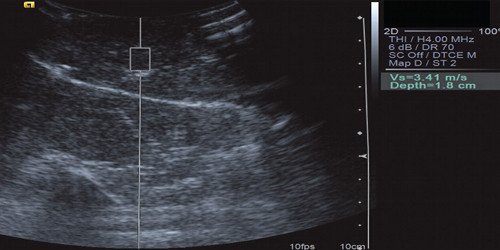
Рис. 15. Эластометрия объемного образования печени. Показатель СРПВ (скорость распространения поперечной волны) в центральных отделах опухоли был от 3,38 до 3,96 м/с - фиброзные изменения в центральных отделах ФНГ.
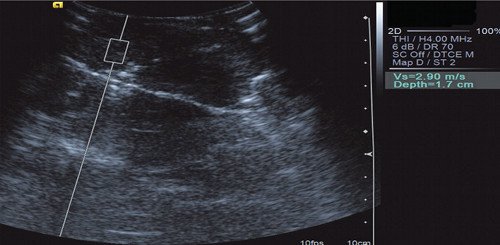
Рис. 16. Эластометрия объемного образования печени. Показатель СРПВ (скорость распространения поперечной волны) в периферических отделах опухоли был от 2,41 до 2,90 м/с.
Гистологическое заключение: фрагмент ткани печени размером 9 × 3 × 3,5 см. На расстоянии 2,5 см от края резекции - образование овальной формы, в капсуле, размером 6 × 5 × 2,5 см, плотной консистенции, бледно-коричневого цвета с тяжами плотной белесоватой ткани. В крае резекции элементов опухолевого роста не обнаружено. Образование в печени морфологически соответствует очаговой узловой гиперплазии.
Заключительный диагноз: "нодулярная гиперплазия печени".
Литература
- Шифф Ю.Р., Соррел М.Ф., Меддрей У.С. Болезни печени по Шиффу/изд. группа "ГЕОТАР-Медиа", Москва, 2010 С. 151-91.
- Nightingale K., McAleavey S., Trahey G. Shear-wave generation using acoustic radiation force: in vivo and ex vivo results // UltrasoundMedBiol. 2003; 29(12): 1715-23.
- Гальперин Э.И., Дюжевой Т.Г. Лекции по гепатопанкреатобилиарной хирургии /Видар-М, 2011; С. 253-71.
- Nightingale K., Soo M.S., Nightingale R., Trahey G. Acoustic radiation force impulse imaging: in vivo demonstration of clinical feasibility // UltrasoundMedBiol. 2002; 28(2): 227-35.
- Garra B.S. Imaging and estimation of tissue elasti-city by ultrasound// Ultrasound Q. 2007; 23(4): 255-68.
- Friedrich-Rust M., Oug M.F., Martens S. et al. Performance of transient elastography for staging of liver fibrosis: a meta-analysis // Gastroenterology 2008; 134: 960-74.
- Борсуков А.В. Эластография в клинической гепатологии. Изд.: Смоленская городская типография. Смоленск, 2011; 215 с.

УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Публикации по теме
- 3D УЗИ в диагностике наружного эндометриоза - George Condous
- Первый опыт применения High Definition Volume Imaging (HDVI) при ультразвуковом исследовании в акушерстве - Фризова Вероника
- Сравнительный анализ данных импульсно-волновой эластографии и эластометрии объемных образований печени in vivo и на макропрепарате - Бердников С.Н.
- Эластография: новые разработки в области ультразвукового оборудования для дифференциальной диагностики узловых образований в щитовидной железе - Салах Эльвагди (Salah Elwagdy)
- Роль трехмерного УЗИ при ведении беременности неустановленной локализации - George Condous

