Микроанатомическая оценка структур в клинической эхографии - возможности и перспективы
Рубрика: Эхография в урологии

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Последние несколько лет отличают клиническую эхографию внедрением в практику ультразвуковых систем так называемого "премиум-класса". В первую очередь они отличаются высокой разрешающей способностью (до 0,1 мм) с соответствующей возможностью дифференцировки тканевых текстур. Таким образом, казалось бы, появилась возможность оценки нормальных структур и патологического процесса на качественно новом уровне. Однако ожидаемого скачка в эхографии, выражаемого в заключениях по характеристике нормальных и измененных структур относительно онтогенеза и патоморфогенеза на соответствующем уровне явно не наблюдается [1].
Упоминаемые технологии не обеспечили значительного снижения числа расхождений в оценке эхографических данных при наиболее распространенных вариантах острой абдоминальной патологии, в частности при травмах, острых воспалительных процессах органов брюшной полости, забрюшинного пространства, мошонки специалисты по ультразвуковой диагностике и клиницисты не имеют сегодня единого мнения, а также общих установок в интерпретации эхографических изображений. Широко не представлены разработки по ассоциациям изменений тональных прогрессий на эхограммах относительно морфологических проявлений так называемых общепатологических процессов (острого воспаления, ишемии, дистрофических изменений и т. д.). Фактически не учитываются закономерности трансформаций теневых градаций в соответствии с изученными фазами эволюций патоморфогенеза и компенсаторно-регенеративных реакций. Абсурдность ситуации проявляется в частой нерешимости назвать врачомспециалистом УЗИ свое заключение эхографическим диагнозом, пропуская вперед значимость клинических проявлений патологических состояний. Подобная позиция зачастую нивелирует возможности эхографии, превращая ее в рутинный метод бесконечного накопления аналитических данных. Остаются в стороне и практически не учитываются стратегические наработки в клинической морфологии, обосновывающие приоритет значимости оценки патологических состояний именно на так называемом доклиническом этапе [2]. Как следствие большинство лечащих врачей продолжают ориентироваться на клинические проявления патологического процесса. Очевидно, перечисленное никак не способствует уменьшению диагностического периода и объективизации своевременного выбора рациональной лечебной тактики, что собственно и позволяет обозначить ситуацию в абдоминальной эхографии как кризисную.
Принципиально следующее: столь ли нова ситуация, представляемая как кризисная? Или с нечто подобным практической медицине приходилось сталкиваться?
Обратимся к истории медицины. Уместно и весьма наглядно в нашем аспекте вспомнить об истории развития клинической морфологии (или, в частности, патоморфологии), которую условно можно разделить на три периода: макроскопический, микроскопический и ультрамикроскопический [3].
Изначально, от древних времен почти до середины XIX века изменения органов при различных заболеваниях изучались лишь визуально, без специальных оптических инструментов - 1-й период. При этом учитывались размеры, общий вид, цвет, консистенция, дополнительные включения и признаки травматических повреждений. Среди крупнейших обобщающих трудов этого периода выделяется работа одного из основоположников патологической анатомии, итальянского врача и анатома Джованни Морганьи "О местонахождении и причинах болезней, открываемых посредством рассечения". В ней впервые была представлена идея сопоставления симптомов различных патологических состояний с морфологическими изменениями органов. Собственно реализация этой идеи по сути и явилась началом развития клинико-анатомического направления при изучении заболеваний и травматических повреждений у человека. Кстати, уместно напомнить, что исключительно "посредством рассечения" морфологического субстрата Рене Лаэннеку удалось обосновать практическую значимость акустического метода в диагностике с помощью предложенного им стетоскопа. Изначально, конечно, Лаэннек выслушивал пораженные патологическим процессом ткани, образно говоря, "разглядывал их ухом". Однако в итоге он сопоставлял свои данные именно с результатами, полученными "посредством рассечения" и непосредственной визуальной оценки изучаемых органов, подчеркивая важность подобных ассоциаций. Завершение 1-го, макроскопического периода обозначается выходом фундаментального руководства австрийского патолога, чеха по происхождению, основателя первой в Европе самостоятельной кафедры патологической анатомии в Венском университете в 1844 г. Карла Рокитанского. В этом многотомном труде представлены классификации и описания основных изучаемых в тот исторический период заболеваний. Как раз в этот период и наметился определенного рода кризис, который выражался в трудности проведения четких параллелей между морфологически, казалось бы, не измененными органами и многообразными, "беспричинными", с точки зрения анатомии, нарушениями их функции. "Аналитический" вывод для большинства медиков-академистов напрашивался сам собой: в основе заболеваний изначально лежат исключительно функциональные изменения.
Наметившийся кризис был преодолен в середине XIX века с распространением светооптических микроскопов, достаточно мощных для оценки структур на уровне тканей и клеток. Наступление "микроскопического" периода развития патологической анатомии условно можно обозначить с момента выхода фундаментальных работ Рудольфа Вирхова, обобщенных в классическом труде "Целлюлярная патология" (1858). Применение микроскопа позволило объяснить многие функциональные нарушения изначально структурными изменениями до деструкций на уровне тканей и клеток вследствие ишемических, воспалительных, травматических и других причин.
Фактически идентичная кризисная ситуация сложилась к середине ХХ века: неразрешимыми оставались вопросы морфологической основы функциональных изменений уже на уровне клетки. Кризис опять-таки был разрешен с внедрением в практику электронного микроскопа и развитием ультрамикроскопических технологий. Эти исследования обозначили начало развития 3-го периода патологической морфологии - "ультрамикроскопического".
Таким образом, при ознакомлении с этапами развития патоморфологических дисциплин очевидна эволюция воззрений на основу морфологических изменений, сопровождающих общепатологические процессы. Причем сущности прикладных теорий в оценке клинического значения морфологических трансформаций на каждом из исторических этапов целиком зависели от прогресса технических возможностей, в частности от параметров разрешающей способности оптических систем при оценке морфологических объектов до ультраструктур включительно.
Цель предельно кратко представленного экскурса в историю развития клинической морфологии очевидна: продемонстрировать явную аналогию с развитием "звуковидения" в оценке внутренних структур и эхографических признаков трансформации последних при общепатологических процессах.
Сегодня клиническая эхография, повидимому, как раз и переживает кризис своего первого - "макроскопического" этапа. Появились ультразвуковые технологии, обеспечивающие недоступную для недавнего прошлого разрешающую способность - в десятые доли миллиметра. По-видимому, приходит время начала развития второго этапа эхографии - "микроскопического". Относительно именно "клинического звуковидения", точнее будет обозначить этот этап несколько по-другому - "микроанатомический". Предлагаемый термин позаимствован из названия фундаментальной работы "Human microscopic anatomy. An Atlas for Students of Medicine and Biology" [4]. В российском издании он впервые встречается в монографии А.А. Заварзина [5]. Этот термин наиболее адекватен относительно оценки эхографических изображений, получаемых на сканерах с разрешающей способностью в десятые доли миллиметра. Это продиктовано следующими соображениями.
Во-первых, необходимостью более точно обозначить фрагмент визуализируемого морфологического субстрата. Например, если мы "рассматриваем" на экране пирамиду нормальной почки не в виде привычного до сих пор гипоэхогенного включения весьма типичного по форме, а как совокупность дифференцируемых между собой тубулярных элементов, очевидно термин "микроанатомическая картина" (или "рисунок микроанатомических структур") будет больше подходить для описания графической текстуры, отражающей конкретную морфологическую субстанцию (рис. 1).
В поддержку предлагаемого термина уместно заметить, что его уже удалось встретить в отечественном пособии по эхографии: "микроанатомия предстательной железы" [6]. И хотя слово "микроанатомия" было представлено в контексте исключительно для предварительного ознакомления с нормальной морфологией органа, тем не менее именно этим термином изначально предопределялся автором возможный уровень оценки структур с помощью УЗИ.
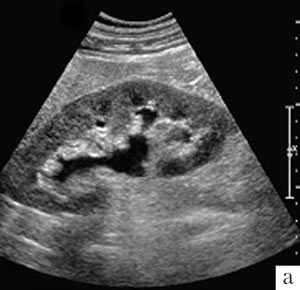
а) Низкочастотный режим - 3,5 МГц. Низкое разрешение. Изображение продольного скана почки с изображением пирамид в виде гипоэхогенных включений в паренхиме.
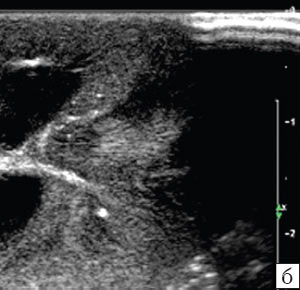
б) Высокочастотный режим - 17,0 МГц. Высокое разрешение. Изображение участка кортико-медуллярного фрагмента с дифференцируемыми тубуло-интерстициальными и форникальными элементами.
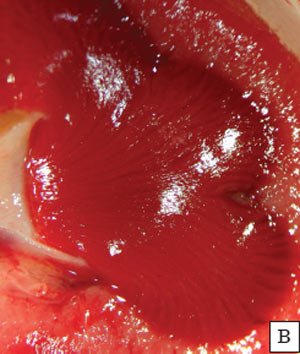
в) Препарат почечной пирамиды. Бинокулярная лупа ув. 4х. Фрагмент препарата нормальной почки ребенка 10 лет (аутопсия): тубулярные элементы пирамиды.
Во-вторых, понятие "эхографическая оценка на микроанатомическом уровне" определена возможностью визуализации сосудисто-тканевых фрагментов с морфологическими элементами, часто не обозначенными в широко распространенных руководствах и атласах по макроскопической анатомии. Например, описание строения придатка яичка с упоминанием о так называемых выносящих канальцах (дольках придатка) диаметром до 0,1-0,3 мм представлено лишь в пособиях по гистологии и микроанатомии [4, 7]. При этом термин "дольки придатка яичка" (рис. 2) включен в Международную анатомическую номенклатуру [8].
Однако в общей массе ни врачи-специалисты УЗИ, ни тем более клиницисты к этому этапу сегодня еще не готовы. Очевидно, мало кто готов к оценкам структур и их изменений с помощью эхографии на микроанатомическoм уровне.
Первая и основная причина - отсутствие в настоящее время равномерного и повсеместного распространения высокоразрешающих эхографических технологий. Очевидно, прогрессивное развитие каких-либо прикладных теорий по оценке структур на соответствующем уровне при таких условиях априори невозможно. Сегодня же практически повсеместно специалисты по ультразвуковой диагностике, с технической точки зрения, могут продолжать пытаться (подчеркнем, "пытаться " в самом хорошем смысле) судить о "местонахождении и причинах болезней посредством рассечения" только в лучших традициях Джованни Морганьи. При этом главенствующее значение, конечно, как и до середины XIX века, для морфологов имеет оценка положения, размеров, общего вида, консистенции органов и дополнительных включений, а также признаков нарушения целостности органных структур.
Вторая причина - неготовность к подобному уровню оценки структур лечащих врачей. Даже если у нас - специалистов по УЗИ - будет иметься на то техническая возможность и мы настойчиво и аргументировано попытаемся внедрять понятие "микроанатомическая оценка структур", нас поначалу, почти наверняка, не поймут клиницисты, ибо большинство лечащих врачей, подчеркнем - большинство, привыкли весьма утрированно оценивать данные лучевых интраскопических исследований. Под словом "утрированно" подразумевается оценка клиницистами структур и патологических изменений на "макроскопическом" уровне. Пожалуйста, весьма распространенный на практике пример. Сегодня почти все урологи под понятием "острая обструкция мочевыводящих путей" (или под нередко применяемым словосочетанием "блок почки") подразумевают обструкцию на "органном" уровне в виде признаков дилатации мочеточника и фрагментов коллекторной системы почки. Соответственно определяется и уровень поиска причин обструкции - исключительно "макроскопический" (независимо от генеза: мочекаменная болезнь, травма, острое воспаление и т. д.). При этом клиницист, как правило, требует от врача УЗИ изучить и почку, и мочеточник не более как с двумя целями: оценить наличие и степень дилатации мочевыводящих путей, а также попытаться выявить (или исключить) абтурирующий агент.
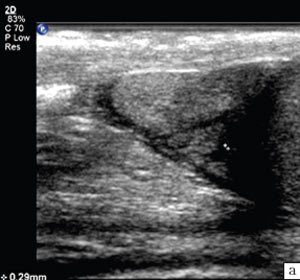
а) Изображение выносящих канальцев придатка яичка мальчика 11 лет.
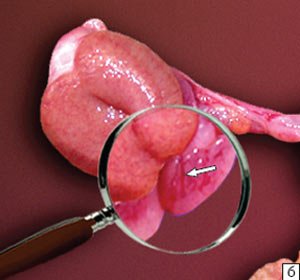
б) Препарат придатка яичка с выносящими канальцами ребенка 10 лет, ув. 2х (аутопсия).
При попытках специалистом по эхографии предоставить аргументированную оценку на микроанатомическом уровне, например, реально обосновать признаки внутрипочечной (интраренальной) обструкции за счет перитубулярного отека, к сожалению, нередко возникает достаточно неадекватная реакция со стороны лечащего врача. Если не предвзято подходить к подобным ситуациям, то мало в чем можно упрекнуть клинициста. Казус в том, что теоретические обоснования оценки тех же изменений внутрипочечных структур на микроанатомическом уровне при ренальной обструкции давно существуют и являются общепризнанной академической классикой. Однако технически ни с помощью стандартных рентгенологических методик, ни с помощью эхографии признаки упомянутых академических проявлений интраренальной обструкции мочевых путей (например, вариантов интраренального рефлюкса) до теперешнего времени на практике предоставить было чаще всего невозможно. Очевидно, основная масса лечащих врачей второй половины ХХ века "выросла" на требованиях и к себе, и к коллегам в клинической оценке структур на макроскопическом уровне, независимо от имеющихся теоретических основ микроанатомического обоснования патологических процессов. Визуализирующие технологии соответствующего уровня делали и делают их уверенными в себе. Именно поэтому большинство клиницистов сегодня еще не желает иметь кругозор патологоанатома, ибо это поначалу явно лишит их чувства уверенности в себе как профессионала, потребует значительных усилий на самоусовершенствование, а также осознание морфологии и патологических процессов на другом, не затрагиваемом ранее практикой, уровне. Очевидно, сегодня клиницистам пока "комфортнее" продолжать проводить оценку структур на макроскопическом уровне развития клинической морфологии при поддержке повсеместно распространенных визуализирующих технологий соответствующих возможностей.
Наконец, третья причина неготовности оценивать с помощью эхографии структуры и их изменения на микроанатомическом уровне. Эта причина в нас - специалистах по клинической ультразвуковой диагностике. Сразу стоит уточнить: причина, конечно, не одна, безусловно, это совокупность причин. Помимо упомянутых отсутствия соответствующих технологий и изначально сложившейся привычки работать на "макроскопическом" уровне, подобно большинству клиницистов, в нас присутствуют другие, не менее важные факторы неготовности восприятия изображений на уровне микроанатомии. Уделять этим факторам внимания по большому счету нет особого смысла, ибо главенствующее значение имеет лишь один из них - явное отсутствие точек опоры в эхографической оценке тканевых текстур и их трансформаций, т. е. в объективизации данных, определяемых общим понятием эхогенность (или изменение эхогенности).
Уточню ситуацию с помощью уже помогавшего нам примера. Сегодня на широко распространенных сканерах текстура пирамиды почки в норме представлена, как правило, гипоэхогенным участком пирамидной формы (так и ассоциируем эти текстурные участки - почечные пирамидки). При определенных условиях на сканере сверхвысокого разрешения текстуры пирамид представлены конгломератом трубчатых элементов повышенной эхогенности и гипоэхогенными перетубулярными промежутками. При всем желании подобную текстуру в целом нельзя назвать просто гипоэхогенным участком. Очевидной становится зависимость оценки эхогенности конкретного морфологического субстрата от возможностей визуализирующей техники по показателям разрешающей способности (см. рис.1).
При этом изменения параметров настройки самого прибора (контрастность, яркость, интенсивность отраженного сигнала и т. д.) не влияют на наличие и специфичность рисунка рассматриваемых трубчатых структур. В определенной степени он, конечно, изменится относительно общей тональности, но будет присутствовать. Принципиально: образ визуализируемого объекта с присутствием специфических текстурных элементов будет сохранен и ассоциирован с конкретной микроанатомической субстанцией. В рассмотренном примере - это образ конгломерата трубочек и перитубулярный мезенхимально-сосудистый компонент. Все подобно тому, как на "слабых" аппаратах всегда будет сохраняться образ органа в целом, вне зависимости изменений "вручную" на экране, например, степени отражения сигнала от его паренхимы. Только оцениваемый образ - уже не орган, а тканевой фрагмент, или, как мы стали его называть - микроанатомический фрагмент органа. При этом признаки конкретного морфологического субстрата, определяющие его графический образ, априори не могут определяться изменяемыми параметрами настройки технических средств. Они присутствуют всегда и определены исключительно свойствами изучаемого субстрата, а также изменяются в первую очередь с изменением акустических свойств самого субстрата.
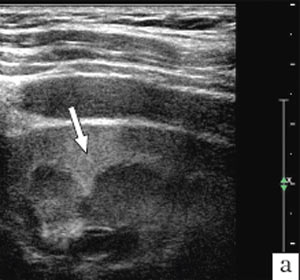
а) Пациентка 11 лет, острый пиелонефрит, признаки очага воспалительной инфильтрации.
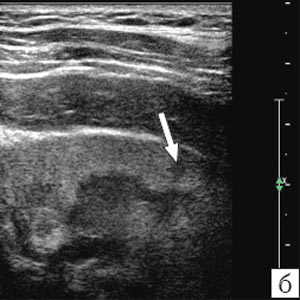
б) Эта же пациентка, признаки экссудации в кортикальном отделе паренхимы почки.
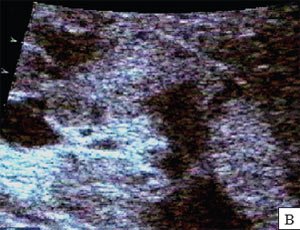
в) Пациент 5 лет, острый пиелонефрит, признаки интраренального тубуло интерстициального рефлюкса в виде формирующейся апостемы.
Постоянно на микроанатомическом уровне будут проявляться фазы патоморфогенеза общепатологических процессов. Например, при остром паренхиматозном воспалении каждая из фаз процесса будет иметь свою микроанатомическую картину. Фаза инфильтрации всегда будет характеризоваться повышением эхогенности вследствие периваскулярной лейкоцитарной инфильтрации. Для фазы воспалительной экссудации будет характерно появление в паренхиме гипоэхогенных фокусов различных размеров и формы за счет имбибиции периваскулярных пространств воспалительным экссудатом. Для деструкции характерны анэхогенные включения, обусловленные лизисом тканевых компонентов. Перечисленные проявления будут иметь место всегда. Возможности же высокоразрешающих технологий позволят лишь подчеркнуть их специфику в зависимости от конкретного изучаемого паренхиматозного органа, а также особенностей проявления и распространения воспалительного процесса в конкретном органе (рис. 3).
Таким образом:
- современные ультразвуковые технологии позволяют визуализировать внутренние структуры на параметрах разрешения, позволяющих употреблять термин "микроанатомический уровень";
- перманентный кризис в абдоминальной эхографии определен отсутствием единых концепций оценки структур, учитывающих, в том числе характеристику эволюционирующих патологических и компенсаторно-регенеративных процессов на микроанатомическом уровне;
- потенциал выхода из обозначенного кризиса включает необходимость конструктивной ревизии имеющихся в эхографии положений оценки структур, учитывающих сегодня в большинстве случаев лишь макроанатомические параметры;
- оценка данных УЗИ с учетом микроанатомических проявлений эволюции структур в онтогенезе и при адаптационно-регенеративных процессах позволит более широко использовать метод в диагностике на доклиническом этапе развития патологии.
Литература
- Быковский В.А. К принципам оценки составляющих эхографическое изображение // Абдоминальная эхография: проблемы - сложности - ошибки. М.: Реал Тайм. 2006. С.152-194.
- Саркисов Д.С. Очерки по структурным основам гомеостаза. М.: Медицина. 1977. 348 с.
- Саркисов Д.С. Очерки истории общей патологии. Изд. 2-е. М.: Медицина. 1993. 506 с.
- Krstic R.V. Human Microscopic Anatomy. Berlin: Springer-Verlag. 1994. P. 615.
- Заварзин А.А. Курс гистологии и микроскопической анатомии. Ленинградское отделение МЕДГИЗ. 1938. 662 с.
- Громов А.И. Ультразвуковое исследование предстательной железы. М.: Биоинформсервис 1999. 8 с.
- Крстич Р.В. Иллюстрированная энциклопедия по гистологии человека. С.-Пб: Сотис. 2001. 531 с.
- Международная анатомическая терминология (с официальным списком русских эквивалентов). Под ред. Л.Л. Колесникова. М.: Медицина. 2003. С. 87.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Публикации по теме
- Случай мультилокулярной кистозной нефромы почки - Курзанцева О.М.
- Ультразвуковая и рентгеновская диагностика травматического и ятрогенного повреждений стенок кист почек - Буйлов В.М.
- Микроанатомическая оценка структур в клинической эхографии - возможности и перспективы - Быковский В.А.
- Трехмерная ультразвуковая ангиография с диуретической нагрузкой в диагностике уретеро-вазальных конфликтов - Перепадя Е.В.
- Скрининговое ультразвуковое исследование почек у больных с повышенным артериальным давлением - Соломка О.В.


