Интраоперационное трансректальное УЗИ при трансуретральной электрорезекции гиперплазии простаты
Москва, Россия.
Рубрика: Эхография в урологии

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Согласно эпидемиологическим исследованиям, гиперплазия предстательной железы является весьма распространенным заболеванием у мужчин среднего, пожилого и старческого возраста. По данным морфологических исследований это заболевание подтверждено у 50% мужского населения в возрасте 60 лет, причем, к 70-ти летнему возрасту процент заболеваемости увеличивается до 70%, а к 90 годам - до 90% [3,8,13]. В 1990 году в США по поводу тех или иных жалоб, связанных с гиперплазией предстательной железы, к врачам-урологам впервые обратилось около 1,2 млн. пациентов [14]. Число лиц, страдающих этим заболеванием в течение определённого времени, составляет многие миллионы. В странах бывшего СССР смертность от гиперплазии предстательной железы в 1986-1989 гг. составила 3,88 на 100000, в Италии 1,41 на 100000, в США 0,26 на 100000 человек [9]. Проблема гиперплазии предстательной железы встает еще более остро в связи с увеличением числа мужчин пожилого и старческого возраста в структуре населения планеты. Это связано, в частности, с увеличением продолжительности жизни людей [10].
Используемые сегодня различные виды хирургического вмешательства обеспечивают большую вероятность уменьшения симптоматики и уродинамических нарушений, связанных с гиперплазией простаты. При этом для трансуретральной резекции простаты характерна высокая эффективность, при меньшем, по сравнению с открытыми вмешательствами, количестве и тяжести осложнений [7]. По данным международных совещаний по лечению гиперплазии простаты, состоявшихся в 1991-2003 гг., Американской и Европейской урологических ассоциаций с 1992 по 2003 год трансуретральная резекция простаты считается "золотым стандартом" лечения гиперплазии предстательной железы [12] и выполняется в 63,7-98,3% среди всех инвазивных методов лечения гиперплазии простаты. Однако, многолетний опыт этих операций показал, что возникающие, как интраоперационные, так и послеоперационные осложнения, в том числе и отдаленные неудовлетворительные результаты [1,2,4,5,6,11], чаще всего обусловлены недостаточной ориентацией хирурга относительно хирургической капсулы предстательной железы.
С целью улучшения визуализации простаты и результатов трансуретральной резекции при ее гиперплазии мы использовали интраоперационное ТРУЗИ. При исследовании определяли топографо-анатомические особенности простаты и внутриорганное взаимоотношение аденоматозных узлов и хирургической капсулы предстательной железы.
Материалы и методы
Для трансректального исследования предстательной железы использовали конвексный ректальный датчик (частотой 7,5 МГц) ультразвукового сканера "Hawk" 2120. Исследование выполняли в 3 этапа и в двух плоскостях - поперечной и сагитальной. Первый этап проводился в сагитальной плоскости одновременно с уретроцистоскопией и позволял визуализировать дистальный конец резектоскопа. При этом оперирующий хирург устанавливал дистальный конец резектоскопа в зоне семенного бугорка (рис. 1 а,б) и медленно смещал инструмент в мочевой пузырь, что позволяло измерять в реальном времени расстояние от петли до капсулы простаты на 5-4-х и 11-13-и часах условного циферблата на всем протяжении простатического отдела уретры (рис. 1 в-е). Исследование в поперечной плоскости было малоинформативным из-за плотного прилегания к инструменту гиперплазированной ткани простаты (боковые доли) (рис. 1ж).
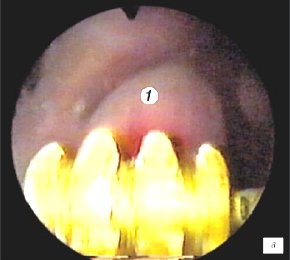
а) Эндоскопическая картина простатического отдела уретры.
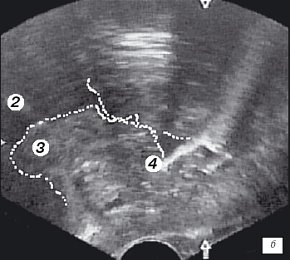
б) Эхограмма простаты (сагитальная проекция). Дистальный конец резектоскопа находится в зоне семенного бугорка.
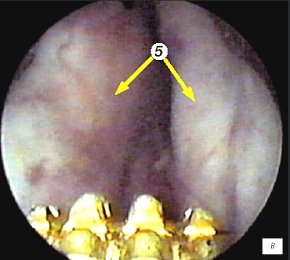
в) Эндоскопическая картина простатического отдела уретры - боковые доли гиперплазии простаты.
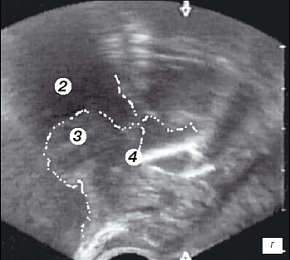
г) Эхограмма простаты (сагитальная проекция). Дистальный конец резектоскопа находится на 1 см выше семенного бугорка.
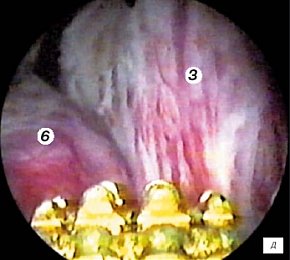
д) Эндоскопическая картина простатического отдела уретры - средняя доля гиперплазии простаты.
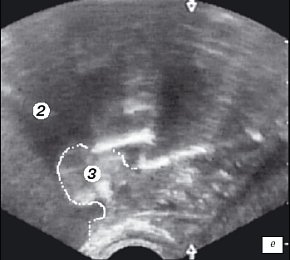
е) Эхограмма простаты (сагитальная проекция). Дистальный конец резектоскопа находится на средней доле гиперплазии простаты.
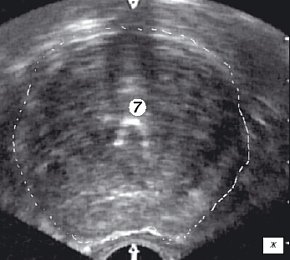
ж) Эхограмма простаты (поперечная проекция). Дистальный конец резектоскопа находится на 1 см выше семенного бугорка.
Второй этап выполняли через 30-40 минут после начала операции и после удаления средней (при ее наличии) и части боковых долей простаты. Уже частично формировалось ложе удаленной гиперплазии простаты. Кроме того, в области пузырно-простатического сегмента при оптико-визуальном контроле определялась капсула простаты, что требовало необходимость УЗ контроля в других ее зонах. При исследовании в поперечной и сагитальной плоскостях оценивалась симметричность удаленной ткани боковых долей простаты, объем оставшейся гиперплазии, а также визуализировались вдающиеся в просвет уретры узлы неудаленной аденоматозной ткани. Тщательно измеряли расстояние от петли до капсулы простаты в наиболее опасных для ее перфорации местах (рис. 2 а,б).
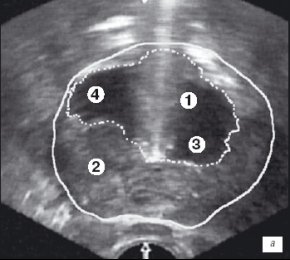
а) Эхограмма простаты (поперечная проекция).
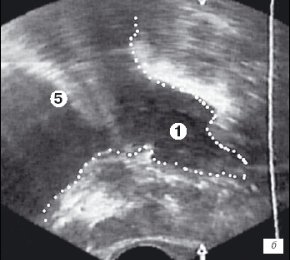
б) Эхограмма простаты (сагиттальная проекция).
Третий этап исследования выполняли по завершению операции для оценки радикальности ее выполнения (рис. 3 а,б). Это позволяло оценить объем удаленной ткани, сформированность ложа, а в случае необходимости, провести удаление или вапоризацию оставшихся участков гиперплазии.
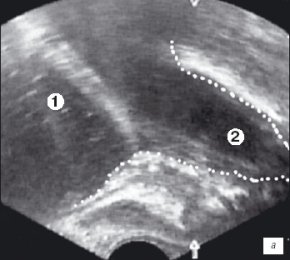
а) Эхограмма простаты (сагиттальная проекция).
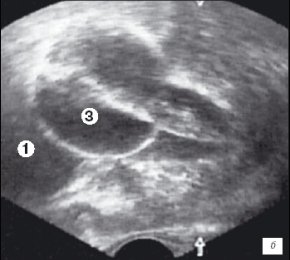
б) Эхограмма простаты (сагитальная проекция). Установка уретрального катетера.
Всего интраоперационное ТРУЗИ выполнено 26 пациентам (n=26) с гиперплазией предстательной железы II стадии в возрасте от 52 до 79 лет (I группа). Объем предстательной железы в этой группе варьировал от 36,5 до 141,2 см³. Контрольную группу составили 26 пациентов (II группа), объемом простаты от 34,9 до 130,1 см³., которым не выполнялось интраоперационное ТРУЗИ. При этом средняя объемная скорость мочеиспускания во всех группах была примерно одинаковой и составила 9,8±0,8 мл/с. Также не существенно отличалось между группами количество остаточной мочи, которое составило в среднем 166±4,5 мл. Средняя длительность операции в I группе составила 75±1,8 минуты соответственно, а во II - 86±2,1мин. Средняя длительность одного сеанса ТРУЗИ составила 3,7±0,9 мин. Следует отметить, что 6 пациентам с объемом простаты до 60 см³. было достаточным выполнение 2-х ТРУЗИ - в начале и в конце операции, а 4 пациентам с объемом простаты более 60 см³ понадобилось дополнительное ТРУЗИ.
Результаты
Послеоперационные осложнения, потребовавшие повторных эндоскопических вмешательств, в I группе возникли у 2-х больных, во II - у 5-и. Средняя объемная скорость мочеиспускания через месяц после трансуретральной резекции простаты в I группе составила 21,4±1,4 мл/с, во II - 18,8±1,1мл/с. При контрольном ТРУЗИ через 5 суток после трансуретральной резекции простаты средний объем простаты в I группе составил 39,8±2,1 см³, во II - 47,7±3,2 см³.
Выводы
Информация, получаемая при интраоперационном ТРУЗИ, помогает хирургу лучше ориентироваться в ходе операции и свести к минимуму опасность перфорации капсулы простаты. Данное исследование позволяет избежать ложных рецидивов, минимизирует интраоперационные осложнения и увеличивает радикальность трансуретральной электрорезекции гиперплазии простаты, что значительно улучшает отдаленные результаты оперативного лечения.
Литература
- Лопаткин Н.А., Мартов А.Г., Козлов С.А.: Всероссийское научное общество урологов. Пленум: материалы. - Курск, 1993 г. - С. 112 - 113.
- Лопаткин Н.А., Симонов В.Я., Козлов С.А.: Урол. и нефрол., 1984 г. N 1. - С. 1 - 7.
- Лопаткин Н.А.: Доброкачественная гиперплазия предстательной железы. Под ред. Лопаткина. Н. А. - Москва, 1997 г. - С. 5.
- Лопаткин Н.А.: Осложнения ТУР предстательной железы и аденомэктомии. Доброкачественная гиперплазия предстательной железы. Под ред. Лопаткина Н. А.- Москва, 1997 г. - С. 163 - 167.
- Мартов А.Г., Лопаткин Н.А. Практическое руководство по трансуретральной эндоскопической электрохирургии доброкачественной гиперплазии предстательной железы. - Москва. - Триада Х. - 1997 г. С. 95 - 103.
- Мартов А.Г.: Доброкачественная гиперплазия предстательной железы. Под ред. Лопаткина Н.А. - Москва, 1997 г. - С. 151 - 161.
- Митьков В.В. Клиническое руководство по ультразвуковой диагностике. - Т. 1. - М.: Видар, 1996.
- Насникова И.Ю., Митьков В.В., Хитрова А.Н., Герасимова Н.П. // Ультразвуковая диагностика. - 1987. - N 3. - С. 43.
- Ткачук В.Н., Аль-Шукри С.Х., Лукьянов А.Э., Темкин Д.Б. Факторы влияющие на развитие гнойно-воспалительных осложнений после ТУР у больных ДГПЖ. Международный медицинский Конгресс "Медицина высоких технологий в XXI веке". Челябинск 1999 г. Сборник тезизов докладов. С. 179 - 180.
- Веrry S.J., Coffey D.S., Walsh P.S., et. al., .The development of human benign hyperplasia: with age. J. Urol., 1984. -Vol. 132. - P. 474.
- Boyle P., Napalkov P. Epidemiology of Benign Prostatic Hyperplasia: Current Perspectives, European Urology, N.29 (suppl. 1), 1996, pp. 7-11.
- Boyle P., Maissonneuve P., Napalkov P. Prostate diseases beyond the year 2000: present and future burden of prostate diseases, In Textbook of Benign Prostatic Hyperplasia, Oxford, 1996, pp. 543-544.
- Mebust W.K., Holtgrewe H.L., Cockett A.T. et al.: J. Urol. -1989.-Vol. 141.-P. 243 - 247.
- Woodwell D. Office visits to urologists: United States, 1989-1990, National Ambulatory Medical Care Survey. In "Advance Data from vital and health statistics", No.234, Hyattsville: National Center for Health Statistics, 1992, pp. 1-12.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Публикации по теме
- Фармакоэходопплерография препростатического венозного сплетения в диагностике венокорпоральной эректильной дисфункции - Аляев Ю.Г.
- Сравнительная оценка лучевых методов в диагностике жидкостных образований почек - Аляев Ю.Г.
- Интраоперационное трансректальное УЗИ при трансуретральной электрорезекции гиперплазии простаты - Аляев Ю.Г.
- Трансуретральная пункционная биопсия опухоли мочевого пузыря - Аляев Ю.Г.
- Диагностика и лечение жидкостных образований почек - Аляев Ю.Г.


