Фетальные аритмии: антенальная ультразвуковая дифференциальная диагностика, прогнозирование постнатальных результатов и перинатальная практика
Рубрика: Эхография в акушерстве
УЗИ сканер Samsung W10
Аппарат экспертного/премиум класса поможет расширить возможности диагностики, благодаря интуитивно понятным алгоритмам обработки и точным инструментам анализа.
Введение
При обнаружении любых фетальных аномалий неотъемлемой составляющей работы специалиста пренатальной эхографии и медицины плода является прогнозирование исхода беременности. Сложность адекватного перинатального и постнатального прогноза при нарушениях сердечного ритма плода заключается в их неопределенном клиническом значении, так как эти нарушения могут быть как благоприятными, транзиторными, так и крайне опасными, связанными с риском тяжелых осложнений на всех этапах перинатального периода. Не более 15% фетальных аритмий являются опасными для жизни плода [1].
Аритмии плода могут проявляться в виде нерегулярных, неритмичных сокращений либо в изменении их частоты - замедлении или учащении, могут быть постоянными либо транзиторными. Постоянное изменение базальной частоты сердечных сокращений (ЧСС) в виде тахикардии >180 уд/мин или брадикардии <100 уд/мин ассоциировано с состояниями, потенциально опасными для жизни плода [2]. Нерегулярный ритм сокращений сердца чаще связан с преждевременными импульсами, а также нарушением их проведения, т.е. с патологией водителей ритма и проводящих путей.
Среди причин этих нарушений - ишемия, воспалительные процессы, электролитный дисбаланс, структурные пороки, в том числе наследуемые генетически [3]. К факторам риска развития аритмий плода относят: острую вирусную инфекцию, приводящую к развитию миокардита [4], патологические иммунные реакции с воздействием материнских антител на клетки проводящей системы сердца плода.
Ультразвуковое сканирование является ведущим, а часто практически единственным способом диагностики нарушений сердечного ритма плода. Для дифференциальной диагностики вариантов фетальных аритмий используются различные режимы:
- М-режим (курсор пересекает одновременно предсердие и желудочек, т.е. проходит через центр сердца плода) позволяет одновременно регистрировать ритмы сокращений предсердий и желудочков и оценивать атриовентрикулярное (AV) проведение (рис. 1);
- импульсно-волновая допплерография (ИВД), при которой широкий контрольный объем устанавливается, перекрывая одновременно артерию и вену (допплерограмма при этом имеет 2 спектра - артериальный и венозный - по разные стороны базовой линии).
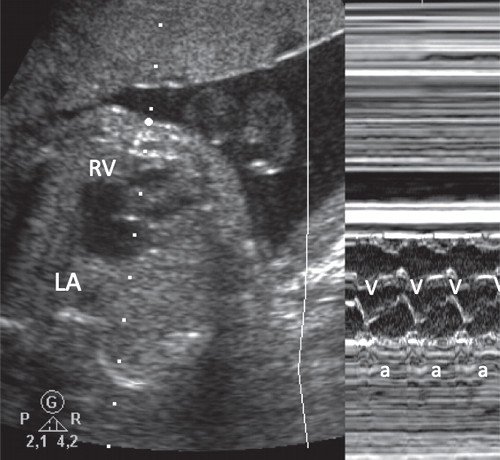
Рис. 1. Для определения соответствия сокращений предсердий и желудочков курсор М-режима пересекает центр сердца и проходит одновременно через правый желудочек (RV) и левое предсердие (LA).
Одновременная импульсно-волновая допплерография артерии и вены может проводиться:
- интракардиально - с одновременной регистрацией притока к митральному клапану и оттока в аорту (рис. 2);
- одновременно на близко расположенных артериях и венах плода, например, на почечных, легочных сосудах, дуге аорты и брахиоцефальной вене, восходящей аорте и верхней полой вене (ВПВ) (рис. 3);
- на сосудах пуповины.
Это также позволяет оценивать взаимоотношения между предсердными и желудочковыми сокращениями. При этом могут измеряться интервалы предсердно-желудочкового (атриовентрикулярного, AV) и желудочко-предсердного (вентрикуло-атриального, VA) времени (см. рис. 3) механические аналоги электрокардиографических PR и RP-интервалов [5].
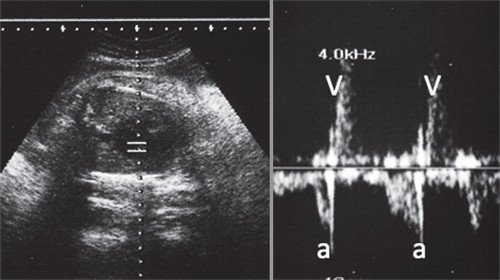
Рис. 2. Одновременная интракардиальная допплерография митрального притока (а - часть спектра ниже базовой линии) и оттока в аорту (v - спектр выше базовой линии).
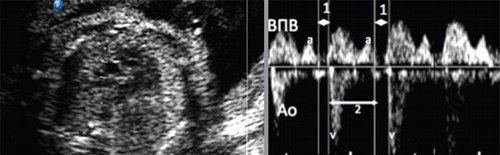
Рис. 3. Одновременная артериально-венозная импульсно-волновая допплерография восходящей аорты (Ао) и верхней полой вены (ВПВ) при нормальном АV проведении:
1 - механические интервалы AV времени - промежуток от начала предсердной систолы (а), соответствующей реверсной волне ВПВ, до начала желудочковой систолы (v);
2 - механический интервал VA времени - промежуток между началом желудочковой систолы и началом предсердной систолы.
При нормальном синусовом ритме 2 > 1, т.е. интервал VA длиннее интервала AV.
Нерегулярный ритм ЧСС
Периодические неритмичные сокращения (экстрасистолы) генерируются эктопическими клетками проводящей системы. Эпизодические или периодические преждевременные сокращения предсердий (предсердные экстрасистолы, ПЭ) встречаются чаще, их возникновение связано обычно с "незрелостью" проводящих путей сердца плода. Аускультативно и эхографически ПЭ проявляются в виде внеочередных и "выпадающих" сокращений, соответствующих эктопическому импульсу и компенсаторной паузе (рис. 4, а). В абсолютном большинстве случаев ПЭ изолированы, имеют транзиторный и доброкачественный характер и не требуют лечения на пренатальном и постнатальном этапах [6].
Преждевременные сокращения желудочков (желудочковые экстрасистолы, ЖЭ) встречаются реже (рис. 4, б) и могут ассоциироваться с патологией миокарда внутрисердечных перегородок, в котором залегают проводящие пути, к примеру, с дефектами перегородок [2, 4].
Рекомендуемая тактика при экстрасистолии - еженедельный эхографический или кардиотомографический мониторинг ЧСС в связи с существующим потенциальным низким риском (не чаще 1% случаев) развития более тяжелых форм аритмий плода [2].
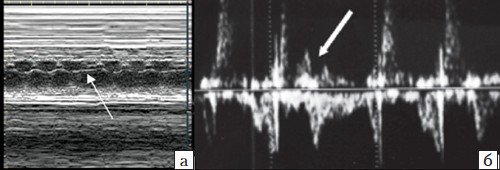
а) Предсердная экстрасистола, за которой следует компенсаторная пауза (стрелка), во всех случаях эти нарушения сердечного ритма имели транзиторный и доброкачественный характер;
б) Желудочковая экстрасистола (стрелка) в нашем наблюдении ассоциировалась с дефектами миокарда межжелудочковой перегородки и необходимостью коррекции после рождения.
Брадикардия плода
Короткие эпизоды брадикардии (длительностью до 1-2 минут) либо асистолии (длительностью до нескольких секунд) нередко возникают в I-II триместрах беременности (рис. 5), являются транзиторными, доброкачественными и не требуют мониторинга либо терапии.
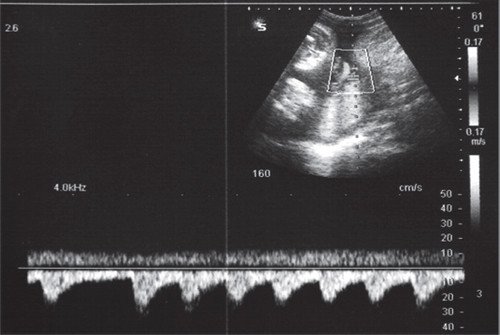
Рис. 5. Эпизоды транзиторной доброкачественной брадикардии - асистолии плода на этапе II триместра беременности встречались нередко, не сопровождались структурной патологией сердца и не осложняли течение беременности.
Синусовая брадикардия - стойкое замедление ЧСС ниже 100 уд/мин с регистрацией AV проводимости 1:1 (т.е. предсердия и желудочки имеют одинаковую частоту сокращений). Стойкая синусовая брадикардия плода (рис. 6) почти всегда связана с серьезными нарушениями его состояния (дистрессом, т.е. гипоксией, метаболическим ацидозом), а также с серьезной врожденной патологией водителя ритма.
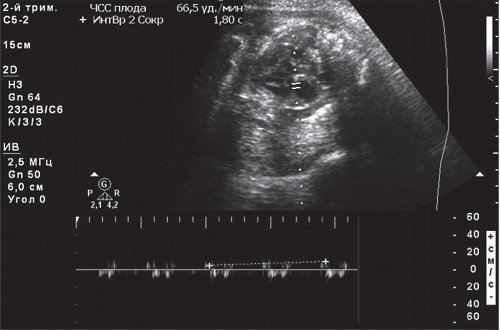
Рис. 6. Синусовая брадикардия - стойкая регистрация базальной ЧСС плода 65 уд/мин при декомпенсированной плацентарной дисфункции, тяжелом антенатальном дистрессе (метаболическом ацидозе) плода на 32-й неделе беременности.
При предсердной бигеминии или тригеминии (преждевременных блокированных сокращениях предсердий) частота сокращений желудочков плода может снижаться до 60-100 уд/мин. При этом блокируется проведение к желудочкам каждого второго (бигеминия) либо каждого третьего (тригеминия) предсердного импульса (рис. 7-9).
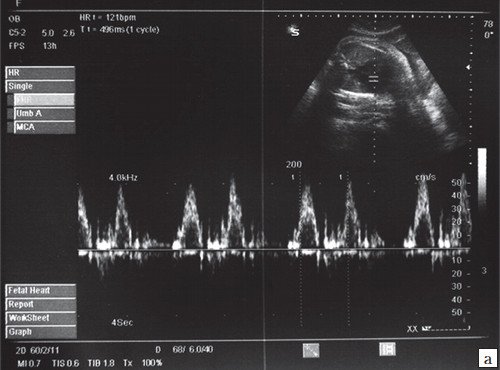
а) При предсердной бигеминии в 28 недель беременности.
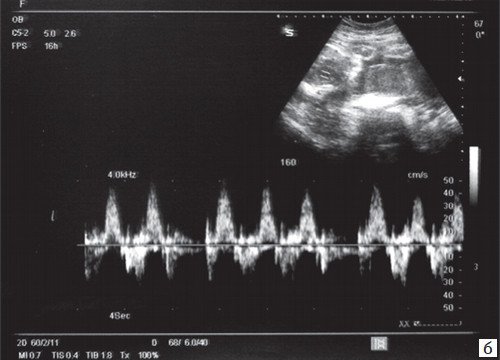
б) При предсердной тригеминии в 35 недель c блокированным проведением предсердно-желудочковых импульсов.
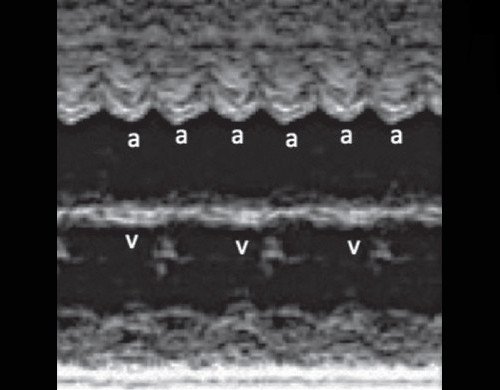
Регистрация частоты сокращения предсердий (а) и желудочков (v) в М-режиме.
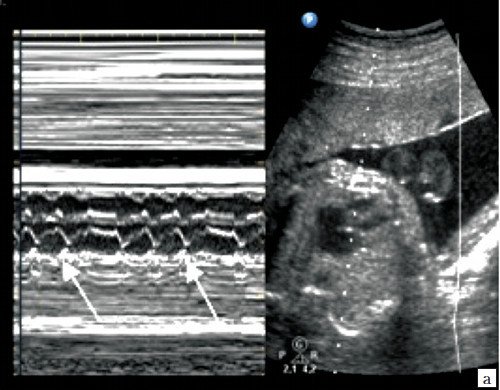
а) Каждое третье сокращение предсердия (стрелка) возникает преждевременно и блокируется, не проводится к желудочку.
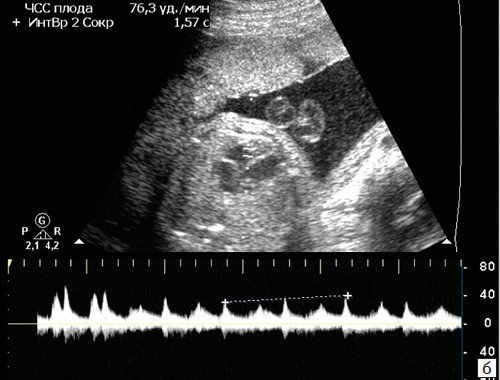
б) В результате формируется желудочковая брадисистолия 76 уд/мин.
Атриовентрикулярная блокада формируется в половине случаев на фоне врожденного порока сердца (ВПС) [4], в частности может ассоциироваться с изомеризмом, cиндромом удлиненного интервала QТ, а также с проникновением к плоду материнских антител при аутоиммунных соединительнотканных заболеваниях. Различают три степени AV блокады, однако при антенатальном ультразвуковом сканировании возможно выявление II и III степени патологии [7]. При II степени AV блокады (рис. 10) от предсердий к желудочкам проводятся не все импульсы, а только их часть (каждый второй - при проведении 2:1 и каждый третий импульс - при проведении 3:1).
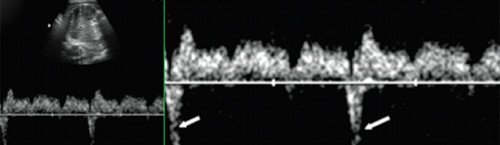
Усиление реверсного компонента в нижней полой вене (стрелки) как признак объемной перегрузки правых отделов сердца (снимок предоставлен проф. И.С. Лукьяновой).
При III степени AV блокады (полной AV блокаде) предсердно-желудочковое проведение полностью прервано, сокращения предсердий и желудочков абсолютно разобщены (рис. 11).
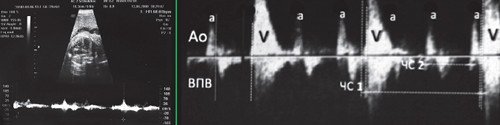
Сокращения предсердий (а) и желудочков (v) разобщены. Частота сокращений желудочков (ЧС1) в несколько раз меньше частоты сокращения предсердий (ЧС2). Интервалы AV времени (промежутки между вертикальными пунктирными линиями) различаются.
Предсердная бигеминия (тригеминия) с блокированными преждевременными кращениями может быть спутана с тяжелой AV блокадой, так как оба состояния характеризуются более высокой частотой сокращений предсердий, чем желудочков. Однако дифференциальный диагноз этих состояний важен в связи с разным прогнозом: желудочковая брадисистолия при предсердной бигеминии не требует лечения и может спонтанно восстанавливаться, тогда как полная AV блокада является необратимым состоянием, может сопровождаться водянкой плода и неблагоприятным перинатальным результатом.
Одновременная импульсно-волновой допплерографии восходящей аорты и ВПВ (см. рис. 3) позволяет оценить механический интервал AV времени - промежуток между началом реверсной волны в ВПВ (соответствует систоле предсердий) и началом систолической волны в аорте (соответствует началу желудочковой систолы). При AV блокаде временные интервалы между последовательными предсердными импульсами выраженно варьируют, беспорядочны (см. рис. 11).
В сравнении с опытом лечения фетальных тахикардий, сведения об эффективности пренатального лечения АV блокады ограничены имеющимися единичными сообщениями [8].
Тахикардия плода
Хорошо известно, что в процессе дифференциальной диагностики фетальных тахиаритмий периодические недлительные эпизоды возрастания ЧСС до 180-200 уд/мин рассматриваются как акцелерации физиологические нейрорегуляторные реакции в рамках вариабельности сердечного ритма, за счет формирующегося к III триместру миокардиального рефлекса плода. Тахикардия - стойкое возрастание ЧСС более 180 или 190 уд/мин [2, 7]. Это нарушение ритма может быть бессимптомным либо приводить к застойной сердечной недостаточности, дилатации сердечных камер, водянке плода и его внутриутробной гибели.
Основные этиопатогенетические формы стойких тахикардий: синусовая, суправентрикулярная (наджелудочковая) и вентрикулярная (желудочковая). Стойкая синусовая тахикардия - частота сокращения предсердий 180-200 уд/мин (рис. 12) с АV проведением 1:1. В клинической практике такой аритмией могут сопровождаться дистресс, анемия плода, инфекционные процессы, материнская гипертермия, тиреотоксикоз, прием беременной - β-миметиков или тиреоидных препаратов [8].
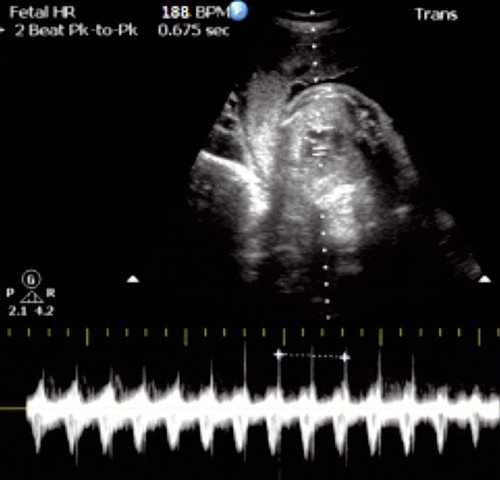
Базальная ЧСС 188 уд/мин на фоне анемической формы гемолитической болезни плода.
Суправентрикулярная тахикардия (СВТ) - ЧСС от 200 до 300 уд/мин (рис. 13, 14). При нормальном АV проведении такой вид нарушения ритма может иметь благоприятный постнатальный прогноз. В то же время фетальная СВТ может вызываться дополнительными, эктопическими проводящими путями (при синдроме Вольффа - Паркинсона - Уайта, WPW).
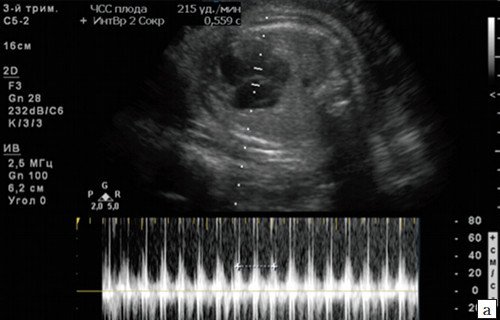
а) Беременность 35 недель, ЧСС 215 уд/мин с АV проведением 1:1. Индуцированные роды в 38 недель, сразу после пересечения пуповины восстановился нормальный сердечный ритм плода.
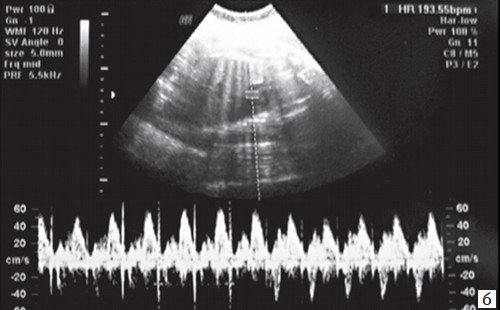
б) Беременность 35 недель, базальная ЧСС 194-205 уд/мин с АV проведением 1:1. Высокая ЧСС сохранялась и после рождения (постнатальный WPW-синдром), в связи с чем новорожденному назначались антиаритмические препараты.

а) ЧCC 220-260 уд/мин, АV проведение 1:1, без структурных аномалий сердца.
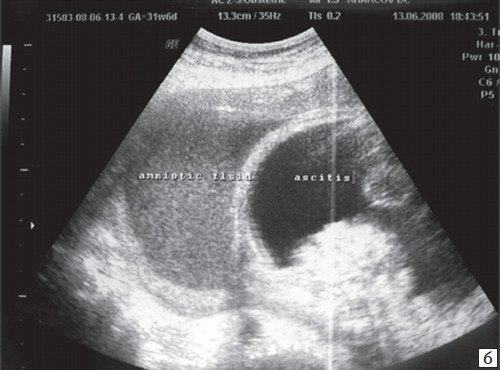
б) Универсальный отек плода развился после трех суток тахиаритмии.
Трепетание (мерцание) предсердий (рис. 15, 16) - тип суправентрикулярной тахикардии, при котором частота сокращения предсердий возрастает до 300-400-500 уд/мин, а частота желудочковых сокращений сохраняется на уровне 150-250 уд/мин за счет замедления АV проведения (2:1 или 3:1). При отсутствии аномалий сердца СВТ диагностируется во II-III триместре беременности.
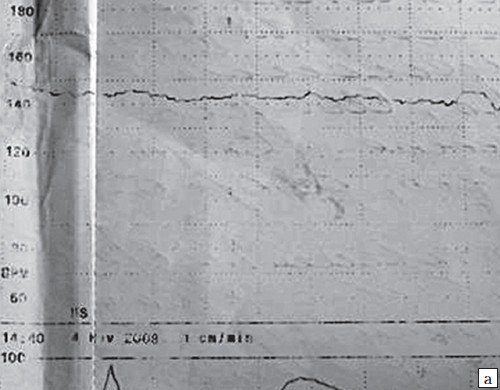
а) При очень высокой ЧСС плода крайне сложно интерпретировать аускультативные данные, кардиотокограмма также не отражает истинной ЧСС плода и выглядит как монотонный ареактивный ритм, все это может повлечь ошибочную клиническую диагностику дистресса плода.
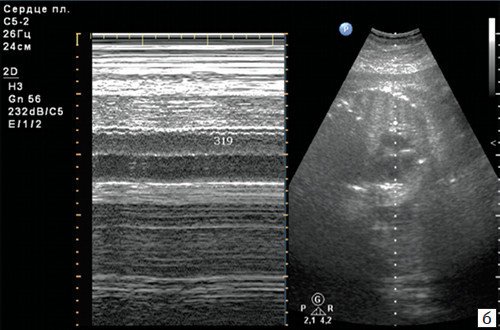
б) В М-режиме регистрируется ЧCC плода 300-320 уд/мин при АV проведении 1:1.
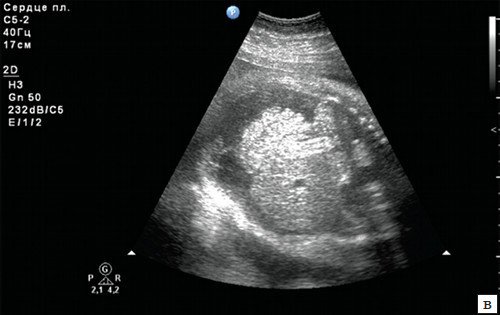
в) Универсальный отек плода.
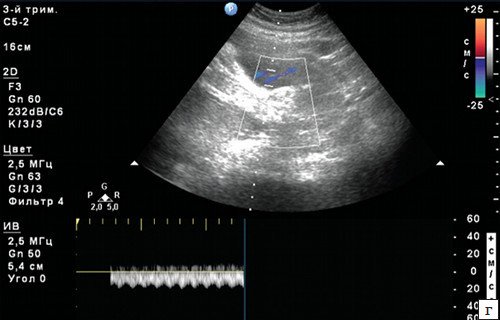
г) Допплеровский спектр в артерии пуповины без признаков повышения дистальной резистентности.

а) По типу трепетания предсердий с блоком 2:1.
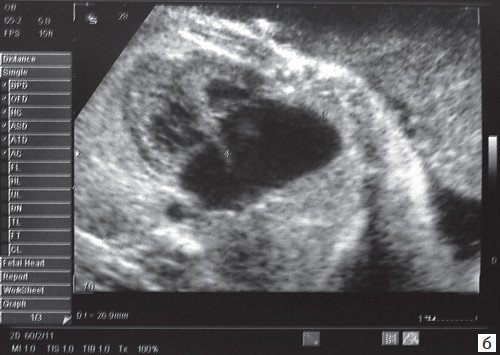
б) При аномалии Эбштейна. Частота сокращений предсердий 415 уд/мин, желудочков - 220 уд/мин.
При развитии суправентрикулярной тахикардии на антенатальном этапе крайне высок риск развития тяжелых осложнений - водянки (см. рис. 14, 15), гибели плода [10]. В формировании объема циркулирующей крови плода основное значение имеют не белки плазмы, а циркуляция лимфы: при венозном застое и возрастании венозного давления значительная часть жидкости оттекает в лимфатическую систему, где задерживается. Таким образом, патогенез водянки при аритмии плода связан с высокой гидрофильностью тканей [7]. Без антиаритмической терапии универсальный отек плода развивается обычно после нескольких суток тахиаритмии, и так же быстро восстанавливается после нормализации ритма ЧСС. Перинатальная смертность при наличии водянки составляет 20-50 % [11], а наличие структурных аномалий сердца значительно ухудшает постнатальный прогноз (см. рис. 16).
Одновременная артериально-венозная импульсно-волновая допплерография восходящей аорты и ВПВ c оценкой соотношения AV и VA интервалов позволяет дифференцировать варианты тахиаритмий с длинным и коротким VA интервалом, которые имеют разный механизм (рис. 17). Короткий VA интервал (VA/AV отношение < 1) связан с механизмом повторного входа волны возбуждения в сердце (re-entry-механизмом) с ускоренным VA проведением (RP interval
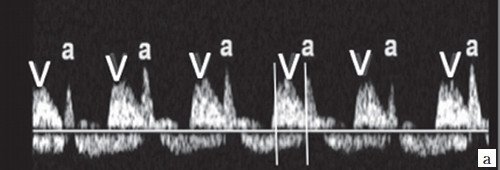
а) Короткий VA интервал (VA < AV).
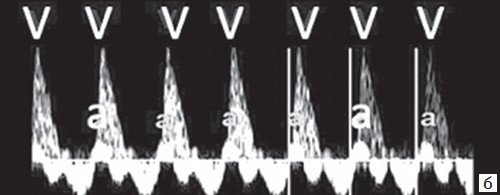
б) Длинный VA интервал (VA > AV).
Тахиаритмии с длинными и короткими VA интервалами имеют различный механизм, поэтому и различный прогноз трансплацентарной терапии.
В настоящее время досрочное родоразрешение при суправентрикулярной тахикардии признано патогенетически необоснованной тактикой (высокий риск развития отека легких у ребенка после рождения на фоне сохраняющейся тахиаритмии) [12]. Клиническими протоколами большинства зарубежных стран регламентировано проведение внутриутробной трансплацентарной антиаритмической терапии. В качестве препарата первой линии антиаритмического лечения плода широко применяется дигоксин. Соталол, амиодарон и флекаинид используются в качестве препаратов второго ряда, когда при помощи дигоксина не удается достичь нормализации синусового ритма [7, 13, 14].
Вентрикулярная тахикардия - редкий тип аритмии, проявляется возрастанием ЧСС желудочков, нормальным предсердным ритмом и разобщением сокращений предсердий и желудочков (рис. 18). Встречаются идиопатические (первичные) и вторичные варианты патологии на фоне органических изменений. Постнатально часто возникают осложнения.
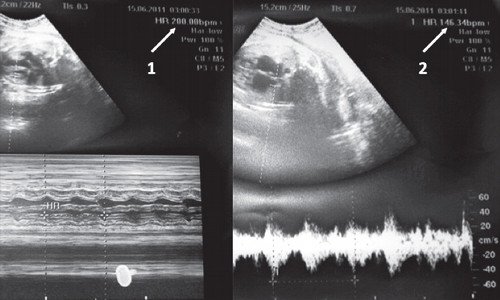
Частота сокращений желудочков (стрелка 1) 200 уд/мин, предсердий (стрелка 2) - 146 уд/мин.
Цель исследования - усовершенствование диагностики, адекватного прогнозирования и перинатальной тактики при различных типах фетальных аритмий.
Материал и методы
Проведено антенатальное эхографическое обследование 27 плодов с различными типами нарушения фетального сердечного ритма: транзиторными эпизодами брадикардии - асистолии во II триместре беременности (6); изолированными преждевременными сокращениями предсердий (5); изолированными преждевременными сокращениями желудочков (1); преждевременными сокращениями предсердий с блокированным проведением предсердно-желудочковых импульсов (4); синусовой брадикардией (3); AV блокадой II степени (1); полной AV блокадой (1); СВТ с AV проведением 1:1 (4); СВТ по типу трепетания предсердий с проведением 2:1 (1); вентрикулярной тахикардией (1). Эхографические и допплерографические исследования проводились с использованием современных ультразвуковых сканеров. После рождения проводился клинический мониторинг состояния детей, сравнительный анализ перинатальных результатов.
Результаты
На этапе антенат ального эхографического и допплерографического исследования плода возможен дифференциальный диагноз типа фетальной аритмии, а также прогноз эффективности трансплацентарной антиаритмической терапии и перинатальный прогноз. В 19 (76%) случаях нарушения сердечного ритма плода выявлялись в конце II - начале III триместра беременности. На рис. 4-18 представлены эхограммы и спектральные допплерограммы, иллюстрирующие различные типы нарушений сердечного ритма плода, а также приведены соответствующие данные неонатального катамнеза. Сравнительный анализ перинатальных результатов позволил выявить нарушения с благоприятным и неблагоприятным постнатальным прогнозом.
В исследованных нами случаях благоприятный постнатальный результат (нормализация ритма, отсутствие необходимости в коррекции после рождения) имели плоды со следующими типами нарушений фетального сердечного ритма: транзиторные эпизоды брадикардии - асистолии на этапе II триместра беременности; изолированные преждевременные сокращения предсердий; преждевременные сокращения предсердий с блокированным проведением предсердно-желудочковых импульсов (предсердная бигеминия либо тригеминия); СВТ 200-220 уд/мин, с АV проведением 1:1.
Необходимость в трансплацентарном антиаритмическом лечении, а также кардиохирургической или терапевтической коррекции после рождения имели новорожденные со следующими типами антенатальных аритмий: преждевременные сокращения желудочков (ассоциировались с дефектом межжелудочковой перегородки); СВТ 220-260 уд/мин с универсальным отеком плода; СВТ 194-205 уд/мин (постнатально нестабильный ритм за счет WPW-синдрома).
Неблагоприятный перинатальный результат (антенатальная, неонатальная смерть, тяжелые неонатальные и интраоперационные гемодинамические нарушения) имели следующие типы нарушений ритма плода: синусовая брадикардия (ассоциация с антенатальным метаболическим ацидозом, респираторными, гемодинамическими и неврологическими расстройствами в неонатальном периоде, перинатальными потерями); AV блокада II и III степени (ассоциация с универсальным отеком и антенатальной гибелью плода); СВТ 300-319 уд/мин при проведении 1:1 с водянкой плода; СВТ по типу трепетания предсердий с блоком 2:1 (сопутствующая аномалия Эбштейна); вентрикулярная тахикардия (ассоциация с гемодинамической нестабильностью и отеком легких новорожденного).
Выводы
Большинство выявленных нарушений сердечного ритма плода обнаруживаются на этапах конца II - начала III триместра, что подтверждает мнение о необходимости проведения третьего ультразвукового исследования в этот период беременности. При обнаружении аритмии плода с неблагоприятным либо неоднозначным перинатальным прогнозом целесообразно родоразрешение в акушерском стационаре высшего уровня аккредитации - перинатальном центре.
Литература
- George M. Graham. Evaluation of Fetal Arrhythmias. Donald School Journal of Ultrasound in Obstetrics and Gynecology 2010; 4(1): 51-57.
- Callen P.W. Ultrasonography in Obstetrics and Gynecology: Elsevier Health Sciences, 2011. 1180 p.
- Strasburger J.F., Wakai R.T. Fetal cardiac arrhythmia detection and in utero therapy. Nat.Rev.Cardiol. 2010; 7(5): 277-290.
- Бокерия Е.Л. Фетальные и неонатальные аритмии (клиника, диагностика, лечение) // Автореф. дис. д-ра мед. наук. Москва, 2012. 48 с.
- Pasquini L., Seale A.N., Belmar C. et al. PR interval: a comparison of electrical and mechanical methods in the fetus. Early Hum. Dev. 2006; 83(4): 231-237.
- Котлукова Н.П., Хузина О.М., Немировский В.Б. и др. Фетальные и неонатальные нарушения сердечного ритма и проводимости // Педиатрия. 2007. Т 8, N 2. С. 5-12.
- Gembruch U., Hecher K., Steine H. Ultraschalldiagnostik in Geburtshilfe und Gynдkologie (German Edition): Springer, 2013: P. 385-394.
- Maeno Y., Hirose A., Kanbe T., Hori D. Fetal arrhythmia: prenatal diagnosis and perinatal management. J. Obstet. Gynaecol. Res. 2009; 35(4): 623-629.
- Sonesson S.E. Diagnosis and treatment of fetal Arrhythmias // XIX Nordic Congress of Perinatal Medicine, May 19-21, 2005, Lund.
- Fouron J.C. Fetal arrhythmias: The saint-Justine Hospital experience. Prenatal Diagnosis 2004; 24: 1068-1080.
- Oudjik M.A., Gooskens R.H.J.M., Stoutenbeek P. et al. Neurological outcome of childreen who were treated for fetal tachycardia complicated by hydrops. Ultrasound Obstet Gynecol 2004; 24: 154-158.
- Fouron J.C., Fournier A., Proulx F. et al. Management of fetal tachyarrhythmia based on superior vena cava/aorta Doppler flow recordings. Heart 2003; 89: 1211-1216.
- Schleich J.M., Bernard du Haut Cilly F., Laurent M.C. et al. Early prenatal managment of fetal ventricular tachycardia treated in utero by amiodarone with long term follow-up. Prenat Diagn 2000; 20: 449-452.
- Frohn-Mulder I.M., Stewart P.A., Witsenburg M. et al. The efficacity of Flecaпne versus digoxin in the managment of fetal supraventricular tachycardia. Prenat Diagn. 1995;15: 1297-1302.

УЗИ сканер Samsung W10
Аппарат экспертного/премиум класса поможет расширить возможности диагностики, благодаря интуитивно понятным алгоритмам обработки и точным инструментам анализа.
Публикации по теме
- Неразвивающаяся внематочная беременность. Случай из практики - Лукьянова Е.А.
- Оценка носовой кости в I триместре беременности: как, где, когда и зачем мы делаем - Андреева Е.Н.
- Фетальные аритмии: антенальная ультразвуковая дифференциальная диагностика, прогнозирование постнатальных результатов и перинатальная практика - Сафонова И.Н.
- Гемодинамика матки после хирургического гемостаза при акушерских кровотечениях - Волков А.Е.
- Возможности 3D эхографии в прогнозировании репродуктивных исходов после консервативной миомэктомии - Тохунц Карине


