Ультразвуковые и допплерографические критерии диагностики вариантов фето-фетальной трансфузии и селективной задержки роста одного из монозиготных близнецов
Институт педиатрии, акушерства и гинекологии АМН Украины, Киев.
Рубрика: Эхография в акушерстве
УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Фето-фетальный трансфузионный синдром (ФФТС) - тяжелое осложнение течения многоплодной монохориальной беременности, cвязанное с наличием трансплацентарных сосудистых коммуникаций. Синдром развивается в 10-15% случаев при монозиготной беременности [1, 2]. В основе этиопатогенеза синдрома лежит циркуляторный дисбаланс между внутриплацентарными сосудистыми руслами плодов-близнецов. Некорригированное течение синдрома сопровождается высокой перинатальной смертностью и заболеваемостью - с частотой от 56 до 100% в зависимости от гестационного срока, формы и тяжести гемодинамических нарушений [3, 4].
За счет наличия межпуповинных васкулярных аномалий формируются межблизнецовые отношения "плод-донор - плодреципиент" [5]. Вследствие несбалансированной гемотрансфузии у донора развивается гиповолемия и анемия на фоне резкой задержки внутриутробного роста, формируется выраженный олигогидрамнион. У близнецареципиента за счет гемодинамического дисбаланса развивается гиперволемия и полицитемия. Увеличение почечного кровотока и повышение продукции мочи приводит к возрастанию объема амниотической жидкости, резко выраженному полигидрамниону - фактору повышенного риска индукции преждевременных родов [6-8].
Хронический ФФТС необходимо дифференцировать с другими патологическими состояниями монозиготной многоплодной беременности, встречающимися реже: острой межблизнецовой трансфузией (ОМТ) и селективной задержкой роста (CЗР) одного из плодов. Несмотря на ряд схожих клинических проявлений, эти состояния имеют прогноз, отличный от прогноза при хроническом тяжелом ФФТС, требуют иной терапевтической тактики.
Хроническая форма ФФТС проявляется с середины II триместра гестации, имеет тяжелое течение, сопряжена с резко выраженным гемодинамическим дисбалансом между циркуляторными системами плодовблизнецов [9]. Клинически в течении хронического ФФТС различают 5 стадий (таблица). Критериями, на основании которых дифференцируется клиническая стадия синдрома, являются ультразвуковые и допплерографические изменения [10].
| Ультразвуковые критерии | Клиническая стадия ФФТС | ||||
|---|---|---|---|---|---|
| I | II | III | IV | V | |
| Полиолигогидрамнион | + | + | + | + | + |
| Мочевой пузырь донора | + | - | - | - | - |
| Патологические допплерограммы | - | - | + | + | + |
| Водянка реципиента | - | - | - | + | + |
| Внутриутробная гибель плода (плодов) | - | - | - | - | + |
При естественном некорригированном течении тяжелого хронического ФФТС прогноз для реципиента неблагоприятен, для донора - абсолютно неблагоприятен. В случае антенатальной гибели одного из плодов (донора) развивается острая гиповолемия реципиента с переносом тромбопластического материала от умершего плода к живому и развитием у него ДВС-синдрома (диссеминированное внутрисосудистое свёртывание) и церебральных нарушений, что представляет непосредственную угрозу для его жизни и может приводить к тяжелой инвалидизации в последующем. Этиопатогенетически обоснованная терапевтическая тактика при данном варианте осложнения многоплодия - фетоскопическая лазерная коагуляция трансплацентарных анастомозов [11, 12]. Многочисленные публикации последних лет свидетельствуют о возможности эффективно снизить перинатальную смертность при тяжелом течении синдрома за счет устранения функционирующих межблизнецовых сосудистых шунтов [13, 14].
Острая межблизнецовая трансфузия (ОМТ) - циркуляторный дисбаланс, развивающийся на фоне предшествующего благополучия. Манифестирует позже чем хронический ФФТС - в конце II-III триместров. Рекомендуемая терапевтическая тактика при развитии острого многоводия во время беременности - cерийные декомпрессионные амниоредукции, снижающие риск преждевременных родов [15].
Селективная задержка роста одного из близнецов (дискордантный рост монозиготных близнецов) характеризуется отставанием роста одного из плодов [15]. При этом межблизнецовая трансфузия незначительна либо отсутствует, патогенез нарушений связан преимущественно с проявлениями плацентарной дисфункции, либо функциональной патологией плода. Терапевтическая тактика в большинстве таких случаев выжидательноконсервативная [16]. При остром нарушении плацентарно-плодового кровообращения возможна антенатальная гибель одного из плодов-близнецов. В подобном случае показана фетоскопическая лазерная коагуляция его пуповины. При наличии соответствующего гестационного срока и адекватной перинатальной тактике прогноз для жизни и здоровья второго плода может быть благоприятным.
Очевидной представляется невозможность клинической диагностики ФФТС на антенатальном этапе без применения серийных ультразвуковых и допплерографических исследований.
Целью работы явилось выявление последовательности ультразвуковых и допплерографических изменений на разных стадиях некорригированного хронического ФФТС, при острой межблизнецовой трансфузии и селективной задержке роста одного из монозиготных близнецов.
Материалы и методы
Проведен ультразвуковой и допплерометрический фетоплацентарный мониторинг 5 пар близнецов с некорригированым осложненным течением монохориальной двуплодной беременности: трех - с хроническим прогрессирующим ФФТС, одной - клиническими проявлениями ОМТ, одной - селективной задержкой роста одного из близнецов. Оценивалась динамика фетометрических данных, особенности доступных визуализации внеплацентарных пуповинных сосудов, количество амниотической жидкости, проводилась триплексная допплерография кровотока пуповинных артерий, фетальных сосудов - аорты и венозного протока.
Проведен сравнительный анализ перинатальных исходов, а также результатов патоморфологических исследований последов.
Результаты и обсуждение
У двух из 3 женщин с хроническим ФФТС имелись указания на наличие в анамнезе пороков развития плода, перинатальных потерь и преждевременных родов. Средний возраст женщин составил 27,8±0,8 лет.
Минимальными опорными ультразвуковыми критериями клинической стадии синдрома были сочетание маловодия и многоводия амниотических полостей близнецов при диспропорциональных фетометрических показателях. При исследовании плодов в 20-21 нед выявлено отставание размеров одного из близнецов в среднем на -1,2±0,17 SD. В 25 нед размеры плодов-доноров соответствовали 23,2±1,4 нед, в дальнейшем динамика их фетометрических показателей отсутствовала. Динамика роста плодов-реципиентов на протяжении всей серии исследований соответствовала средним показателям для срока гестации.
На рис. 1-12 представлены ультразвуковые и допплерографические признаки разных клинических стадий тяжелой формы хронического прогрессирующего ФФТС.
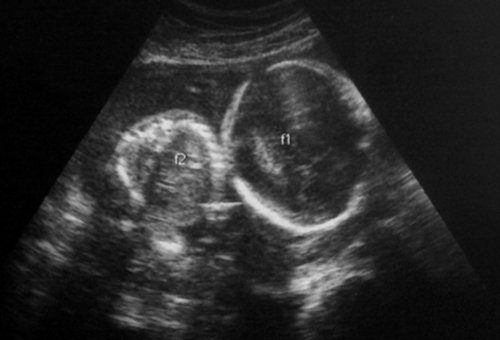
Рис. 1. Двуплодная монохориальная беременность, гестационный срок 25 нед. Выраженно дискордантный рост плодов: поперечное сечение туловища плода-донора (слева), аксиальное сечение головы плода-реципиента (справа). Отставание фетометрических показателей меньшего плода более чем на 3 SD.
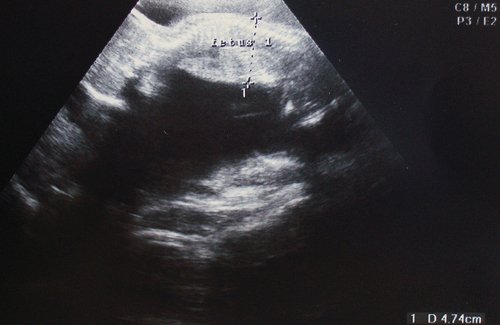
Рис. 2. "Застрявший" близнец ("кокон-признак") - косвенный критерий олигогидрамниона. Плод фиксирован у передней стенки матки, неподвижен. Полигидрамнион близнеца-реципиента (глубокий карман амниотической жидкости ниже изображения плода). Cимметричная задержка роста плода-донора. На сонограмме его мочевой пузырь еще визуализируется. I стадия ФФТС.
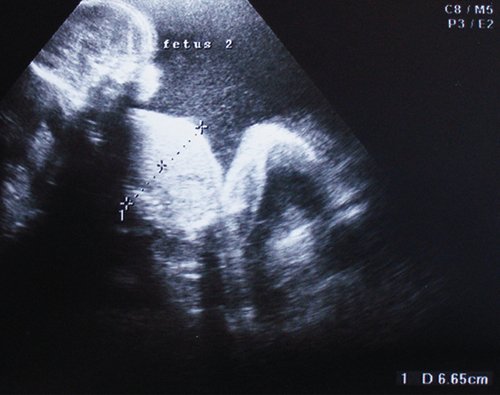
Рис. 3. Плод-реципиент, имеющий нормальные для срока гестации размеры.
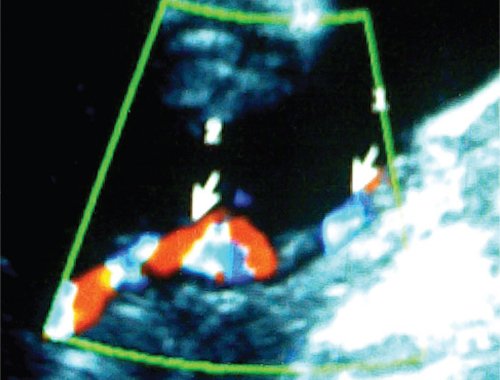
Рис. 4. Режим ЦДК. Внеплацентарные пуповинные аномалии: гипоплазия и оболочечное прикрепление пуповины плода-донора (правее), краевое отхождение от плаценты пуповины плода-реципиента (слева). Визуализируется участок пуповины меньшего диаметра, в котором отсутствует регистрация кровотока (стрелка) - нефункционирующий внеплацентарный шунт.
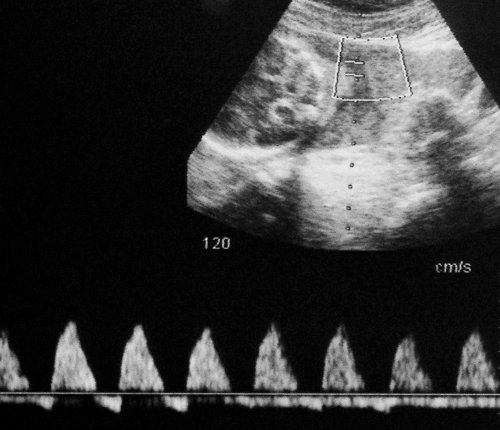
Рис. 5. Длительно регистрируемый постоянный нулевой диастолический кровоток, эпизоды реверсного диастолического кровотока в пуповинных артериях плода-донора. III стадия фето-фетального трансфузионного синдрома.
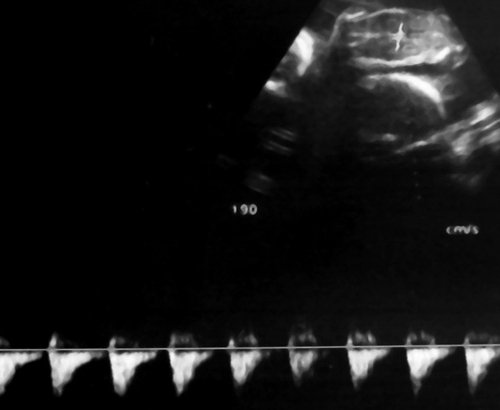
Рис. 6. Длительно регистрируемый нулевой диастолический кровоток в аорте близнеца-донора. Отсутствует визуализация мочевого пузыря плода.
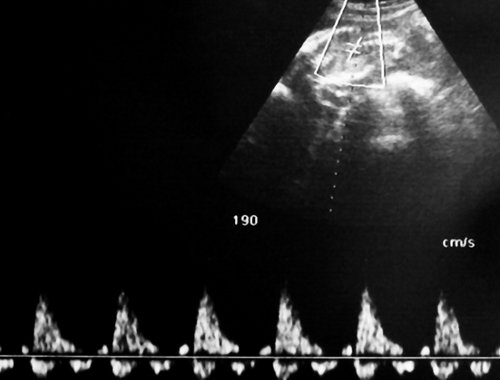
Рис. 7. Реверсный диастолический кровоток в торакальной аорте близнеца-донора. В условиях фето-фетальной трансфузии спектры, характерные для терминальной фетальной гемодинамики, могут регистрироваться до нескольких недель.
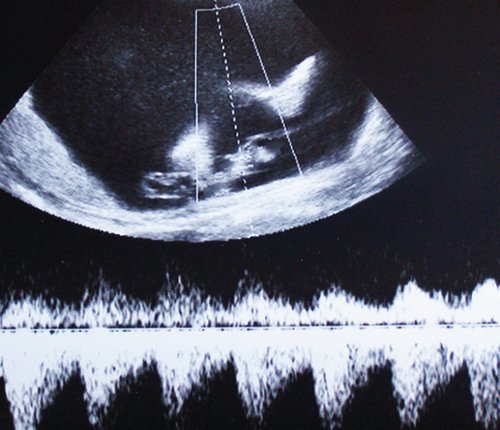
Рис. 8. Нормальная спектральная допплерограмма пуповинных артерий плода-реципиента сохраняется даже на фоне его терминального состояния, вплоть до внутриутробной гибели; выраженный полигидрамнион.
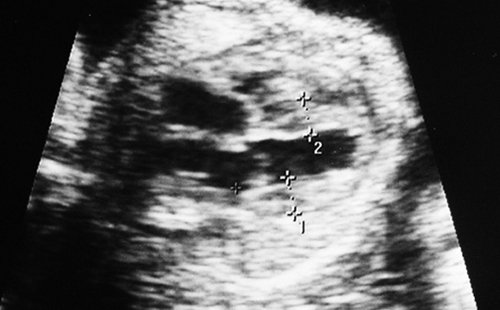
Рис. 9. Гипертрофическая компенсаторная кардиомегалия плода-реципиента (гестационный срок 26-27 нед): площадь сечения сердца занимает около 1/2 площади поперечного сечения грудной клетки, толщина миокарда желудочков и межжелудочковой перегородки сердца плода 6,5 и 6,8 мм соответственно.
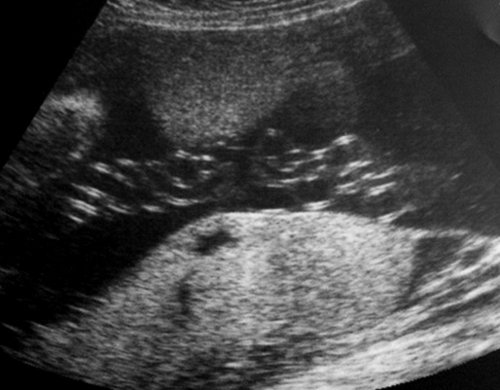
Рис. 10. Пуповина плода-реципиента с признаками многократного "скручивания". Изменения зарегистрированы одновременно с допплерографическими признаками повышения резистентности венозного протока (см. рис. 11).
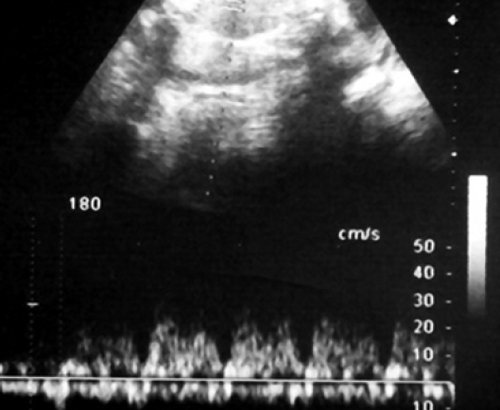
Рис. 11. Начальная стадия нарушения венозной гемодинамики плода-реципиента - повышение резистентности в венозном протоке, которое предшествует началу развития отека (маркер скорого перехода III клинической стадии в IV).
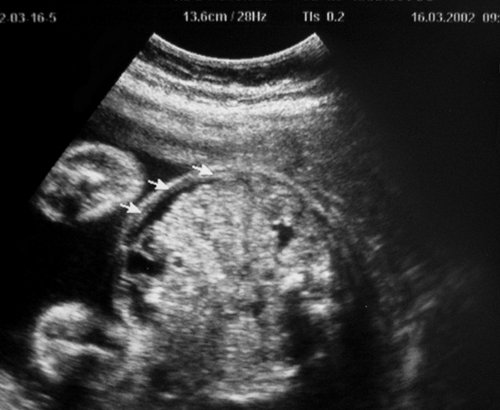
Рис. 12. Признаки развития сердечной недостаточности плода-реципиента вследствие гемодинамической перегрузки, начальный асцит (стрелки). IV, предтерминальная, стадия тяжелого хронического фето-фетального трансфузионного синдрома. Внутриутробная гибель обоих плодов наступила менее чем через 24 ч.
Определение выраженного многоводия амниотической полости большего плода не вызывало затруднений и характеризовалось значительной глубиной вертикального кармана амниотической жидкости (11,34±2,26 см). В то же время адекватное измерение размеров амниотической полости меньшего плода оказалось почти невозможным, особенно в случае агидрамниона, так как амниотическая оболочка плотно прилежит к плоду, "укутывая" его. Ультразвуковой симптомом агидрамниона при этом служит признак "кокона", или "застрявшего" плода ("stuck twin"): плоддонор прилежит к одной из стенок матки, фиксирован собственной амниотической оболочкой, неподвижен [3]. Признак сохранялся при динамическом наблюдении на всех стадиях прогрессирующего ФФТС. Формированию агидрамниона патогенетически предшествовало появление прогностически неблагоприятного ультразвукового симптома - отсутствия визуализации мочевого пузыря донора, что свидетельствовало о запуске патологических гемодинамических механизмов, прогрессивном течении синдрома и развитии его II клинической стадии.
Межблизнецовые внутриплацентарные анастомозы были не единственным проявлением особенностей пуповинных сосудов. Для всех плодов при тяжелом хроническом ФФТС были характерны различные внеплацентарные изменения морфологии пуповин, выявленные антенатально в разных сочетаниях с помощью УЗИ: различная толщина пуповин близнецов за счет гипоплазии пуповинных сосудов меньшего плода, а также его гиповолемии; аномальное количество сосудов; децентрированное (краевое) отхождение пуповинных сосудов от плаценты; оболочечный ход сосудов пуповины; внеплацентарные межпуповинные анастомозы; многократно перекрученная, чрезмерно извитая пуповина большего плода; отсутствие спирального хода сосудов пуповины меньшего плода.
Патогномоничными для III клинической стадии тяжелой формы хронического ФФТС были гемодинамические изменения фетальных и пуповинных сосудов, регистрируемые с помощью спектральной допплерографии.
Для фетоплацентарной гемодинамики плодадонора было характерным резкое снижение - вплоть до отсутствия - кровотока в почечных артериях. Длительной (до нескольких недель) была регистрация терминальных типов гемодинамических спектров: нулевого и реверсного диастолического кровотока в пуповинных артериях, торакальном и абдоминальном отделах аорты плода-донора. Средняя длительность периода регистрации терминальных гемодинамических спектров в пуповинных артериях и аорте донора составила 2,6±0,5 нед. Следует отметить, что в других случаях, вне ФФТС, регистрация критических гемодинамических фетальных и плацентарно-плодовых нарушений предшествует быстрому - в течение 24-72 ч - развитию терминального состояния и внутриутробной гибели плода [17].
В то же время для пуповинных артерий плода-реципиента были характерны нормальные показатели кровотока, без повышения индексов сосудистой резистентности, регистрируемые вплоть до развития декомпенсированной трансфузии и гибели плодов. Особенностью плодовой гемодинамики близнеца-реципиента являлось нарастание объемной перегрузки с развитием застойной сердечной недостаточности, имевшей допплерографические проявления в виде повышения резистентности кровотока в субдиафрагмальных венозных сосудах плода прежде всего в венозном протоке. Ультразвуковым критерием позднего периода III клинической стадии ФФТС была регистрация допплерограммы венозного протока плода-реципиента с повышением систолодиастолического отношения (S/D) более 3,5. Таким образом, при тяжелом хроническом ФФТС именно патологические венозные допплерограммы реципиента свидетельствуют о скором развитии предтерминального состояния, что необходимо принимать во внимание при выработке акушерской тактики.
Во всех 3 случаях у близнеца-реципиента наблюдалась гипертрофическая кардиомиопатия, имевшая сначала "рабочий", компенсаторный характер в связи с гиперволемией, с формированием затем диастолической и систолической дисфукции. Средняя толщина миокарда желудочков сердца большего плода на этапе предтерминальной стадии ФФТС составляла 6,57±0,02 мм, толщина миокарда межжелудочковой перегородки - 7,18±0,04 мм.
Вслед за регистрацией патологического спектра кровотока в венозном протоке быстро появлялись ультразвуковые признаки застойной сердечной недостаточности плода-реципиента: асцит, гидроторакс, гидроперикард либо анасарка, что отражало развитие IV клинической стадии тяжелого хронического ФФТС. Эта стадия в 2 случаях имела небольшую продолжительность (1-2 дня) и завершилась регистрацией внутриутробной гибели обоих пар плодов в 27+4и 28+2нед гестации; вес близнецов при рождении составил 690 и 1140 г и 810 и 1280 г, соответственно. В третьем случае при регистрации нарушений венозной гемодинамики реципиента было проведено оперативное родоразрешение в 30+1нед (вес при рождении составил 780 и 1630 г, меньший плод погиб интранатально, у большего плода имели место тяжелый интранатальный дистресс, полицитемия и неонатальные осложнения, связанные с недоношенностью).
Морфологическое исследование последа во всех случаях выявило наличие различных форм внутриплацентарных сосудистых анастомозов (артерио-артериальных, васкулярных цепей, артериовенозных, вено-венозных и сочетанных форм), а также внеплацентарных пуповинных аномалий.
В качестве иллюстрации синдрома острой межблизнецовой трансфузии и селективной задержки роста одного из плодов приводим клинические наблюдения.
Пациентка К., 28 лет, первобеременная, с монохориальной двуплодной беременностью, отягощенной синдромом острой межблизнецовой трансфузии,находилась под наблюдением с 31+3нед гестации в связи с быстро нарастающим многоводием при симметричном росте плодов, соответствующем средним гестационным параметрам (рис. 13). Ультразвуковой мониторинг выявил нормальную динамику биометрических показателей плодов. На протяжении серии последовательных наблюдений сохранялся почечный кровоток обоих плодов и визуализация их мочевых пузырей. Допплерографические показатели плодово-плацентарной и фетальной артериальной и венозной гемодинамики не были нарушены. Выраженное прогрессирующее многоводие индуцировало преждевременное отхождение околоплодных вод первого плода в 32 нед, в связи с чем наблюдалась асимметрия объема амниотических полостей плодов. Преждевременные роды произошли в 33+5нед беременности, вес плодов при рождении составил 2050 и 2120 г. Постнатально у одного из близнецов наблюдалась полицитемическая гиперволемия (при рождении Hb 193 г/л), у второго - гиповолемия, анемия (Hb 122 г/л). Перинатальные осложнения были связаны преимущественно с недоношенностью, при этом новорожденные имели в целом благоприятный прогноз. По данным морфологического исследования, в плаценте имели место артерио-артериальные анастомозы.
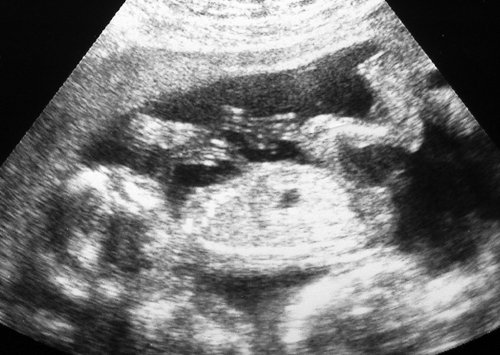
Рис. 13. Беременность 31 нед. Монохориальная моноамниотическая двойня. Острая межблизнецовая трансфузия. Выраженное острое многоводие.
Селективная задержка роста одного из плодов. У беременной И., 20 лет, (в анамнезе 1 самопроизвольный аборт), при УЗИ в 21 нед были обнаружены признаки умеренно дискордантного роста монозиготных близнецов - отставание размеров одного из плодов (-0,65 SD). С 28 нед и до завершения беременности различия фетометрических параметров и расчетной массы плодов составляли 13,7±1,13% (рис. 14). При динамическом измерении максимальных вертикальных карманов амниотических полостей наблюдалась стойкая асимметрия значений - 68,4±9,65 и 95,3±7,13 мм у меньшего и большего близнецов, соответственно. Эхографические признаки хронического прогрессирующего ФФТС, а также особенности доступных визуализации внеплацентарных пуповинных сосудов отсутствовали. Допплерографически выявлялись нарушения плодово-плацентарной артериальной гемодинамики обоих плодов: S/D в пуповинных артериях меньшего плода 4,13±0,567, в пуповинных артериях большего плода - 3,83±0,644 за период наблюдения за счет повышения периферической резистентности плацентарного сосудистого русла. Средние значения S/D в венозном протоке плодов не превышали нормальные и регистрировались на уровне 2,86±0,186 и 2,79±0,134. В исходе беременности - преждевременные роды в 36 нед, интранатальный дистресс меньшего плода, при рождении масса близнецов составила 2340 и 2770 г, гемоглобин новорожденных - 170 и 174 г/л. Патоморфологическое исследование последа не выявило наличия внутриплацентарных сосудистых анастомозов.
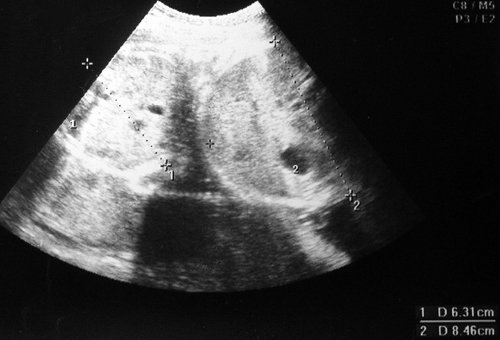
Рис. 14. Беременность 35-36 нед. Дискордантный рост монозиготных близнецов. Поперечные сечения туловищ плодов, имеющие разные диаметры и окружности. Допплерографически регистрировались признаки повышения резистентности в пуповинных артериях обоих плодов, венозная фетальная гемодинамика без изменений.
Выводы
В современной акушерской клинике сонография имеет безусловный приоритет как в первичной диагностике фето-фетального трансфузионного синдрома, так и в определении его клинической стадии, оценке гемодинамики фетоплацентарных систем плодов, их функционального состояния, прогнозировании перинатального исхода, дифференциальном диагнозе с другими вариантами осложнений монохориального многоплодия. Адекватный диагноз является необходимым условием выработки индивидуальной терапевтической тактики и cпособствует улучшению перинатальных результатов.
Литература
- Urig M.A., Clewell W.H., Elliott J.P. Twin-twin transfusion syndrome //Am. J. Obstet. Gynecol. 1990. V. 163. P. 1522-1526.
- Некрасова Е.С. Многоплодная беременность М.: Реальное Время, 2009. 144 с.
- Quintero R.A., Chmait R.H. The cocoon sign: a potential sonographic pitfall in the diagnosis of twin-twin transfusion syndrome // Ultrasound Obstet. Gynecol. 2004. V. 23. Р. 38-41.
- Campbell S. Opinion: twin-to-twin transfusion syndrome: debates on the etiology, natural history and management // Ultrasound. Obstet. Gynecol. 2000. V. l6. P. 210-213.
- Bermudes C., Becerra C.H., Bornick P.W. et al. Plasental types and twin-twin transfusion syndrome // Am. J. Obstet. Gynecol. 2002. V. 187. P. 489-494.
- Bruner J.P., Rosemond R.L. Twin-to-twin transfusion syndrome: a subset of the twin oligohidramnios- polyhydramnios sequence //Am. J. Obstet. Gynecol. 1993. V. 169. P. 925-930.
- Cincotta R.B., Oldham J., Sampson A. Antepartum and postpartum complications of twin-twin transfusion // Aust. NZ. J. Obstet. Gynecol. 1996. V. 36. P. 303-308.
- Galea P., Scott J. M., Goel K.M. Feto-fetal transfusion syndrome // Arch. Dis. Child. 1982. V. 57(10). Р. 781-783.
- Гусева О.В. Фето-фетальный трансфузионный синдром: современные представления о патогенезе, диагностике и лечении // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. 2000. N1. С. 7-17.
- Quintero R.A, Bornick P.W., Morales W.J. et al. Stage-based treatment of twin-twin transfusion syndrome: preliminary study / 10th World Congress of Ultrasound in Obstetrics and Gynecology. 2000; Zagreb, Croatia.
- Maschke C., Diemert A., Hecher K., Bartmann P. Long-term outcome after intrauterine laser treatment for twin-to-twin transfusion syndrome // Prenatal. Diagnosis. 2011. V. 31(7). P. 647-653.
- Chalouhi G.E., Essaoui M., Stirnemann J. et al. Laser therapy for twin-to twin transfusion syndrome (TTTS) // Prenatal Diagnosis. 2011. V. 31(7). P. 637-646.
- Senat M.V., Deprest J., Boulvain M. et al. Endoscopic laser surgery versus serial amnioreduction for severe twin-to-twin transfusion syndrome // N. Engl. J. Med. 2004. V. 351. P. 136-144.
- Robyr R., Quarello E., Ville Y. Management of fetofetal transfusion syndrome // Prenat. Diagn. 2005. V. 25(9). P. 786-95.
- Thilaganathan B., Sairam S., Papageorghiou A.T., Bhide A. Problem-based obstetric ultrasound / Informa UK, 2007. P. 117-120.
- Huber A., Diehl W., Zikulnig L. et al. Perinatal outcome in monochorionic twin pregnancies complicated by amniotic fluid discordance without severe twin-twin transfusion syndrome // Ultrasound Obstet. Gynecol. 2006. V. 27(1). Р. 48-52.
- Абдуллаев Р.Я., Сафонова И.Н., Лукьянова И.С. Допплерометрия сосудов фетоплацентарного комплекса: диагностика плацентарных нарушений. Харьков: Нове слово, 2008. 52 с.

УЗИ аппарат HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Публикации по теме
- Новые ультразвуковые технологии в оценке постнатального прогноза при диафрагмальной грыже у плода - Юдина Е.В.
- Новый ультразвуковой признак в оценке срединных структур головного мозга плода в 11-14 недель беременности в норме - Андреева Е.Н.
- Ультразвуковые и допплерографические критерии диагностики вариантов фето-фетальной трансфузии и селективной задержки роста одного из монозиготных близнецов - Сафонова И.Н.
- Нейробластома плода. Возможности пренатальной диагностики и прогноз - Тихоненко И.В.
- Осмотр сердца плода в ходе рутинного ультразвукового исследования во II триместре беременности: анализ наиболее распространенных ошибок - E.C. Некрасова

