Возможности ультразвукового исследования в диагностике кистозной формы дуоденальной дистрофии
Рубрика: Эхография брюшной полости

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Эктопией или гетеротопией поджелудочной железы называется необычная локализация панкреатической ткани, имеющей собственное кровоснабжение и протоковую систему, без сосудистого, нервного или анатомического контакта с обычно расположенной (ортотопической) поджелудочной железы [1, 2]. Гетеротопия поджелудочной железы может происходить либо вследствие метаплазии полипотентных эндодермальных клеток in situ, либо посредством перемещения эмбриональных панкреатических клеток в соседние структуры [2, 3].
Чаще всего эктопию поджелудочной железы обнаруживают случайно при аутопсиях, операциях или эндоскопических исследованиях верхних отделов желудочно-кишечного тракта. Первое сообщение о выявлении гетеротопии панкреатической ткани, вызвавшей обструкцию пилорического отдела кишки, и обзор литературы, посвященной причине этого явления, сделал E.G. Krieg в 1941 г. [4]. Эктопическая поджелудочная железа выявляется в стенке двенадцатиперстной кишки в 25-35% случаев [5, 6].
В отечественной литературе встречаются лишь единичные сообщения о данной патологии. Первое сообщение было сделано В.Я. Левкиным в 1982 г. [7], позднее, в 1995 г., М.В. Данилова и Т.В. Саввина сообщили о результатах исследования, основанного на анализе операционного материала пациентов с данной патологией [8]. Сообщения о предоперационной диагностике эктопической поджелудочной железы в отечественной литературе отсутствуют.
Несмотря на врожденный характер патологии, панкреатическая гетеротопия любой локализации обычно проявляется у взрослых вследствие вызываемых ею осложнений [9, 10] и до появления жалоб лечения не требует [11].
К редким осложнениям эктопической поджелудочной железы относятся также кистозная дистрофия и злокачественная трансформация [9, 12, 13].
Дуоденальная дистрофия - это хроническое воспаление ткани поджелудочной железы, эктопированной в стенку двенадцатиперстной кишки. Из-за затруднений в постановке диагноза и неопределенных признаков впервые она была описана только в 1970 г. французскими авторами F. Potet и N. Duclert [14]. Дуоденальная дистрофия чаще встречается в молодом возрасте, проявляясь фиброзным утолщением стенки двенадцатиперстной кишки с образованием кист в ее мышечном и/или подслизистом слое [15]. Заболевание может быть самостоятельным, но прогрессирование эктопического панкреатита (обычно в вертикальной ветви двенадцатиперстной кишки) может приводить к сдавливанию главного панкреатического протока и последующему обструктивному панкреатиту в ортотопической железе [15, 16]. В зависимости от преобладания фиброзных или кистозных изменений выделяют кистозный и солидный варианты дуоденальной дистрофии, которые являются не разными заболеваниями, а стадиями одного патологического процесса. Отношение к варианту определяется диаметром кист, выявляемых при лучевых методах исследования: кистозной формой заболевания считается при диаметре кист более 1 см, солидной - менее 1 см [16].
Клинически заболевание проявляется такими неспецифическими симптомами, как боли в эпигастральной области или правом подреберье, потеря веса, тошнота и рвота, вызываемая дуоденальным стенозом.
В отличие от гетеротопий других локализаций осложнением дуоденальной дистрофии обычно является острый или хронический панкреатит в ортотопической железе [10, 17] с образованием воспалительной опухоли в головке или поражением железы на всем протяжении с дилатацией главного протока. Дифференциальная диагностика при данной патологии проводится с опухолями, воспалительными заболеваниями и врожденными аномалиями.
Выявление эктопической поджелудочной железы до операции - достаточно сложная задача, даже с использованием современных диагностических возможностей. В литературе мы не нашли сообщений о критериях диагностики данной патологии при трансабдоминальном ультразвуковом исследовании. Несмотря на то, что исследователи отмечали использование трансабдоминального УЗИ при обследовании пациентов [18], данных о его эффективности и роли в алгоритме обследования не приведено.
Материал и методы
В Институте хирургии им. А.В. Вишневского с 2005 по 2009 г. проходили обследование и хирургическое лечение 15 пациентов (из них 13 мужчин) с кистозной формой дуоденальной дистрофии. Возраст пациентов варьировал от 25 до 65 лет. До операции всем пациентам выполняли УЗИ, включавшее исследование в В-режиме, дуплексное сканирование в режимах цветового допплеровского картирования, энергии отраженного допплеровского сигнала и импульсной допплерографии, при необходимости выполняли трех- и четырехмерную реконструкцию ультразвукового изображения.
Все пациенты были оперированы, образования морфологически верифицированы как кистозная форма дуоденальной дистрофии.
В 23 (95,8%) случаях кистозная форма дуоденальной дистрофии была диагностирована до операции по данным лучевых методов диагностики. В 1 наблюдении дооперационно предполагали наличие гастроинтестинальной стромальной опухоли двенадцатиперстной кишки, которую при морфологическом исследовании верифицировали как кистозную форму дуоденальной дистрофии.
В 23 наблюдениях картина заболевания была типичной, в 1 - атипичной. На наш взгляд, типичную и атипичную формы целесообразно рассмотреть отдельно.
Результаты исследования
Анализ данных анамнеза и результатов клинического обследования показал, что в большинстве случаев (79,2%) заболевание имеет достаточно длительное течение - от 1 года до 11 лет. За этот период пациентов неоднократно госпитализировали в разные стационары, где им проводилось лечение, однако, как правило, в качестве основного был поставлен диагноз хронического панкреатита. Дуоденальная дистрофия не была верифицирована ни в одном случае, поэтому 19 пациентов обратились в Институт хирургии им. А.В. Вишневского с беспокоящими их в течение достаточно длительного времени жалобами. В 4 случаях обращение в институт было связано с наличием у пациентов кистозного образования в эпигастральной области, диагностированного по данным лучевых методов исследования, однако без указания точной локализации, жалоб они не предъявляли. Один больной был госпитализирован в связи с невозможностью перорального приема пищи, а в течение последних 3 дней даже жидкости, 22 пациента предъявляли жалобы на боли различного характера, 21 - в верхнем отделе брюшной полости, 12 - на похудание.
При рассмотрении пола и возраста пациентов наши данные свидетельствуют, что возраст мужчин варьировал от 34 до 65 лет (в среднем 49,37±2,10 года), женщин - от 25 до 60 лет (в среднем 46±10,69 лет). Таким образом, развитие заболевания у взрослого пациента происходит в любом возрасте независимо от пола.
Анализ приведенных данных свидетельствует, что во всех случаях было диагностировано утолщение стенки нисходящей ветви двенадцатиперстной кишки, в толще которой выявлялись кистозные образования: одно (рис. 1) - в 14 (58,3%) случаях, два - в 2 (8,3%), несколько - в 4 (16,7%) случаях и множественные образования, сливающиеся между собой (рис. 2), - в 4 (16,7%) случаях.
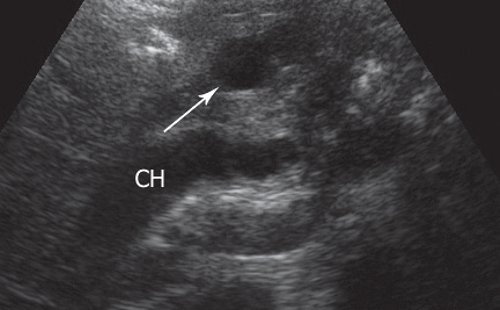
Рис. 1. УЗ-картина единичного кистозного образования в стенке двенадцатиперстной кишки (указано стрелкой).
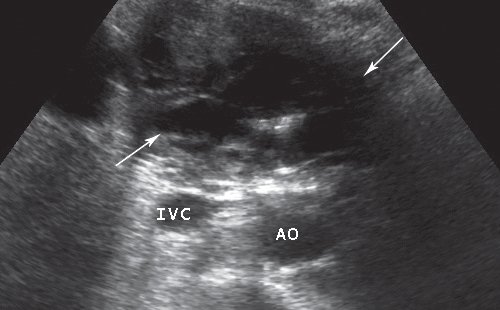
Рис. 2. УЗ-картина множественных кистозных образований двенадцатиперстной кишки, сливающихся между собой (указано стрелками).
В 23 случаях при типичной картине кистозная форма дуоденальной дистрофии развилась на фоне хронического панкреатита: в 12 случаях преимущественно была поражена головка железы, в 4 - головка и тело, в 7 - все отделы железы. При этом у 12 (52,2%) больных течение хронического панкреатита осложнилось формированием постнекротических кист. Панкреатическая гипертензия была диагностирована в 10 (43,5%) случаях (рис. 3), в двух из них имело место кистозное расширение главного панкреатического протока на всем протяжении. В 4 случаях был выявлен хронический калькулезный панкреатит с наличием кальцинатов как в паренхиме железы, так и в просвете главного панкреатического протока (рис. 4).
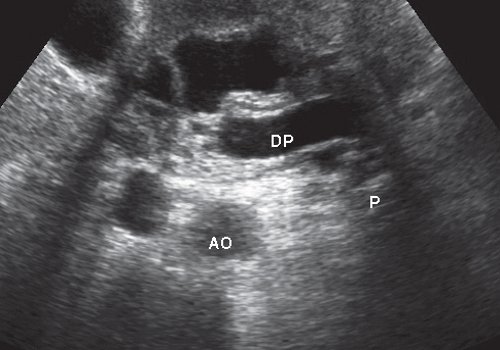
Рис. 3. Изображение кистозного образования в стенке двенадцатиперстной кишки.
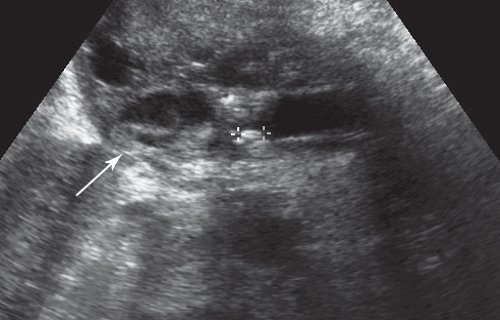
Рис. 4. Изображение кистозного образования в стенке двенадцатиперстной кишки (указано стрелкой). В просвете расширенного главного панкреатического протока визуализируется гиперэхогенный конкремент (отмечен крестиками).
При проведении УЗИ в некоторых случаях для четкой дифференциации и локализации образования нужно непосредственно перед исследованием дать пациенту выпить 200-250 мл жидкости (не заглатывая воздух). При продвижении жидкости из желудка в двенадцатиперстной кишке она как бы "омывает" стенку с образованием и четко локализует его в стенке кишки. При исследовании нисходящей ветви двенадцатиперстной кишки (кишка слабо смещалась относительно головки поджелудочной железы при форсированном дыхании и в режиме четырехмерной реконструкции УЗ-изображения), ее задняя стенка была неравномерно уплотнена, утолщена в пределах от 16,4 до 80 мм. Протяженность выявленных изменений варьировала от 23,2 до 76 мм. Слизистый слой стенки не был изменен, в мышечном слое стенки кишки определялось образование/образования неправильной округлой формы, размерами от 7 мм в диаметре до 27x43,2 мм, толщиной до 25,2 мм, с четкими ровными контурами в тонкой гиперэхогенной капсуле с наличием тонких гиперэхогенных перегородок. При дуплексном сканировании кровотока в капсуле и перегородках образования не было выявлено ни в одном наблюдении.
Во всех наблюдениях при типичной дуоденальной дистрофии желудочнодвенадцатиперстная артерия была смещена кпереди и влево. Артерия при этом определялась справа от выявленного образования.
Развитие описанных выше изменений в поджелудочной железе привело к следующим осложнениям: билиарная гипертензия была выявлена в 7 случаях (рис. 5), портальная гипертензия - в 6 [в одном с формированием выраженной сети венозных коллатералей (рис. 6)], экстравазальная компрессия воротной (рис. 7), селезеночной, верхней брыжеечной и нижней полой вен - в 4, 2, 1 и 1 случае соответственно, тромбоз селезеночной вены - в 1 случае. Увеличение парапанкреатических лимфатических узлов (см. рис. 5) отмечено в 11 (45,8%) случаях.
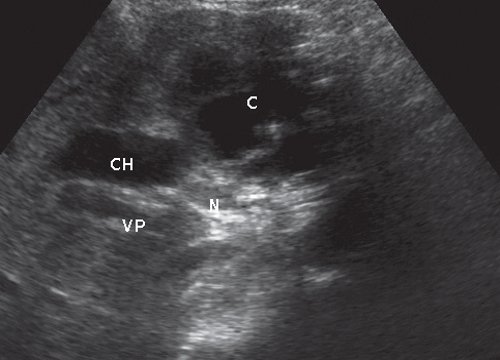
Рис. 5. Изображение кистозного образования (С) в стенке двенадцатиперстной кишки.
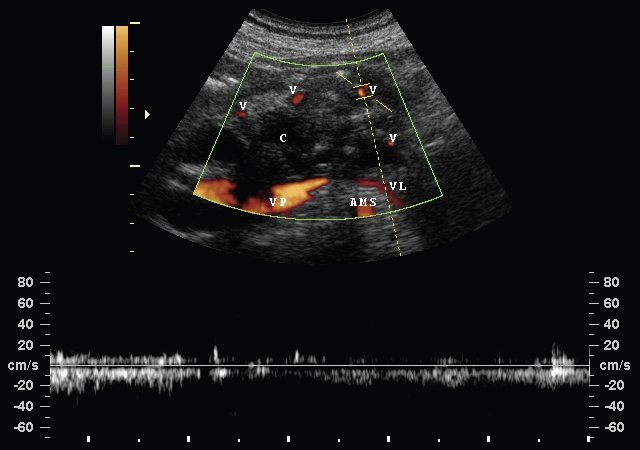
Рис. 6. Дуплексное сканирование кровотока в венозных коллатералях, развившихся вследствие прогрессирования хронического панкреатита.
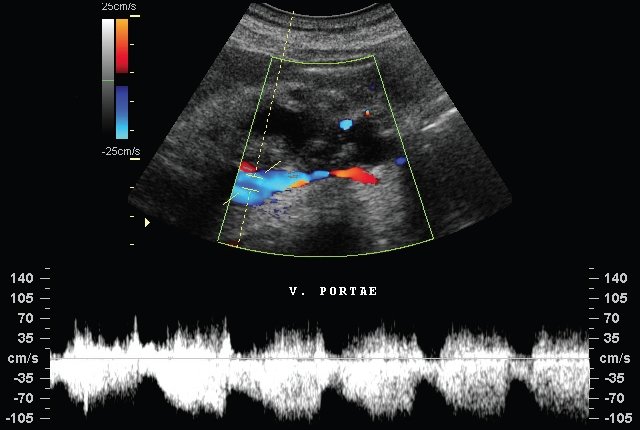
Рис. 7. Экстравазальная компрессия воротной вены (V. PORTAE) при хроническом панкреатите в режиме дуплексного сканирования.
Подобная картина типична для дуоденальной дистрофии. У пациента развивается хронический панкреатит как в орто-, так и в эктопической поджелудочной железы. Последняя вызывает блокаду оттока желчи и панкреатического сока, усугубляя течение хронического воспаления и калькулез протоковой системы и паренхимы ортотопической железы.
В 1 наблюдении был выявлен атипичный случай дуоденальной дистрофии. При УЗИ диагностировали утолщение стенки двенадцатиперстной кишки, в толще которой визуализировалось образование с достаточно четкими ровными контурами, по структуре анэхогенное, неоднородное, с наличием тонких изоэхогенных перегородок. В режиме цветового допплеровского картирования и энергии отраженного допплеровского сигнала данных о наличии кровотока в перегородках не было получено. В поджелудочной железе были поражены только зоны крючковидного отростка и нижней части головки железы (рис. 8), отсутствовали изменения вирсунгова протока, тела, хвоста и части головки поджелудочной железы, а также признаки билиарной гипертензии. Это заставляет думать либо о выраженной изолированной дуоденальной дистрофии с атрофией крючковидного отростка, либо о блокаде эктопированной тканью аномального протока крючковидного отростка в стенке двенадцатиперстной кишки.
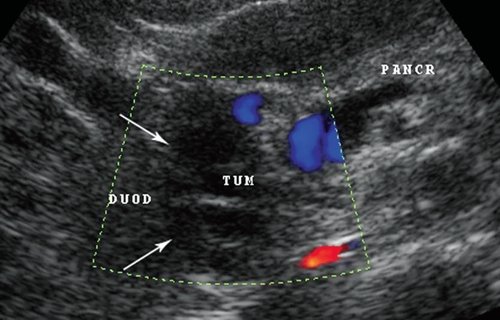
Рис. 8. Изображение кистозного образования (TUM, указано стрелками) в стенке двенадцатиперстной кишки (DUOD) на фоне неизмененной паренхимы поджелудочной железы (PANCR), за исключением крючковидного отростка, в режиме цветового допплеровского картирования.
Все пациенты были оперированы:
- гастропанкреатодуоденальная резекция - в 5 (20,8%) случаях;
- пилоросохраняющая панкреатодуоденальная резекция - в 14 (58,3%) случаях;
- тотальная резекция головки с циркулярной резекцией нисходящей ветви двенадцатиперстной кишки - в 1 (4,2%) случае;
- субтотальная резекция головки поджелудочной железы с сохранением двенадцатиперстной кишки, вскрытием кисты двенадцатиперстной кишки и наложением гастроэнтеро- и энтероэнтероанастомоза - в 1 (4,2%) случае;
- субтотальная резекция головки поджелудочной железы с сохранением двенадцатиперстной кишки и наложением продольного панкреатоэнтероанастомоза на выключенной по Ру петле кишки - в 3 (12,5%) случаях.
При гистологическом исследовании удаленных панкреатодуоденальных комплексов с образованием стенки двенадцатиперстной кишки (рис. 9, а, б; 10, а) в слизистой и подслизистой двенадцатиперстной кишки местами отмечалась лимфоидная инфильтрация. Мышечный слой был утолщен, в нем имелись участки гетеротопии поджелудочной железы в виде ацинусов и протоков (рис. 9, в). Последние были расширены, имели признаки хронического воспаления вокруг. Кроме того, выявлялись кистозные образования, стенки которых на большем протяжении не имели эпителиальной выстилки, а на отдельных участках были выстланы железистым эпителием (рис. 9, г; 10, б). По-видимому, в этих случаях шла речь о расширенных протоках. Ткань поджелудочной железы была с выраженным склерозом, расширенными протоками и признаками хронического воспаления.
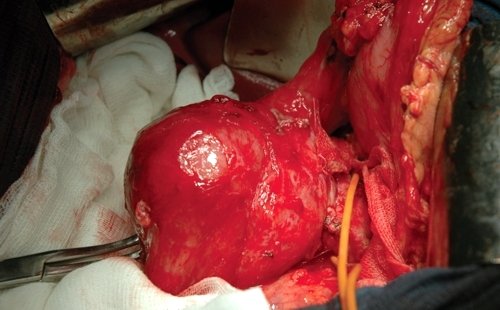
а) Интраоперационный препарат.
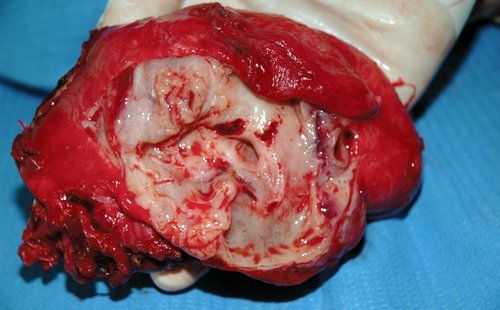
б) Удаленный препарат в разрезе.
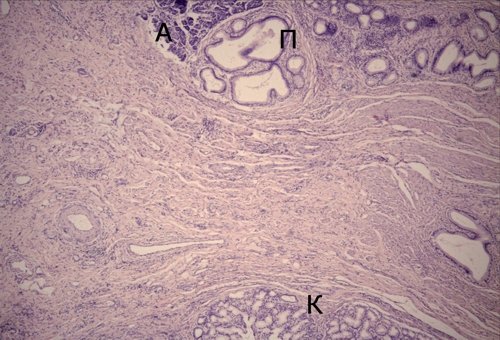
в) Микропрепарат. Гетеротопия ткани (ацинусов - А и протоков - П) поджелудочной железы в двенадцатиперстной кишке (К). Окраска гематоксилином и эозином. Ув. 50.
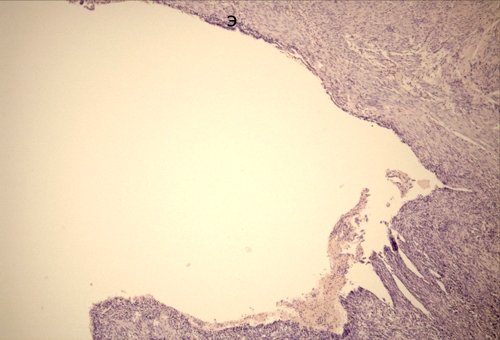
г) Микропрепарат. Расширенный проток с участками сохраненного эпителия (Э) - киста в стенке двенадцатиперстной кишки. Окраска гематоксилином и эозином. Ув. 50.
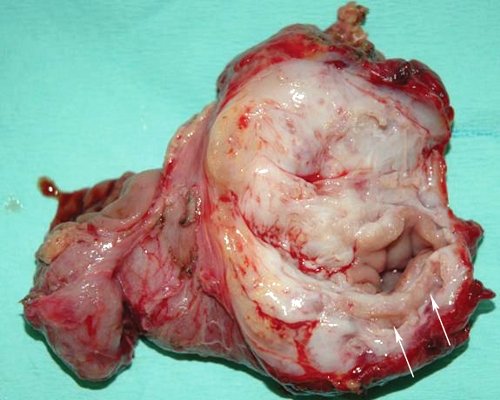
а) Удаленный препарат в разрезе (стрелками указано кистозное образование).
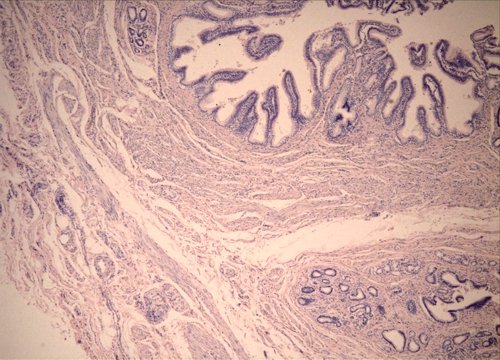
б) Микропрепарат. Кисты в стенке двенадцатиперстной кишки. Окраска гематоксилином и эозином. Ув. 100.
Заключение
Выявление патологических изменений эктопической поджелудочной железы до операции, безусловно, важно, так как наличие эктопической поджелудочной железы позволяет объяснить неэффективность у целого ряда больных хроническим панкреатитом таких операций, как дистальная резекция поджелудочной железы или наложение панкреатодигистивных анастомозов, когда первичный патологический очаг, вызывающий вторичные изменения в железе, оказывается неудаленным. Длительное течение заболевания у большинства наших пациентов связано с тем, что ранее у них не была диагностирована эктопическая поджелудочная железа, вследствие чего тактика лечения не являлась наиболее оптимальной и адекватной.
В нашем исследовании выявление дуоденальной дистрофии в 93,3% наблюдений лучевыми методами исследования до операции обеспечило адекватный выбор лечебной тактики.
Обследование пациентов нужно начинать с УЗИ, которое дает возможность в полном объеме оценить ситуацию и поставить правильный диагноз. УЗ-критериями дуоденальной дистрофии являются утолщение стенки двенадцатиперстной кишки и наличие в ее структуре кистозного образования. При возникновении сложностей в определении локализации образования необходимо непосредственно перед исследованием дать пациенту выпить 200-250 мл жидкости. УЗИ позволяет также диагностировать осложнения, развившиеся вследствие прогрессирования заболевания (билиарная и/или панкреатическая гипертензия, портальная гипертензия с возможным развитием венозных коллатералей), оценить степень экстравазальной компрессии заинтересованных в патологическом процессе сосудов.
Литература
- Dolan R.V., ReMine W.H., Dockerthy M.B. The fate of heterotopic pancreatic tissue. A study of 212 cases // Arch Surg. 1974; 109: 762-765.
- Skandalakis J.E., Grey S.W. Embriology for surgeons: the embryological basis for treatment of congenital anomalies. 2nd ed. Baltimore. Williams Wilkins 1994: 366-387.
- Clarke B.E. Myoepithelial hamartoma of gastrointestinal tract: report of eight cases with comment concerning genesis and nomenclature // Arch. Pathol. 1940; 30: 143.
- Krieg E.G. Heteroptopic pancreatic tissue producing pyloric obstruction: a review and case report // Ann Surg. 1941 Mar; 113(3): 364-370.
- Moen J., Mack E. Small bowel obstruction caused by heterotopic pancreas in an adult // Am Surg 1989; 55: 503-504.
- Skandalakis J.E., Skandalakis L.J., Colborn G.L. Congenital anomalies and variations of the pancreas and pancreatic and extrahepatic bile ducts // In Beger H.G. et al. (ed) The Pancreas, Oxford, Blackwell Science, 1998: 28-30.
- Левкин В.Я. Гетеротопия панкреатической ткани // Вест. хир. им. И.И. Грек. 1982 May. 128(5): 59-61.
- Данилов М.В., Федоров В.Д. Гиперпластические и дизонтогенетические процессы как этиологические факторы хронического панкреатита // Хирургия поджелудочной железы. М.: Медицина. 1995; 44-48.
- Gabata T., Kadoya M., Terayama N. et al. Groove pancreatic carcinomas: radiological and pathological findings // Eur Radiol. 2003 Jul; 13(7): 1679-1684. Epub 2002 Nov 19.
- Galloro G., Napolitano V., Magno L. et al. Diagnosis and therapeutic management of cystic dystrophy of the duodenal wall in heterotopic pancreas. A case report and revision of the literature // JOP. 2008 Nov 3; 9(6): 725-732.
- Pang L.S. Pancreatic heterotopia: a reappraisal and clinicopathologic analysis of 32 cases // South Med J. 1988; 81: 1264-1275.
- Flejou J.F., Potet F., Molas G. et al. Cystic dystrophy of the gastric and duodenal wall developing in heterotopic pancreas: an unrecognized entity // Gut 1993; 34: 343-347.
- Jeng K., Yang K.C., Kuo H. Malignant degeneration of heterotopic pancreas // Gastrointest Endosc 1991; 37: 196-198.
- Potet F., Duclert N. Dystrophie kystique sur pancreas aberrant de la paroi duodenale // Arch. Fr. Mal. App. Dig. 1970; 59: 223.
- Indinnimeo M., Cicchini C., Stazi A. et al. Duodenal pancreatic heterotopy diagnosed by magnetic resonance cholangiopancreatography: report of a case // Surg Today 2001; 31: 928-931.
- Graziani R., Tapparelli M., Malago R. et al. The Various Imaging Aspects of Chronic Pancreatitis // J Pancreas (Online) 2005; 6(Suppl.1): 73-88.
- Armstrong C.P., King P.M., Dixon K.M. The clinical significance of heterotopic pancreas in the gastrointestinal tract // Br J Surg 1981; 68: 384-387.
- Glaser M., Roskar Z., Skalicky M., Krajnc I. Cystic dystrophy of the duodenal wall in a heterotopic pancreas // Wien Klin Wochenschr. 2002 Dec 30; 114(23-24): 1013-1016.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Публикации по теме
- Сочетанное применение ультразвукового исследования и компьютерной томографии в диагностике альвеококкоза печени - Курзанцева О.М.
- Случай ультразвуковой диагностики дивертикулита толстой кишки - Васильченко С.А.
- Возможности ультразвукового исследования в диагностике кистозной формы дуоденальной дистрофии - Степанова Ю.А.
- Особенности ультразвуковой картины у больных циррозом печени с разной степенью активности алкогольного гепатита - Шипов О.Ю.
- Посттравматический панкреатит, осложненный псевдокистой поджелудочной железы - Молчанова О.В.


