Случай ультразвуковой диагностики нефункционирующей нейроэндокринной опухоли поджелудочной железы
Рубрика: Эхография брюшной полости

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Нейроэндокринные опухоли (НЭО) - новообразования, способные синтезировать биологически активные вещества, источником которых являются клетки диффузной эндокринной системы (ДЭС). Последние могут депонировать предшественников биогенных аминов, и синтезировать их наряду с полипептидными гормонами. Генетически клетки ДЭС относятся к клеткам APUD-системы (amine precursor uptake and decarboxilation), поэтому длительное время опухоли из этих клеток назывались "апудомами". В отечественной литературе НЭО поджелудочной железы нередко называются карциноидами [1], в зарубежной литературе под карциноидами подразумевают только "истинные" серотонинпродуцирующиеопухоли [2].
НЭО органов пищеварения по разным статистическим данным, выявляются с частотой 12-15 на 1 млн населения и среди них новообразования поджелудочной железы составляют до 70-80% [3, 4]. НЭО поджелудочной железы, наряду с опухолями легких, бронхов, желудочнокишечного тракта, почек, кожи составляют менее 1% всех злокачественных образований человека [5, 6] и даже крупные клиники редко имеют опыт лечения более 100 таких пациентов [7].
Выделяют функционирующие и нефункционирующие НЭО. В большинстве наблюдений (75-80%) у пациентов с НЭО с клинической симптоматикой могут развиваться тяжелые патологические состояния, обусловленные гормональной активностью этих опухолей, такие как гипогликемия, синдромы Золлингера - Эллисона, Вернера - Моррисона и др. Кроме того, к некоторым из этих синдромов может приводить не только новообразование поджелудочной железы, но и НЭО другой локализации прежде всего желудка и двенадцатиперстной кишки, а также микроаденоматоз с незидиобластозом. Как правило, при наличии клиники заболевания постановка синдромного диагноза у пациентов с НЭО не представляет больших сложностей. Труднее обстоит дело с диагностикой НЭО при отсутствии их активности или при так называемых нефункционирующих опухолях.
Так, в 30-35% наблюдений развитие НЭО не сопровождается развитием гиперфункциональных синдромов, поэтому такие опухоли часто называют нефункционирующими [8]. Термин "нефункционирующие" НЭО весьма условен и отражает лишь отсутствие в клинической картине заболевания специфических симптомов и синдромов. При этом опухолевые клетки могут либо продуцировать функционально инертный гормон, либо вырабатывать его в недостаточных для клинической манифестации количествах, либо продуцировать гормон, не вызывающий специфических симптомов, или возможен нарушенный механизм реализации действия гормонов. К таким опухолям часто относят РР-клеточные, А- и D-клеточные опухоли [8, 9]. Клиническая картина нефункционирующих опухолей поджелудочной железы складывается из неспецифичных симптомов, чаще обусловленных сдавлением окружающих органов и тканей, выраженных меньше, чем при других злокачественных новообразованиях железы. Общее состояние больных долгое время остается относительно удовлетворительным [7, 8, 10]. Синдромы гормональной гиперфункции могут проявляться только на поздних стадиях, когда опухоль достигнет больших размеров или появятся отдаленные метастазы. Поэтому размер выявленных опухолей в среднем составляет 10 см (от 3,5 до 20 см) [11-13]. Анатомическая связь головки поджелудочной железы c общим желчным протоком и двенадцатиперстной кишкой и относительно быстрое вовлечение их в патологический процесс определяют то, что большинство (54%) нефункционирующих НЭО поджелудочной железы диагностируются именно в ее головке [13].
НЭО желудочно-кишечного тракта характеризуются длительным течением и более редким метастазированием, чем типичные аденокарциномы. Обычно высокодифференцированные опухоли диаметром до 2 см являются доброкачественными, опухоли более 3 см относят либо к опухолям с пограничным потенциалом злокачественности, либо к злокачественным. Частота метастазирования карциноидных опухолей коррелирует со степенью дифференцировки и размерами новообразования. При первичной опухоли менее 1 см в диаметре метастазы обнаруживаются только в 2% случаев, при опухоли, размеры которой превышают 2 см - у 90% больных [14].
Основная роль в постановке диагноза, определении распространенности опухолевого процесса и принятии решения о тактике лечения принадлежит инструментальным методам обследования.
Описания случаев успешной ультразвуковой диагностики нефункционирующей нейроэндокринной опухоли поджелудочной железы в ее хвостовом отделе в литературе нам не встретилось. Именно поэтому в настоящем сообщении хотим поделиться своим опытом.
Клиническое наблюдение
Пациенту К., 51 года, впервые в его жизни выполнено УЗИ органов брюшной полости в режиме скрининга. В течение нескольких лет отмечает прибавку в весе и периодический дискомфорт в эпигастральной зоне. Жалоб на момент обследования не было. УЗИ выполнено на цифровом УЗ-сканере экспертного класса Accuvix-XQ (Medison). Размеры печени умеренно увеличены. Паренхима печени, поджелудочной железы повышенной эхогенности, желчные протоки и проток поджелудочной железы не расширены. Желчный пузырь, селезенка, почки - без признаков органической патологии. В верхнем квадранте брюшной полости, в зоне "хвостовой отдел поджелудочной железы - верхний полюс левой почки - ворота селезенки", выявлено дополнительное образование неправильной округлой формы, сниженной эхогенности, с довольно четкими, неровными контурами, с дорсальным псевдоусилением эхо-сигнала, размером 3,0x2,8x2,7 см (объем 11,8 мл). При ЦДК образование определялось как гиповаскулярное. Экстравазальной компрессии магистральных сосудов, признаков их прорастания, а также признаков диффузного перехода на близлежащие ткани не выявлено. Образование лучше визуализировалось в ортостазе (стоя). Заключение: Дополнительное образование в верхнем квадранте брюшной полости неопределенной органной принадлежности, диффузные изменения в паренхиме печени, поджелудочной железы (рис. 1).
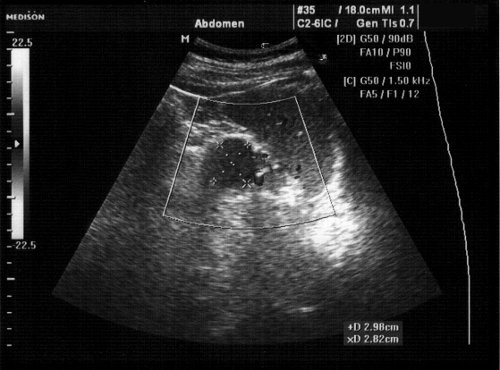
Рис. 1. Дополнительное округлое гипоэхогенное образование в верхнем наружном квадранте брюшной полости в проекции ворот селезенки.
В целях топической диагностики образования была проведена компьютерная томография (КТ) на 32-срезовом компьютерном томографе. На томограммах печень увеличена за счет правой доли, с четкими и ровными контурами, структура ее однородная, внутрипеченочные желчные протоки не расширены. Денситометрические показатели паренхимы снижены до 43-46 HU. Очаговых образований в печени не обнаружено. Воротная и селезеночная вены не расширены. Общий желчный проток обычной ширины - 0,45 см. Желчный пузырь обычных размеров, содержимое его гомогенное. Рентгеноконтрастных конкрементов не выявлено. Форма и размеры головки и тела поджелудочной железы не изменены (толщина головки - 2,9 см; толщина тела - 3,6 см), денситометрические показатели паренхимы не изменены, дольчатость сохранена. На уровне хвоста дольчатость сглажена, толщина его до 3,6 см. В структуре паренхимы железы на этом уровне выявляется дополнительное образование округлой формы, размером 3,3 (вертикальный) x 3,7 (поперечный) x 4,1 (переднезадний) см (объем 26,0 мл). Образование прилежит к наружному контуру левой почки на уровне границы верхней и средней трети. В нативную фазу плотность образования изоденсивна ткани поджелудочной железы (33-35 HU), в артериальную фазу ткань образования активно накапливает контрастное вещество, прослеживается усиление до 74 HU. Контуры его четкие, структура однородная. В паренхиматозную фазу плотность образования изоденсивна ткани железы, в отсроченную фазу прослеживается симптом "вымывания контраста", плотность образования до 52 HU; контурируется четкая капсула до 0,4 см. Вирсунгов проток не расширен. Перипанкреатическая клетчатка однородная. Селезенка не увеличена, однородная по плотности. Метастазы в лимфатические узлы и печень не выявлены. Заключение: КТ-признаки дополнительного гиперваскулярного образования хвоста поджелудочной железы, умеренной гепатомегалии, дистрофических изменений паренхимы печени по типу жирового гепатоза (рис. 2).
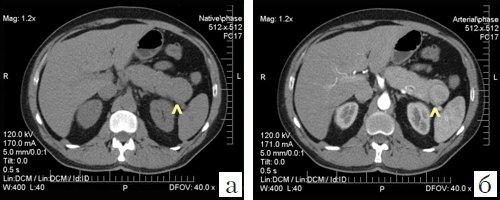
а) Нативное изображение, ткань образования изоденсивна ткани поджелудочной железы.
б) Активное накопление контрастного вещества тканью образования, в большей степени по периферии.
При лабораторной диагностике уровень углеводного антигена в крови (маркер карциномы поджелудочной железы - СА-19-9) составил 10 ЕД/мл (при референсных значениях - меньше 37).
На консультации хирургом было высказано предположение о наличии у пациента нефункционирующей нейроэндокринной опухоли поджелудочной железы и предложено ее оперативное удаление. В связи с отсутствием жалоб, пациент от операции категорически отказался.
Через 2 мес, при повторном УЗИ, размеры опухоли достоверно не изменились (рис. 3). После разъяснительной беседы пациент дал согласие на оперативное лечение.
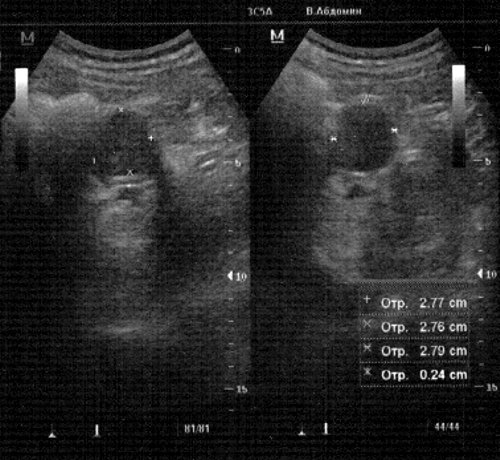
Рис. 3. Дополнительное округлое гипоэхогенное образование в верхнем наружном квадранте брюшной полости в проекции ворот селезенки в двух взаимно перпендикулярных проекциях без признаков динамики.
В хирургическом отделении при осмотре: состояние удовлетворительное. Нормальное телосложение, кожные покровы и видимые слизистые нормальной окраски. В легких дыхание везикулярное, хрипов нет. Тоны сердца ритмичные, шумов не выслушивается. Пульс 80 ударов в минуту, удовлетворительного наполнения, АД 130/90 мм рт. ст. Живот при пальпации мягкий, безболезненный во всех отделах. Симптом Пастернацкого отрицательный с обеих сторон, мочеиспускание не нарушено. При эзофагогастродуоденоскопии выявлена эритематозная (очаговая) гастропатия. Лабораторные исследования (биохимический анализ крови, определение коагулограммы, клинический анализ крови, общий анализ мочи) не выявили диагностически значимых отклонений.
Выбор метода оперативного лечения определялся расположением и размерами опухоли. Была выполнена дистальная резекция поджелудочной железы со спленэктомией.
В патологоанатомическое отделение на исследование единым блоком был прислан материал, представленный резецированной частью поджелудочной железы (длиной 9,0 см) и селезенкой (10,0x6,5x4,0 см). При изучении макропрепарата: капсула поджелудочной железы не напряжена, ткань ее на разрезах серо-желтого цвета, дольчатая. В 5,5 см от края резекции железы и в 2,0 см от селезенки определяется четко очерченный узел в капсуле (5,0x6,0x4,5 см, объем 70,2 мл) мягко-эластичной консистенции, желто-коричневого цвета на разрезах, относительно однородный. Край резекции железы обычного строения, без признаков опухолевого роста. Селезенка синюшно-серая, эластичная, капсула ее тонкая, пульпа темно-вишневого цвета, дает скудный соскоб.
Гистологическое исследование подтвердило нейроэндокринный характер образования. Микроскопически узел в поджелудочной железе представлен опухолевой тканью, построенной из средней величины и крупных клеток с умеренным полиморфизмом ядер, довольно обширным ободком эозинофильной и оптически пустой цитоплазмы, формирующих солидные, альвеолярные, трабекулярные, псевдожелезистые и железистые структуры, в части препаратов - с периваскулярной ориентацией, с большим количеством сосудов капиллярного и синусоидного типа (рис. 4). Митотическая активность очень низкая (0-1 митоз в 10 репрезентативных полях зрения). При окраске по Гримелиусу в цитоплазме опухолевых клеток выявляется нежная гранулярность. Фиброзная капсула опухоли довольно широкая, признаков инвазии опухолевой ткани в капсулу и сосуды не выявлено, некрозы не обнаружены. В окружающей опухоль ткани поджелудочной железы - дистрофические изменения, отек интерстиция. В крае резекции поджелудочной железы опухолевого роста не выявлено. В парапанкреатической клетчатке очаговые кровоизлияния и легкая очаговая лимфоцитарная инфильтрация. В селезенке - неравномерное кровенаполнение красной пульпы, склероз артериол.
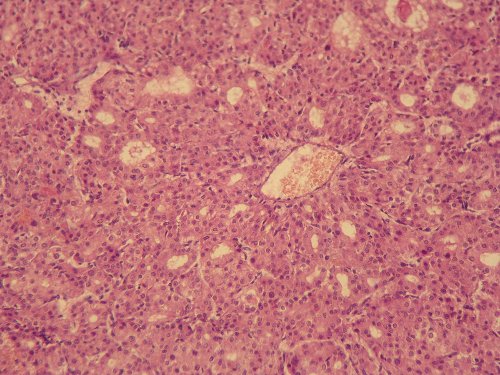
Рис. 4. Патогистологическая картина клеток опухоли поджелудочной железы. Клетки формируют железистые и трабекулярные структуры с периваскулярной ориентацией. Окраска гематоксилином и эозином, x200.
Для верификации нейроэндокринной природы опухоли использовали иммуногистохимические маркеры широкого спектра: антитела к хромогранину А и синаптофизину, а также антитела к гормонам (инсулину, глюкагону, соматостатину, гастрину, панкреатическому полипептиду, серотонину, кальцитонину, адренокортикотропному гормону). Для выявления протоковой дифференцировки опухоли использовали антитела к цитокератинам широкого спектра и селективно к цитокератину 19, карциноэмбриональному антигену, эпителиально-мембранному антигену и к белку р53 (таблица).
| Наименование антител | Результат |
|---|---|
| CD 56 (Clone SPM 128, Spring Bioscience) | + |
| CD 34 (Clone QBEnd 10, Dako) | - |
| Vimentin (Сlone V9, Dako) | - |
| Chromogranin A (Clone LK2H10, BioGenex) | -/+ |
| S 100 (Polyclonal Rabbit Anti-Cow, Dako) | + |
| NSE (Polyclonal Antibody, Spring Bioscience) | + |
| Cytokeratin (Clone MM-1 16, Dako) | +/- |
| Synaptophysin (Clone Snp 88, BioGenex) | -/+ |
| Cytokeratin 8 (Clone С 51, BioGenex) | + |
| ЕМА (Сlone E 29, Diagnostic BioSystems) | -/+ |
| Ki-67 (Clone MIB-1, Dako) | позитивных клеток 0-1 в 10 репрезентативных полях зрения |
Опухолевые клетки экспрессировали CD 56 (Clone SPM 128, Spring Bioscience), S 100 (Polyclonal Rabbit Anti-Cow, Dako) (рис. 5), NSE (Polyclonal Antibody, Spring Bioscience), Cytokeratin 8 (Clone С 51, BioGenex). Около половины клеток экспрессировало панцитокератин [Cytokeratin (Clone MM-1 16, Dako)]. В единичных клетках опухоли экспрессировался Chromogranin A (Clone LK2H10, BioGenex) и Synaptophysin (Clone Snp 88, BioGenex). Маркер пролиферативной активности (Ki-67, Clone MIB-1, Dako) экспрессировался в ядрах 0-1 клеток в 10 репрезентативных полях зрения. Антитело к CD 34 (Clone QBEnd 10, Dako) выявило сеть сосудов капиллярного и синусоидного типа.
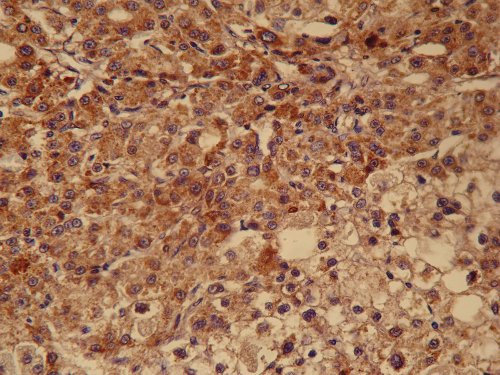
Рис. 5. Иммуногистохимическое исследование удаленной опухоли поджелудочной железы. Клетки опухоли экспрессируют S-100. x400.
Патогистологическое заключение: Гистологическое строение опухоли и иммунофенотип опухолевых клеток (с учетом размера опухоли и низкой митотической активности) соответствуют нефункционирующей нейроэндокринной опухоли поджелудочной железы с неопределенным злокачественным потенциалом.
Послеоперационный период протекал без осложнений. На 24-е сутки пациент в удовлетворительном состоянии выписан под наблюдение онколога.
Обсуждение
Несомненно, что клинически "немые" нефункционирующие НЭО поджелудочной железы, расположенные в хвостовом отделе органа, представляют собой очень сложную для первичной диагностики группу заболеваний.
Однако приведенное наблюдение показывает, что стандартное ультразвуковое обследование, выполненное в режиме скрининга, позволяет обнаружить подобные опухоли именно на стадии "клинического благополучия". Так, выявленная нами бессимптомная "случайная находка" при первом в жизни взрослого пациента УЗИ, расположенная в верхненаружном квадранте брюшной полости, оказалась нефункционирующей нейроэндокринной опухолью поджелудочной железы с неопределенным злокачественным потенциалом. При этом, результаты УЗИ послужили основой для дальнейшего рационального, многостороннего диагностического обследования пациента, позволившего своевременно и результативно провести сложнейшую в техническом исполнении операцию по удалению опухоли на раннем доклиническом этапе.
Отметим, что размеры опухоли при УЗИ составили 16% от истинных (патоморфологических), что, вероятно, может свидетельствовать о полученном эффекте преломления ультразвуковых волн, приводящего к геометрическим искажениям получаемого изображения [15]. Предполагаем, что данный факт имеет важное диагностическое и прогностическое значение при опухолях в описанной области.
Расширение профилактических мероприятий по выявлению заболеваний поджелудочной железы, повышение ответственности врачей не только ультразвуковой диагностики, но и других специальностей, равно как и внимание пациентов к своему здоровью, будет только способствовать улучшению диагностики и прогнозу нефункционирующих НЭО поджелудочной железы, а более детальная оценка данных УЗИ позволит более широко использовать метод в диагностике на доклиническом этапе развития данной патологии.
Выводы
- Нефункционирующие НЭО, расположенные в хвостовом отделе поджелудочной железы, являются редкими формами новообразований и, как правило, характеризуются медленным ростом и бессимптомным течением до момента наступления эффекта сдавления ими окружающих органов и тканей при росте или при появлении метастазов.
- Диагностический алгоритм при выявлении в процессе УЗИ дополнительного образования округлой формы в верхнем наружном квадранте брюшной полости однородной структуры сниженной эхогенности, размерами до 3 см, целесообразно дополнить проведением компьютерной томографии.
- Размеры выявленных при УЗИ нефункционирующих НЭО могут составлять менее 20% от истинных, в связи с физическим эффектом преломления ультразвукового луча.
Литература
- Саввина Т.В. Гистотопографическое исследование поджелудочной железы // Арх. пат. 1979. N11. С. 68-73.
- Creutzfeldt W. Carcinoid Tumors: Development of Our Knowledge // Wld J Surg 1996. V. 20. P. 126-131.
- Eriksson B., Arnberg H., Lindgren P.G. et al. Neuroendocrine pancreatic tumours: clinical presentation, biochemical and histopathological findings in 84 patients // J. Int. Med. 1990. V. 228. P. 103-113.
- Gibril F., Jensen R.T. Somatostatin receptor scintigraphy in the Zollinger - Ellison syndrome // Ann. Int. Med. 1997. V. 126. P. 741-742.
- Benjegard S.A., Flesher N., Allan R.N., Siperstein E. Laparoscopic Radiofrequency Ablation of Neuroendocrine Liver Metastases // Wld J Surg. 2002. V. 26. P. 985-990.
- Capella C., Heitz P.U., Hofler H. et al. Revised Classification of Neuroendocrine tumors of the lung, pancreas and gut // Digestion 1994. V. 55. Suppl 3: P. 11-23.
- Bax N.D.S. Woods H.F., Batchelor A., Jennings M. Clinical manifistations of carcinoid disease // Wld J Surg. 1996. V. 20. P. 142-146.
- Norton J.A., Kivlen M., Li M. et al. Morbidity and mortality of aggressive resection in patients with advanced neuroendocrine tumors // Arch. Surg. 1999. V. 138. N8. P. 859-866.
- Абдулкеримов З.А. "Нефункционирующие" нейроэндокринные опухоли поджелудочной железы: Дисc. ... канд. мед наук. М., 2001.
- Кузин Н.М., Егоров А.В. Нейроэндокринные опухоли поджелудочной железы. М: Медицина, 2001.
- Woods H.F., Batchelor A., Jennings M. Clinical manifistations of carcinoid disease. Wld J Surg. 1996. V. 20: Р. 142-146.
- Кузин Н.М., Егоров А.В, Кондрашин С.А и др. Диагностика и лечение гастринпродуцирующих опухолей поджелудочной железы // Клин. мед. 2002. N 3. С. 71-76.
- Grant C.S. Gastrointestinal endocrine tumours. Insulinoma. Baillieres // Clin. Gastroenterol. 1996. V. 10. N4. P. 645-671.
- Kim D.G., Chejfec G., Prinz R.A. Islet-cell carcinoma of the pancreas // Am Surgeon 1984. V. 55. Р. 325.
- Осипов Л.В. Ультразвуковые диагностические системы: физические принципы и методы. Практическое руководство по ультразвуковой диагностике. Общая ультразвуковая диагностика / Под ред. Митькова В.В. М.: Издательский дом Видар-М. 2003. С. 10. патологии.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Публикации по теме
- Некоторые аспекты диагностики и дифференциальной диагностики механической желтухи - Курзанцева О.М.
- Лучевая диагностика патологии желчного пузыря и желчевыводящих путей - Курзанцева О.М.
- Случай ультразвуковой диагностики нефункционирующей нейроэндокринной опухоли поджелудочной железы - Катерлина И.Р.
- Ультразвуковая диагностика гамартомы селезенки - Степанова Ю.А.
- Лучевая диагностика кистозного рака почки - Курзанцева О.М.


