Возможности эхокардиографического исследования образований атриовентрикулярной борозды
Рубрика: Эхография в кардиологии
УЗ сканер Samsung HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Атриовентрикулярная борозда (АВ-борозда, венечная борозда) - структура на поверхности сердца, отделяющая предсердия от желудочков [1, 2]. Вдоль борозды, как правило, концентрируется эпикардиальный жир [3, 4], также в ней проходят коронарные и лимфатические сосуды, мелкие нервы [2]. Борозда является непрерывной структурой, но для удобства выделяют левую (заднюю) и правую (переднюю) ее части.
В литературных источниках указывается, что при тщательном эхокардиографическом исследовании в АВ-борозде могут быть выявлены разнообразные эхогенные структуры [5]. Эти структуры представляют собой как нормальные анатомические объекты или варианты их строения (расширенный коронарный синус, персистирующая левая верхняя полая вена, липоматозная ткань), так и патологические образования (аневризмы левой огибающей коронарной артерии или нисходящей аорты, опухоли, тромбы, диафрагмальные грыжи) [6-11].
Как правило, области АВ-борозды при стандартном эхокардиографическом исследовании уделяется мало внимания. И образования, выявленные в этой области с использованием ультразвука, должны быть исследованы более подробно с помощью альтернативных методик [12]. Магнитно-резонансная томография (МРТ) и компьютерная томография (КТ) в большинстве случаев позволяют провести полноценную дифференциальную диагностику образований в АВ-борозде, а также определить внесердечные структуры.
Согласно результатам томографических исследований, наиболее часто в венечной борозде обнаруживаются метастатические опухоли сердца [12]. По данным аутопсии метастазы в сердце подтверждены у 10-15% пациентов со злокачественными новообразованиями, причем наиболее распространенными первичными опухолями являются меланома, рак легкого, лимфома и рак молочной железы [13].
Ангиосаркома выступает в качестве наиболее распространенного первичного злокачественного новообразования сердца. В 75% случаев местом возникновения ангиосаркомы является правое предсердие, часто через АВ-борозду происходит ее распространение на свободную стенку правого желудочка [14].
Кардиальные лимфомы могут иметь разнообразные проявления, но общепризнанным является наличие гомогенного инфильтративного образования, покрывающего коронарные артерии и распространяющегося вдоль АВ-борозды. Вторичное поражение сердца у паци- ентов с системной лимфомой обнаруживается у 10% обследованных при аутопсии. Первичная лимфома встречается значительно реже [15].
Параганглиомы правой АВ-борозды представляют собой гиперваскулярную массу с превалирующим кровоснабжением из правой коронарной артерии [16]. Кардиальные или перикардиальные лимфангиомы - это редкие кистозные образования, выявляемые преимущественно у детей. Кардиальные шванномы являются редкими доброкачественными опухолями. Считается, что они происходят из сердечного сплетения или сердечной ветви блуждающего нерва, в связи с чем чаще встречаются в правых отделах сердца.
Также указывается на возможность прямого распространения опухолей легких и средостения в АВ-борозду [12].
Особое внимание уделяется воспалительным и пролиферативным заболеваниям с вовлечением в патологический процесс венечной борозды.
Болезнь Эрдгейма-Честера (БЭЧ) представляет собой нелангенгарсову форму гистиоцитоза, характеризующуюся ксантоматозной инфильтрацией пораженных тканей пенистыми гистиоцитами, окруженными фиброзом. Почти у всех больных отмечаются поражения скелета с симметричным двусторонним метадиафизарным остеосклерозом длинных костей. В 1/3 случаев возможны летальные исходы, связанные с вовлечением сердечно-сосудистой системы. Наиболее частыми кардиальными проявлениями БЭЧ являются: инфильтрация правой АВ-борозды, вовлечение в патологический процесс коронарных артерий, утолщение перикарда, перикардиальный выпот, а также узелковое или объемное утолщение стенки правого предсердия [17]. Диагноз БЭЧ может быть предположен при наличии одного или более из этих признаков, а также при типичных экстракардиальных проявлениях, включая периаортальную и периренальную инфильтрацию и экзофтальм с ретроорбитальным образованием.
При кардиальном саркоидозе существует предрасположенность к инфильтрации АВ-борозды, иногда утолщается межпредсердная перегородка [12].
Аневризмы коронарных артерий могут быть ошибочно приняты за образования АВ-борозды при эхокардиографии (ЭхоКГ), особенно при наличии обильного периферического тромба [6, 12]. Аневризматическая дилатация коронарной артерии может возникнуть на фоне коронарной фистулы, когда аномальное сообщение коронарной артерии с камерой сердца, легочной артерией, коронарным синусом приводит к снижению сосудистого сопротивления, увеличению кровотока и в конечном итоге к расширению пораженной артерии [9]. При этом в большинстве случаев в патологический процесс вовлекается правая коронарная артерия.
За аневризму коронарной артерии или очаговое образование могут быть приняты аневризмы или псевдоаневризмы предсердий или желудочков. Как правило, они возникают в области митрального кольца после митральной аннулопластики, или как осложнение других кардиохирургических вмешательств, или вторично по отношению к инфаркту миокарда, инфекции (чаще всего эндокардит) или травме [18]. МРТ и КТ помогают определить происхождение этих заполненных кровью структур, выступающих в АВ-борозду.
Перикард представляет собой внешнюю границу венечной борозды и, следовательно, перикардиальные поражения приходится дифференцировать с ее объемными образованиями. Лентикулярная хроническая перикардиальная гематома является относительно простым диагнозом при КТ и МРТ, но ее достаточно трудно охарактеризовать с помощью ЭхоКГ [13].
Несмотря на обилие патологических образований, которые могут встретиться при ультразвуковом исследовании (УЗИ) АВ-борозды, в дифференциальной диагностике должны учитываться и нормальные анатомические особенности изучаемой области. Прежде всего, это касается жировых отложений, которые могут выглядеть как объемное образование [19]. В литературе описан случай, когда у пациента с атипичным трепетанием предсердий, ожидающего абляцию, по данным ЭхоКГ была выявлена подвижная структура рядом с придатком левого предсердия, не позволяющая исключить наличие тромба в этой области [11]. Учитывая прогностическую важность находки перед выполнением кардиоверсии или катетерной абляции, а также многообразие анатомических вариантов строения рассматриваемой области, пациенту была выполнена КТ сердца. По данным исследования, выявленная структура представляла собой эпикардиальный жир в поперечном синусе.
В нашей клинической практике было отмечено подобное наблюдение.
Клиническое наблюдение
Пациентка Т., 10 лет, проходила эхокардиографическое обследование амбулаторно по направлению детского кардиолога в связи с частой желудочковой парасистолией (до 20 000 в сутки), диагностированной более трех лет назад.
Жалобы ни обследуемая, ни ее родители не предъявляли. Объективно отмечалась бледно-розовая окраска кожных покровов и слизистых, артериальное давление 110/70 мм рт.ст., пульс 82 уд/мин, удовлетворительных свойств. Аускультативно тоны сердца ясные, ритмичные. При выполненном ранее УЗИ сердца патологических изменений выявлено не было, отмечалось соответствие полостей сердца физическому развитию ребенка, клапанный аппарат без изменений, сократительная способность миокарда левого желудочка в норме.
При проведении стандартной трансторакальной ЭхоКГ с использованием допплеровских методик одновременно в нескольких проекциях у основания задней створки митрального клапана, без четкой связи с клапанным аппаратом, со стороны левого предсердия лоциро- валось гиперэхогенное округлое образование размерами 9,2-9,0-11,8 мм (рис. 1-3).
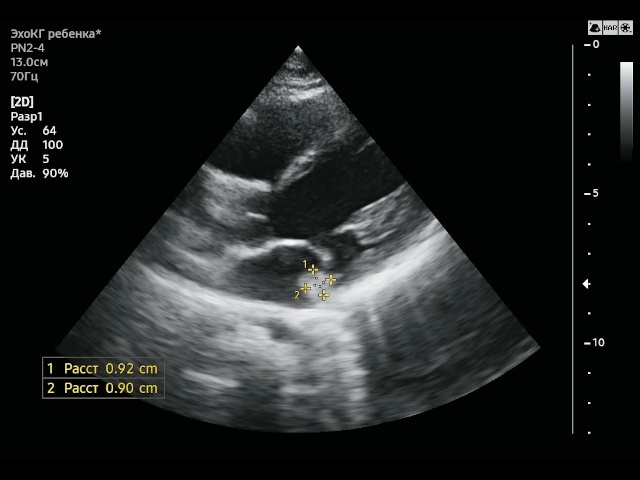
Рис. 1. Образование левой АВ-борозды округлой формы размерами 9,2х9,0 мм. Парастернальная проекция по длинной оси левого желудочка. В-режим.
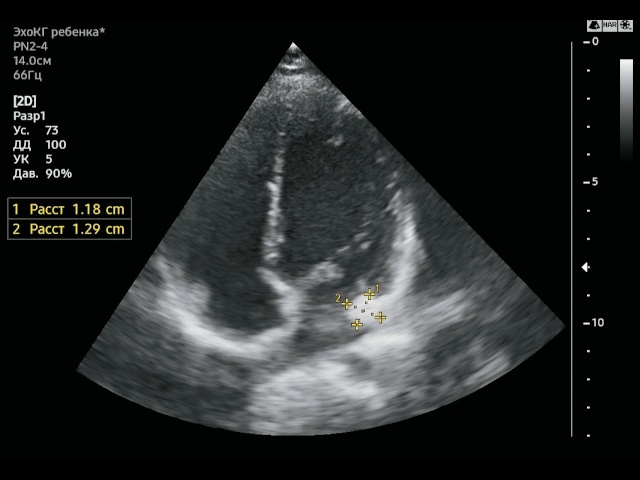
Рис. 2. Образование левой АВ-борозды округлой формы размерами 11,8х12,9 мм. Апикальная четырехкамерная проекция. В-режим.

Рис. 3. Образование левой АВ-борозды округлой формы размерами 9,3х9,7 мм. Апикальная пятикамерная проекция. В-режим.
В связи с регистрацией у ребенка частой желудочковой экстрасистолии, а также объективными трудностями в проведении ультразвуковой дифференциальной диагностики между тромбом левого предсердия и другими образованиями ребенок был направлен на МРТ сердца.
МР-исследование сердца было выполнено по программе HASTE, ТSE, TRUFI, T1-ВИ Т1FS и программе динамического (кино) сканирования в аксиальной, фронтальной и косых плоскостях и в плоскости выводного тракта левого и правого желудочков с толщиной срезов 4-6 мм на фоне и после внутривенного введения гадолинийсодержащего контрастного вещества. Убедительных МР-данных о наличии образования на створках митрального клапана получено не было. Согласно заключению, МР-картина могла соответствовать вялотекущему или персистирующему процессу/ поствоспалительным изменениям миокарда левого желудочка (один основной критерий Lake Louise Criteria Т1/LGE и один дополнительный - наличие жидкости). Выявленное при ЭхоКГ образование, вероятнее всего, соответствовало скоплению жировой ткани в АВ-борозде. Были рекомендованы динамическое наблюдение за образованием, контроль ЭхоКГ 2 раза в год.
Заключение
Таким образом, ЭхоКГ является важным первичным методом исследования в выявлении образований сердца различного генеза. Несмотря на то что для уточнения характера образования может потребоваться более углубленное исследование и привлечение томографических методик, УЗИ сердца незаменимо в качестве неинвазивного и доступного метода оценки сердечных камер, стенок, клапанного аппарата. Нами было показано, что содержимое АВ-борозды может быть визуализировано в парастернальной проекции по длинной оси, в апикальной четырех- и пятикамерной проекции. Важно отметить, что ЭхоКГ может быть широко использована для динамического наблюдения за выявленными изменениями со стороны сердечно-сосудистой системы.
Литература
- Javadikasgari H., Gillinov A. M., Mick S. et al. M. Chapter 21 - Robotic Mitral Valve Surgery // Atlas of Cardiac Surgical Techniques (Second Edition). Elsevier, 2019: 347-363. DOI: 10.1016/b978-0-323-46294-5
- Hargaden M., Singer L. Chapter 20 - Anatomy, Physiology, and Behavior. The Laboratory Rabbit, Guinea Pig, Hamster, and Other Rodents. American College of Laboratory Animal Medicine, Boston: Academic Press, 2012; 1 (1): 575-602. DOI: 10.1016/b978-0-12-380920-9.00020-1
- Antonopoulos A.S., Siasos G., Antoniades Ch., Tousoulis D. (2018-01-01) Chapter 2.1 - Functional Anatomy. Coronary Artery Disease. Academic Press. 2018; 1 (1): 121-126. DOI: 10.1016/b978-0-12-811908-2.00008-8
- Issa Z.F., Miller J.M., Zipes D.P. (2019-01-01). Epicardial Ventricular Tachycardia. Clinical Arrhythmology and Electrophysiology (Third Edition). Philadelphia: Elsevier, 2019; 1 (1): 907-924. DOI: 10.1016/b978-0-323-52356-1.00027-x
- Zuber M., Oechslin E., Jenni R. Echogenic Structures in the Left Atrioventricular Groove: Diagnostic Pitfalls // J Am Soc Echocardiogr. 1998; 11: 381-386. DOI: 10.1016/s0894-7317(98)70107-5
- Aziz K.U., Paul M.H., Bharati S. et al. Echocardiographic features of total anomalous pulmonary venous drainage into the coronary sinus // Am J Cardiol. 1978; 42 (1): 108-113. DOI: 10.1016/0002-9149(78)90993-1
- Snider A.R., Ports T.A., Silverman N.H. Venous anomalies of the coronary sinus: detection by M-mode, two- dimensional and contrast echocardiography // Circulation. 1979; 60: 721-727.
- Fraser R., Dvorkin J., Rossall R., Eidem R. Left superior vena cava: a review of associated congenital heart lesions, catheterization data and roentgenologic findings // Am J Med. 1961; 31: 711. DOI: 10.1016/0002-9343(61)90155-3
- Ryan T.H. Congenital heart disease. 5th ed. Echocardiography. Philadelphia: Lea &Febiger, 1994: 399-401.
- Jakob M., Ritter M., Peter J. Images in cardiovascular medicine: idiopathic hypereosinophilic vasculitis // Circulation. 1995; 91: 2851. DOI: 10.1161/01.CIR.91.11.2851
- Buttinger N., Dooley M., McCready J., Julia J. Epicardial fat pad within the transverse sinus mimicking a left atrial appendage thrombus // Indian Pacing Electrophysiol J. 2021; 21 (3): 174-177. DOI: 10.1016/j.ipej.2021.02.006
- GlocknerJ.F.MagneticResonanceImagingandComputedTomographyofCardiacMassesandPseudomasses in the Atrioventricular Groove // Can Assoc Radiol J. 2018; 69 (1): 78-91. DOI: 10.1016/j.carj.2017.12.004
- Kim E.Y., Choe Y.H., Sung K. et al. Multidetector CT and MR imaging of cardiac tumors // Korean J Radiol. 2009; 10 (2): 164-175. DOI: 10.3348/kjr.2009.10.2.164
- Neragi-Miandoab S., Kim J., Vlahakes G.J. Malignant tumours of the heart: a review of tumour type, diagnosis and therapy // Clin Oncol (R Coll Radiol). 2007; 19 (10): 748-756. DOI: 10.1016/j.clon.2007.06.009
- Hoey E.T., Shahid M., Ganeshan A. et al. MRI assessment of cardiac tumours: part 2, spectrum of appearances of histologically malignant lesions and tumour mimics // Quant Imaging Med Surg. 2014; 4 (6): 489-497. DOI: 10.3978/j.issn.2223-4292.2014.11.25
- Del Forno B., Zingaro C., Di Palma E. et al. Cardiac Paraganglioma Arising From the Right Atrioventricular Groove in a Paraganglioma-Pheochromocytoma Family Syndrome With Evidence of SDHB Gene Mutation: An Unusual Presentation // Ann Thorac Surg. 2016; 102 (3): 215-216. DOI: 10.1016/j.athoracsur.2016.01.072
- Masci P.G., Zampa V., Barison A., Lombardi M. Cardiovascular involvement in Erdheim-Chester disease // Int J Cardiol. 2012; 154 (2): 24-26. DOI: 10.1016/j.ijcard.2011.05.028
- Kasahara H., Beran G., Mohl W. Left ventricular pseudoaneurysm following mitral valve repair // Gen Thorac Cardiovasc Surg. 2009; 57: 221-223. DOI: 10.1007/s11748-008-0364-2
- Silbiger J.J. Echocardiographic examination of the posterior atrioventricular groove // Echocardiography. 2014; 31 (2): 223-233. DOI: 10.1111/echo.12438

УЗ сканер Samsung HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Публикации по теме
- Эхокардиографическая оценка диастолической функции миокарда у детей различных возрастных групп - Салахова А.М.
- Возможности эхокардиографического исследования образований атриовентрикулярной борозды - Салахова А.М.
- Эхокардиография при неотложных состояниях в онкологии - Делягин В.М.
- Коронарные фистулы и шунты с точки зрения локальной гемодинамики. Анатомические и диагностические особенности - Цоколов А.В.
- Особенности эхокардиографической диагностики четырехстворчатого клапана легочной артерии - Салахова А.М.


