Допплеровские исследования при хронических болезнях печени у детей
Рубрика: Эхография в педиатрии
УЗ сканер Samsung HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
Основное применение допплеровского метода при исследовании абдоминальных органов вообще и печени в частности, ограничивается качественной оценкой жидкостных структур, позволяющей дифференцировать кистозные и сосудистые образования, а также определять проходимость сосудов. Информативность количественных показателей, которые могут быть получены при исследовании например портального кровотока, достаточно четко не определены. В связи с этим целью работы было установление ценности допплеровских исследований портального кровотока при хронических болезнях печени и внепечночной форме портальной гипертензии. Оценка кровотока при хронических болезнях печени проводилась у детей с хроническим гепатитом минимальной и выраженной степеней активности, циррозом печени при начальной и сформированной стадиях, и гликогенозе. У основной части больных она проводилась однократно, а у остальных - во время лечения с помощью подсадки фетальных тканей человека.
Материалы и методы
С января 1993 по декабрь 1997 гг. было обследовано более 300 детей в возрасте от 1 года до 16 лет: с внепеченочной формой портальной гипертензии (200), хроническим гепатитом с минимально выраженной активностью (40), выраженной активностью (48), циррозом печени (начальной 52 и сформированной стадиями 55), гликогенозом (27). Кроме этого были обследованы 23 ребенка также с хроническим гепатитом и циррозом печени в процессе терапии, заключающейся в подсадках фетальной ткани человека (ФТЧ). Дети с портальной гипертензией обследовались до проведения оперативного лечения, через 14-20 дн. и 5-6 мес. после него. Пациенты с хроническим гепатитом, циррозом печени и гликогенозом были обследованы однократно. В процессе терапии ФТЧ 23 ребенка с этой патологией были обследованы до подсадки, через 7 дн. и через 6 мес. после каждой подсадки. Максимальное количество подсадок было 4. Таким образом, эти пациенты наблюдались в течение двух лет. Всем детям было проведено допплеровское исследование сосудов портальной системы, когда определяли показатели кровотока по воротной, печеночным и селезеночной венам и печеночной и селезеночной артериям. Кроме этого, у пациентов с анастамозом проводили оценку его проходимости и функционального состояния. Для выяснения характера изменения кровотока в целом у детей с диффузными болезнями печени оценивалась центральная и церебральная гемодинамика. Используемыми показателями для оценки кровотока служили максимальная, средняя и минимальная скорости, индекс резистентности и величина объемного кровотока. Показателями центральной гемодинамики служили ударный и минутный объемы, фракция изгнания и скорость выброса крови в аорту. Все дети с заболеваниями печени проходили клинико-лабораторное исследование, а большинству детей с внепеченочной формой портальной гипертензии было проведено ангиографическое исследование.
Результаты
У всех детей с внепеченочной формой портальной гипертензии до хирургического лечения отмечалось увеличение диаметра селезеночных артерии и вены и увеличение объемного кровотока, несмотря на замедление линейной скорости потока по вене. Величина скорости кровотока по воротной вене у 39% больных снижена, тогда как у остальных она была крайне низкой. У большей части этих пациентов демонстрировались расширенные сосуды в области головки поджелудочной железы, а у 3% диагностировался кровоток по пупочной вене. Направление кровотока по воротной вене у 81% пациентов было обычным, тогда как у остальных оно было гепатофугальным (все эти дети были старшего возраста - от 9 до 11 лет). Индекс резистентности печеночной артерии у детей с нормальной паренхимой печени находился в пределах контрольных показателей (0,7), тогда как у детей с фиброзом он был повышен (0,77-0,86), что было связано с увеличением сопротивления паренхимы печени кровотоку. Та же зависимость наблюдалась в селезеночной артерии - величина индекса находилась в прямой зависимости от степени выраженности изменения в паренхиме.
Сопоставление данных допплеро- и ангиографии показало, что уменьшение показателя скорости кровотока прямо зависит от нарастания давления в портальной системе. Исследование после создания искусственного анастомоза показало его проходимость у всех больных. Через 2-3 недели после портокавального шунтирования наблюдалось еще большее снижение объемного кровотока по воротной вене, его увеличение по селезеночной вене и снижение индекса резистентности в селезеночной и печеночной (у детей с фиброзом) артериях - 0,75±0,02. Данные исследования через 6 мес. показали некоторое снижение кровотока по селезеночной вене и его незначительное возрастание по воротной вене (рис. 1).
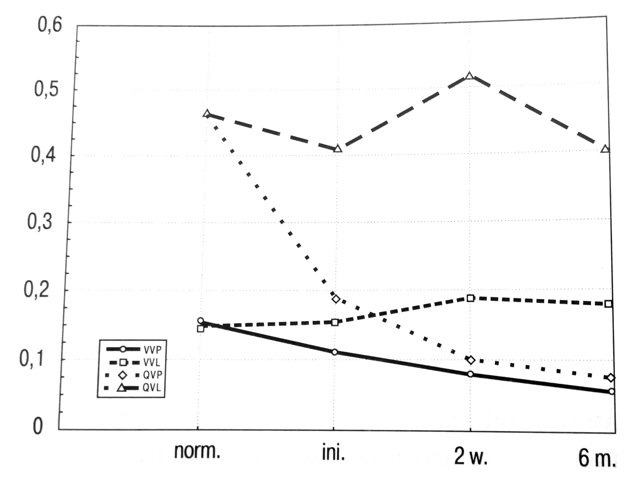
Рис. 1. Скорость и объемный кровоток по воротной и селезеночной венам у детей с внепеченочной портальной гипертензией до и после лечения.
VVL, QVL - скорость, м/сек, и объемный кровоток, л/м, по селезеночной вене;
norm. - нормальные данные;
ini. - исходные данные;
2 w., 6 m. - данные через 2 нед. и 6 мес. после операции.
Оценка кровотока у детей с хроническим гепатитом показала, что уже при минимальной степени активности определяется возрастание объемного кровотока по воротной и печеночным венам, причем за счет увеличения его скорости. Кровоток в селезенке оставался на нормальном уровне. По мере прогрессирования процесса линейная скорость потока замедлялась, но увеличение диаметра воротной вены приводило к нарастанию объемного кровотока. То же самое наблюдалось и в селезеночной вене (рис. 2). Кроме этого, увеличивалась и ригидность печеночной и селезеночной артерий. Показатели центральной и периферической гемодинамики практически не менялись.
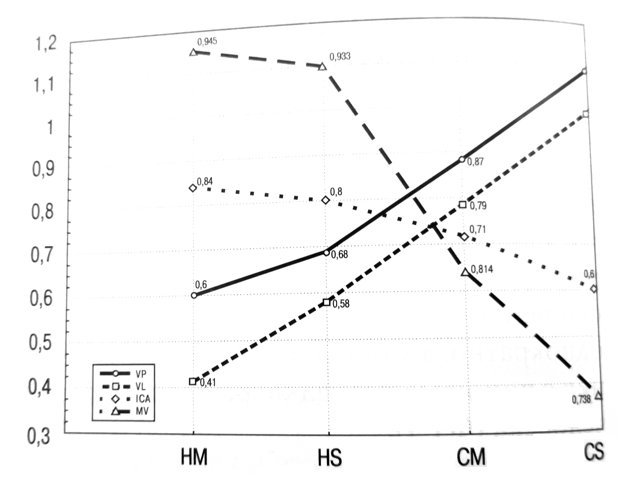
Рис. 2. Объемный кровоток, л/м, по воротной (VP), селезеночной (VL) венам, внутренней сонной артерии (ICA) и минутный объем крови (MV) у детей с хроническими болезнями печени.
CM, CS - цирроз печени начальной и сформированной стадий.
Наиболее выраженные изменения в портальном кровотоке имели место при циррозе печени, когда уже в начальной стадии наблюдали высокий объемный кровоток по воротной вене и печеночной артерии, что указывало на увеличение кровоснабжения печени, при этом объем крови по печеночным венам, выводящим кровь из печени, был также выше нормы, но достоверно ниже притекающего. Показатели центральной гемодинамики: минутный, ударный объемы, фракция изгнания были достоверно уменьшены (см. рис. 2), а церебральной - демонстрировали тенденцию к дефициту кровотока. Возможно, увеличение объема кровотока в портальной системе было связано с депонированием крови в печени, благодаря увеличению емкости ее сосудов.
По мере прогрессирования цирроза в сформированной стадии показатели объемного кровотока несколько увеличивались, как и индекс резистентности печеночной артерии (0,78±0,03), что говорило о возрастании периферического сопротивления паренхимы печени, на что косвенно указывала и линейная форма допплеровской кривой, полученная при оценке кровотока по печеночным артериям. Параллельно наблюдалось снижение объема крови, поступаемой в головной мозг, а также ударного и минутного объемов (см. рис. 2). Показатели портальной гемодинамики, полученные при исследовании детей с гликогенозом, находились в пределах контрольных цифр.
Анализ показателей кровотока, определенных при динамическом исследовании больных с хроническим гепатитом и циррозом печени, в процессе терапии с помощью подсадок фетальных тканей человека показал, что сразу после подсадки наблюдается увеличение скорости и объемного кровотока по воротной и селезеночной венам (на фоне снижения диаметра сосудов), а также снижение пульсового индекса печеночной и селезеночной артерий. Однако результаты исследования перед второй подсадкой показали практический возврат этих данных к исходному уровню. Дальнейшая оценка гемодинамических параметров продемонстрировала такую же тенденцию - увеличение кровотока сразу после подсадки и дальнейшее его уменьшение через 5-6 мес.
Конечные показатели, полученные через полгода после четвертой подсадки, т. е. примерно через 2 года после начала лечения, были несколько выше исходных данных, но эта разница статистически недостоверна. Характер изменения результатов гемодинамических показателей полностью соответствовал данным клинико-лабораторных исследований. При оценке контрольной группы детей с той же патологией, но находящихся на традиционном лечении, достоверных изменений показателей портальной гемодинамики по сравнению с исходными вообще не было (рис. 3).
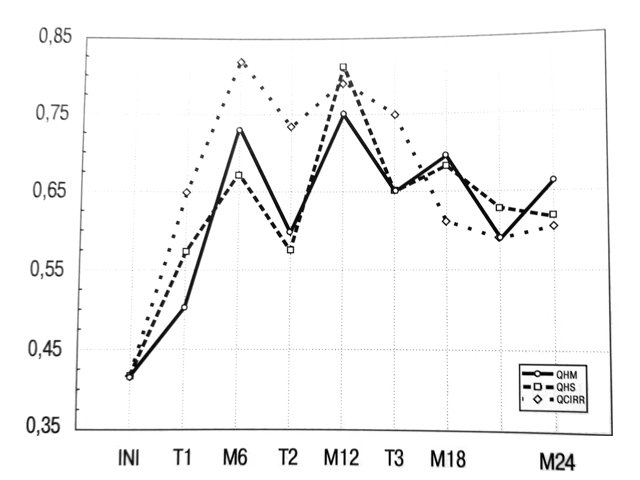
Рис. 3. Объемный кровоток, л/м, по воротной вене у детей с хроническими болезнями печени на фоне лечения фетальной ткани человека.
QCIRR - кровоток при циррозе печени;
Т1, Т2, Т3, Т4 - номера подсадок;
М6, М12, М18, М24 - каждые 6 мес. после подсадки.
Обсуждение
Анализ данных кровотока в портальной системе у детей с внепеченочной портальной гипертензией позволил выделить три типа его нарушения: 1 - с сохраненным естественным, но сниженным венозным оттоком от селезенки к печени; 2 - когда определялся кровоток только по селезеночной вене; 3 - отсутствие кровотока по воротной вене сочеталось с развитием коллатералей. При 2 и 3 типах кровотока имело место повышение резистентности селезеночной артерии. Эти наблюдения позволили сделать вывод, что у детей с внепеченочной портальной гипертензией под воздействием увеличенного портального давления происходят гемодинамические изменения в венозных и артериальных сосудах, приводящие к гипердинамическому типу циркуляции. В результате происходит развитие портосистемных коллатералей, которые, не нормализуя давление в портальной системе, приводят в внутрижелудочному кровотечению [1, 2]. Усиление гемодинамических отклонений, наблюдавшихся у более старших детей, не позволяет рассчитывать на улучшение перфузии печени портальной кровью с возрастом ребенка даже при наиболее легком течении болезни. Увеличение пульсового индекса в селезеночной артерии указывало на возрастание сосудистого сопротивления в селезенке, причиной которого могли быть наличие склеротических изменений в паренхиме органа и портальная гипертензия. Анализ результатов допплерографии после портокавального шунтирования показал проходимость шунтов во всех случаях. Сопоставление данных объемного кровотока с диаметром шунта позволил прийти к выводу, что наиболее адекватную декомпрессию портальной системы обеспечивали анастомозы, имеющие диметр от 8,5 до 10,4 мм (в среднем 9,38±0,55 мм). Оценка данных гемодинамики по сосудам после проведенной операции показала улучшение перфузии селезенки и изменение ее характера в печени, но основные гемодинамические закономерности все же сохранялись, поскольку не наблюдалось полной компенсации портального кровообращения и сокращения его объема. Повторные исследования, проведенные через 6 мес. после операции, выявили сокращение объемного кровотока в портальной системе (снижение объемного кровотока по селезеночным артерии и вене и через шунт), наиболее выраженное у детей в возрасте 5-8 лет. Отсутствие признаков портальной гипертензии позволило связать эти изменения с закрытием артериовенозных фистул. Результаты гемодинамического исследования у детей с хроническими болезнями печени показали, что наиболее ранние отклонения начинают проявляться уже при хроническом гепатите с минимальной степенью активности и постепенным их нарастанием по мере тяжести патологического процесса. При этом наиболее выраженные нарушения в гемодинамике развиваются при начальной стадии цирроза печени, усугубляясь при сформированной, когда увеличивается объем крови в печени, где, по всей вероятности, она депонируется. Это предположение подтверждается демонстрацией увеличенного объемного кровотока через чревный ствол, воротную вену, отчасти печеночные вены, его незначительным увеличением в селезеночной артерии, снижением ударного и минутного объемов, показателя фракции изгнания и объемного кровотока по сосудам шеи. Последний при начальной стадии цирроза почти не страдает, но при сформированной - развивается уже его значительный дефицит. По-видимому имеется недостаток кровенаполнения и в почках, что вызывает спазм почечных сосудов у пациентов с циррозом печени [3]. Можно предположить, что значительное увеличение печеночного кровообращения связано с депонированием крови в расширенных сосудах портальной системы и открытием порто-кавальных фистул.
Увеличение объемного кровотока в селезенке указывает на развитие гиперкинетического типа циркуляции, как и у взрослого контингента больных [4, 5], и являющегося признаком портальной гипертензии. Нормальные показатели кровотока в сосудах портальной системы у детей с гликогенозом подтверждают, что основной причиной, определяющей его изменение, является разрастание соединительной ткани в печени, а не накопление гликогена или жира в гепатоцитах. В качестве объективной оценки состояния печени в процессе терапии с помощью подсадки фетальных тканей человека были использованы, кроме обычных клинико-лабораторных методов, эхо- и допплерографические методы исследования.
В результате было определено, что сразу после подсадки происходило сокращение размеров печени и селезенки и улучшение перфузии этих органов. Однако через 5-6 мес. все показатели практически возвращались к исходному уровню, чтобы затем снова положительно измениться после следующей подсадки. В результате после 4-5-й подсадки имело место незначительное улучшение кровоснабжения органов и сокращение их размеров. Сравнение этих же показателей с полученными при исследовании пациентов с той же патологией печени, но находившихся на традиционном лечении, продемонстрировало несколько лучший эффект при использовании фетальных тканей.
Выводы
В статье продемонстрированы три возможности использования допплерографии при патологии печени и ее сосудов. Можно сделать следующие выводы: метод допплерографии должен обязательно использоваться при оценке сосудов до и после шунтирующих операций; использование метода для оценки кровотока в портальной системе при хронических болезнях печени не имеет большого практического смысла; метод может быть использован для количественной оценки кровотока при динамических исследованиях в процессе терапии, что позволяет косвенно оценить эффективность проводимой терапии.
Литература
- Grossman R., Colombato A. Gastric vascular changes portal hypertension. Hepatology, 1988,6: 1708-1710
- Ralls P. Color Doppler sonography of the hepatic artery and portal venous system. Am.J.Roentgenol., 1990, 155:517-525.
- Platt J., Ellis J., Rubin J. et al. Renal duplex Doppler ultrasonography: a noninvasive predictor of kidney dysfunction and hepatorenal failure in liver diseases. Hepatology, 1994, 2; 362-369.
- Ohnishi K. ,Sato S., Pugliese D. et.al. Changes of splanchnic circulation with progression of chronic liver disease studied by echo-doppler flowmetry. AmJ.Gastroent., 1987, 82:507-511.
- Sato S., Ohnishi K., Sugita S., Okuda K. Splenic artery and superior mesenteric artery blood flow. Nonsurgical doppler as measurement in healthy subjects and patients with chronic liver diseases. Radiology, 1987, 164: 347-352.

УЗ сканер Samsung HS40
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Публикации по теме
- Возможности ультразвуковых исследований при портальной гипертензии у детей - Дворяковский И.В.
- Ультразвуковая характеристика скелетных мышц при хроническом гломерулонефрите у детей - Дворяковский И.В.
- Допплеровские исследования при хронических болезнях печени у детей - Дворяковский И.В.
- Дуплексное допплеровское сканирование почек у детей - Ольхова Е.Б.
- Случай тромбоза правого предсердия у грудного ребенка - Черпакова О.Г.


