Цветовое дуплексное сканирование после шунтирующих операций на артериях нижних конечностей
Рубрика: Эхография в кардиологии

УЗ сканер Samsung HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Современные клинические рекомендации по диагностике и лечению стеноокклюзирующих заболеваний аорты и артерий нижних конечностей рассматривают цветовое дуплексное сканирование в качестве эффективного метода в оценке характера, локализации, протяженности и степени поражения в каждом сегменте артериального русла (класс показаний I, уровень доказательности В) [1-4]. При динамическом наблюдении пациентов, перенесших операцию шунтирования на артериях нижних конечностей, ультразвуковое исследование сосудов является методом выбора для диагностики стеноза шунта и осложнений реконструктивных операций [5]. Многочисленные исследования показали, что без превентивного хирургического вмешательства риск тромбоза стенозированного шунта составляет около 25% [6-8], а регулярное наблюдение с помощью дуплексного сканирования позволяет уточнять или определять показания к превентивным вмешательствам, включая ангиопластику или замену фрагмента шунтирующего сосуда [4].
Виды шунтирующих операций
Операции шунтирования, в зависимости от уровня наложения проксимального (центрального) и дистального анастомозов, подразделяют на аорто-бедренное (аорто-бифеморальное) шунтирование, подвздошно-бедренное, бедренно-подколенное (выше или ниже щели коленного сустава), бедренно-заднебольшеберцовое шунтирование и др. В качестве шунтирующего сосуда (трансплантанта) может быть использована аутовена и протезы (синтетические или биологические), которые анастомозируются с артериями по типу "конец в конец" (рис. 1, 2) или "конец в бок" (рис. 3-5) [9,10].
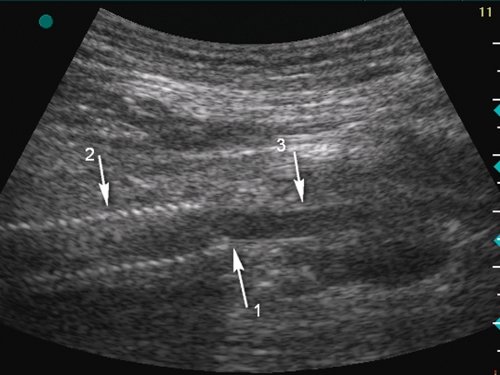
Продольное сечение, стрелка 1 - место соединения синтетического протеза из дакрона (стрелка 2) и биологического протеза (внутренняя грудная артерия быка, стрелка 3). Локализация промежуточного анастомоза - выше уровня щели коленного сустава (уровень верхнего края надколенника).
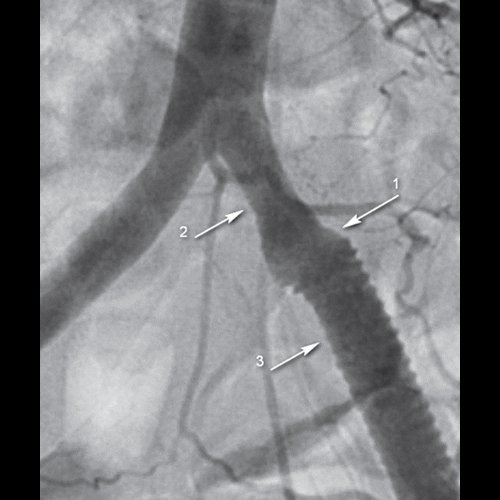
а) Ангиограмма. Продольное сечение, стрелка 1 - место соединения общей подвздошной артерии (стрелка 2) с протезом (стрелка 3).
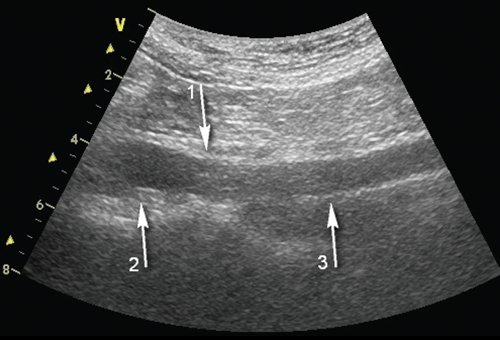
б) Эхограмма. Продольное сечение, стрелка 1 - место соединения общей подвздошной артерии (стрелка 2) с протезом (стрелка 3).
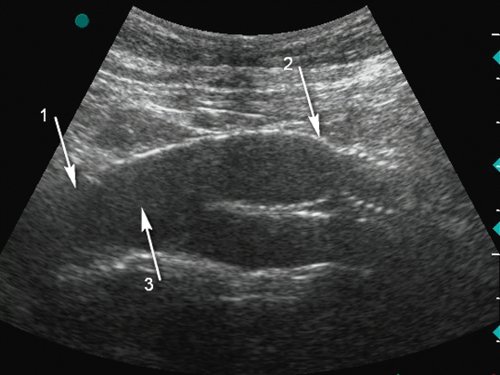
Продольное сечение, стрелка 1 - аорта, стрелка 2 - протез, стрелка 3 - просвет между аортой и протезом.
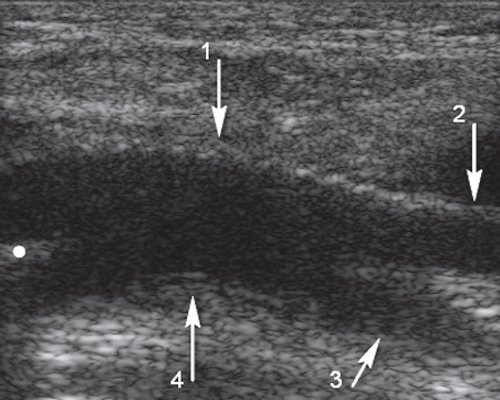
а) Продольное сечение на уровне дистального анастомоза. Стрелка 1 - стенка синтетического протеза, стрелка 2 - сегмент поверхностной бедренной артерии, стрелка 3 - сегмент глубокой бедренной артерии, стрелка 4 - задняя стенка общей бедренной артерии.
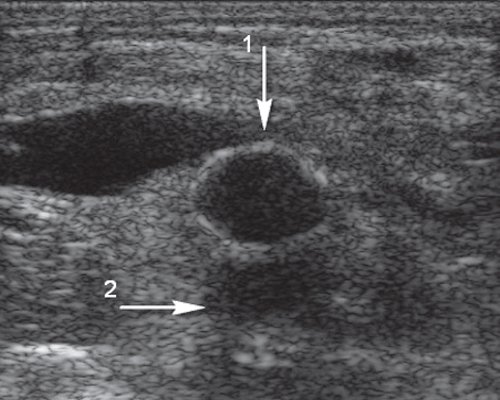
б) Поперечное сечение на 3-5 мм выше уровня дистального анастомоза (уровень поперечного сечения показан точкой на рисунке "а"). Стрелка 1 - протез, стрелка 2 - общая бедренная артерия.
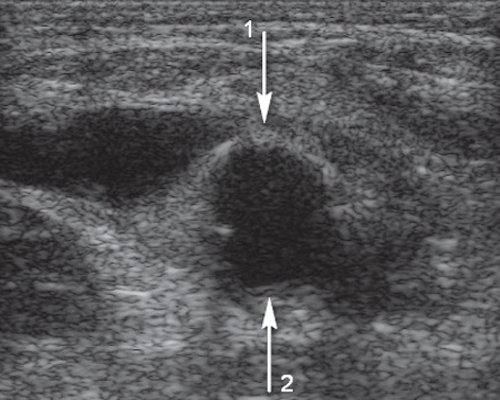
в) Поперечное сечение на уровне дистального анастомоза. Стрелка 1 - передняя стенка протеза, стрелка 2 - задняя стенка общей бедренной артерии.
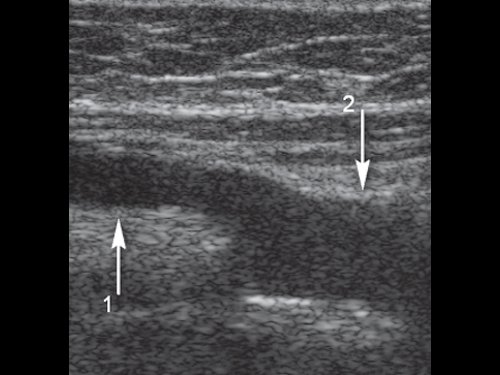
Продольное сечение. Стрелка 1 - аутовена, стрелка 2 - подколенная артерия.
При реконструктивных операциях на артериях бедренно-подколенного и берцового сегментов аутовенозное шунтирование (в позиции in situ или реверсированной большой подкожной веной) характеризуется меньшей частотой тромбоза шунта в отдаленном периоде по сравнению с шунтированием протезом [4, 11-12] (рис. 5-7).
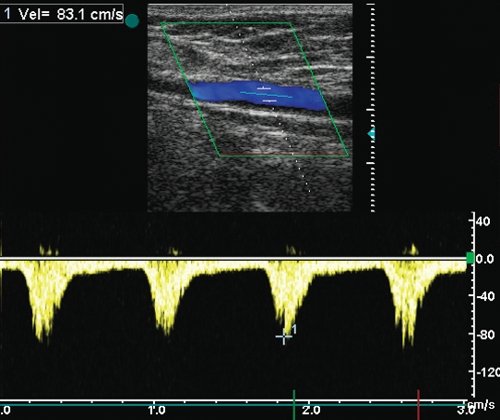
а) Допплерограмма кровотока из шунта на 3-5 см выше зоны стеноза (Vps - 83 см/с).
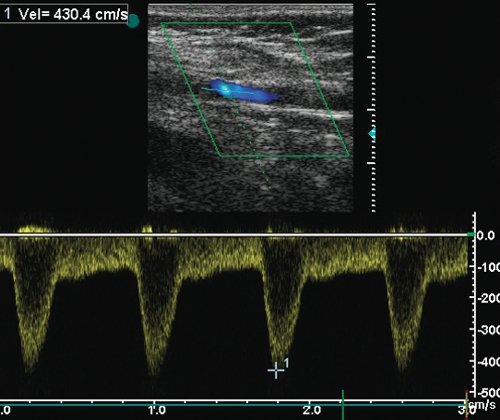
б) Допплерограмма кровотока из зоны стеноза (Vps - 430 см/с).
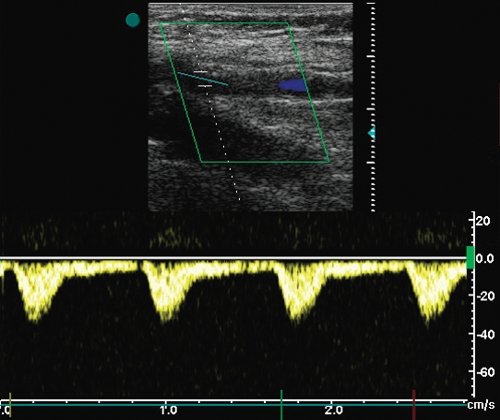
в) Допплерограмма кровотока на 8-10 см дистальнее зоны стеноза (Vps - 35 см/с).
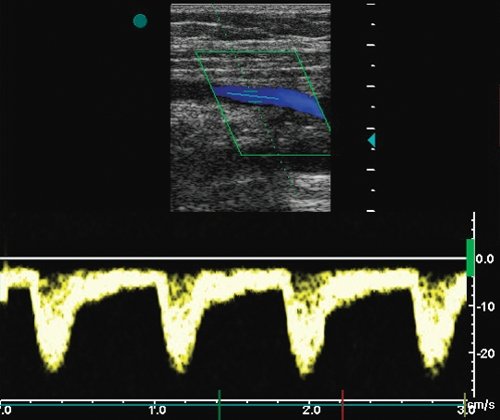
г) Допплерограмма кровотока из шунта на 2-3 см выше уровня дистального анастомоза (Vps - 25 см/с).
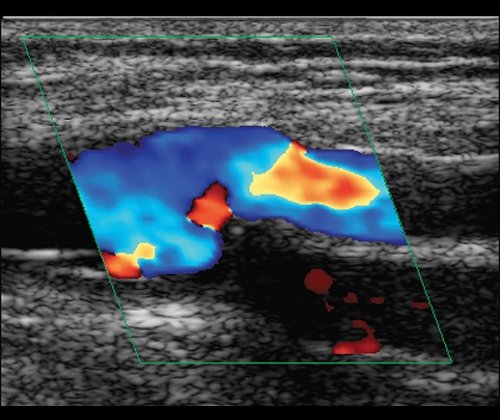
а) Область проксимального анастомоза, продольное сечение, отсутствует дефект наполнения в режиме ЦДК.
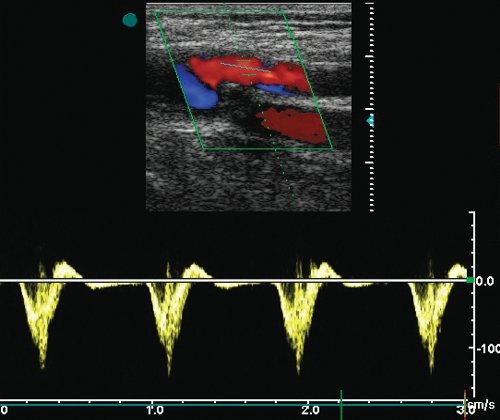
б) Допплерограмма кровотока из зоны проксимального анастомоза (Vps - 125 см/с).
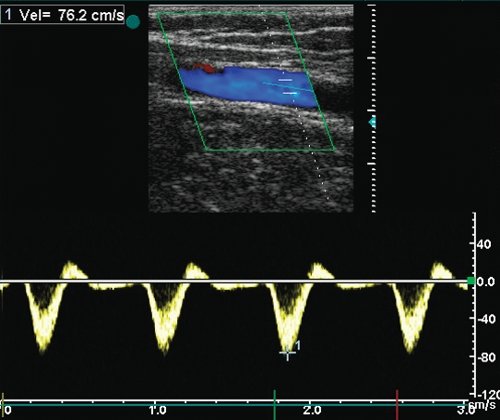
в) Допплерограмма кровотока из средней 1/3 шунта (Vps - 76 см/с).
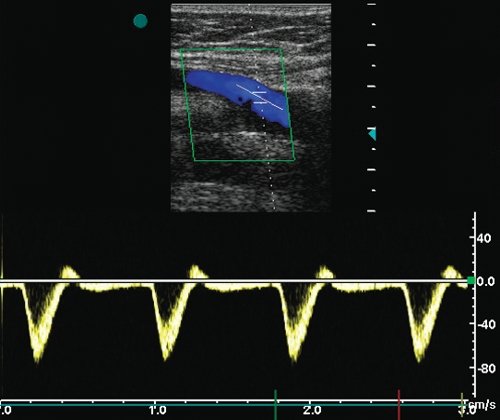
г) Допплерограмма кровотока из шунта на 2-3 см выше уровня дистального анастомоза (Vps - 80 см/с).
Самым длительным эффектом обладают аорто-бедренные шунты [13-14]. При аорто-бедренном шунтировании используют синтетические протезы, материал которых может быть представлен фторлавсаном или дакроном с ребристой структурой (см. рис. 2-4), политетрафторэтиленом или полиуретаном [4, 10] с гладкой внутренней поверхностью (рис. 8).
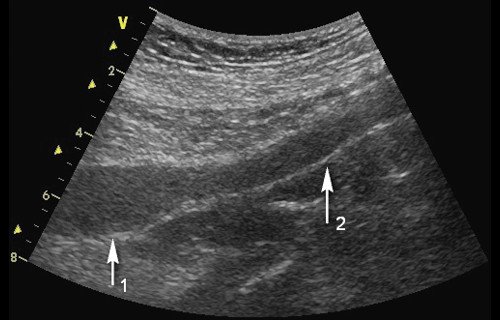
Стрелка 1 - аорта, стрелка 2 - протез.
В ряде исследований показана высокая эффективность операций с применением биологических протезов [15-16], которые представляют собой специально обработанную пупочную вену или сосуды животных (крупного рогатого скота, свиней). Биологические протезы не отличаются по своей структуре от нативной артерии или вены (рис. 9). Однако биологические протезы, по сравнению с аутовенозными и синтетическими, в большей степени могут быть подвергнуты аневризматическому расширению и последующему тромбообразованию (рис. 10).
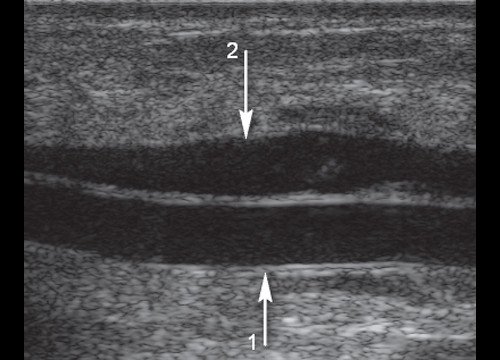
Стрелка 1 - биологический протез, стрелка 2 - анэхогенное жидкостное образование (экссудат) в парапротезном пространстве, косвенный признак воспаления.
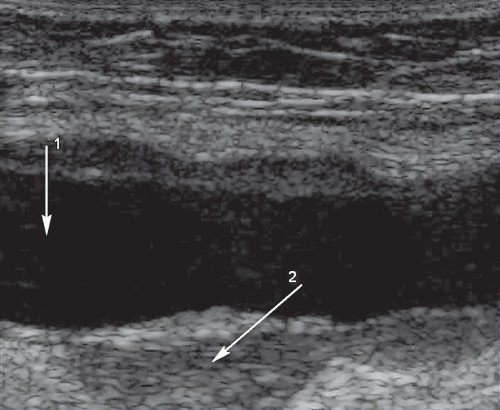
Показана средняя 1/3 бедренно-подколенного шунта, протез неравномерно расширен. Стрелка 1 - функционирующий просвет протеза, стрелка 2 - тромбомассы на уровне максимального аневризматического расширения.
В некоторых случаях в качестве шунтирующего сосуда используют комбинацию протезов (синтетический протез соединяется с аутовеной или соединяют между собой синтетический и биологический протезы) (см. рис. 1). Если реконструкция бедренно-подколенного сегмента выполняется после коррекции поражения аортоподвздошного сегмента, то лучшие результаты наблюдаются при формировании анастомоза с браншей протеза в области дистального анастомоза [4].
Периодичность дуплексного сканирования
Пациенты, перенесшие аутовенозное шунтирование, должны быть периодически (по крайней мере в течение первых 2 лет после операции) обследованы методом дуплексного сканирования с измерением пиковой систолической скорости кровотока (Vps) и расчетом соотношения скоростей кровотока на протяжении всей длины шунта (класс показаний I, уровень доказательности С) [4]. Обследование методом дуплексного сканирования рекомендуется в первый месяц от момента хирургического вмешательства. В том случае, если стеноз аутовенозного шунта не выявляется в первый месяц (примерно 80% шунтов), рекомендуется наблюдение с 6-месячным интервалом в течение первого года, а затем, по истечении первого года после аутовенозного шунтирования, ежегодно [10, 17]. Наблюдение за протезными реконструкциями, как и после аутовенозных реконструкций, рекомендуется с 6-месячным интервалом [17]. Однако в одной из ключевых клинических рекомендаций - Trans-Atlantic Inter-Society Consensus (TASC II) отмечается необходимость только регулярного клинического обследования и измерения плечелодыжечного индекса давления [18].
Основные задачи дуплексного сканирования
В связи с тем, что тромбоз шунта сопровождается низкой вероятностью сохранения конечностей, первостепенными задачами динамического ультразвукового исследования сосудов после шунтирующих операций являются обнаружение ультразвуковых признаков повышенного риска развития тромбоза шунта и ранняя диагностика тромбоза шунта.
Диагностика тромбоза шунта не вызывает затруднений. Заключение о тромбозе делается на основании обнаружения структур в просвете шунта в В-режиме, при отсутствии кровотока в шунте по данным цветового и импульсно-волнового допплеровских режимов (рис. 10, 11), а также на основании характеристик кровотока ниже области дистального анастомоза.
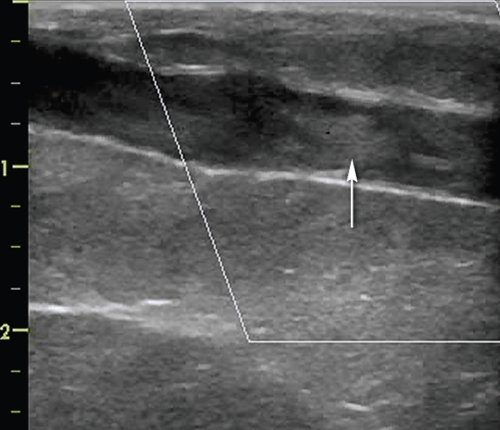
а) Средняя 1/3 бедренно-подколенного аутовенозного шунта. В просвете шунта визуализируются гетерогенные, преимущественно гиперэхогенные структуры (стрелка), кровоток в режиме ЦДК не регистрируется.
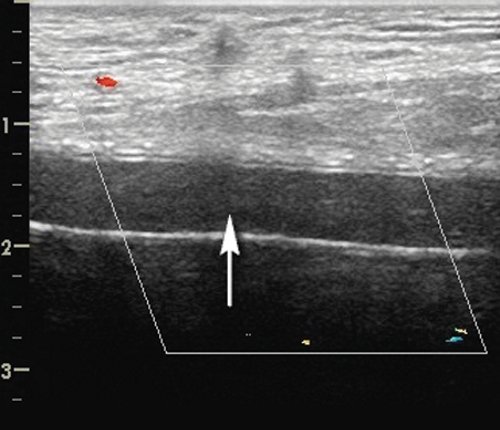
б) Бедренно-подколенное шунтирование протезом из политетрафторэтилена. Средняя 1/3 протеза, анэхогенные структуры в протезе (стрелка), кровоток в режиме ЦДК не регистрируется.
Обнаруженные при ультразвуковом исследовании косвенные признаки воспаления (экссудата) в проекции протеза и инфицирования протеза (см. рис. 9) являются неблагоприятными прогностическими факторами, сопровождающимися высоким риском тромбоза шунта в раннем послеоперационном периоде.
Наиболее значимыми и распространенными предвестниками тромбоза шунта являются стенозы центрального и/или дистального анастомозов, стенозы шунтов вне зон анастомозов, а также снижение скоростных показателей кровотока по шунту [10] (рис. 6, 12, 13). Детально изучена роль дуплексного сканирования после операций аутовенозного шунтирования. Установлено, что около 20% инфраингвинальных аутовенозных шунтов имеют остаточный послеоперационный стеноз или стеноз развивается в течение первого года после реконструкции [6, 10]. Стенозы локализуются как в области анастомозов, так и в любом другом сегменте шунта. Для искусственных или биологических протезов стенотическое поражение протеза вне зон анастомозов менее характерно по сравнению с аутовенозными шунтами [10] (см. рис. 6).
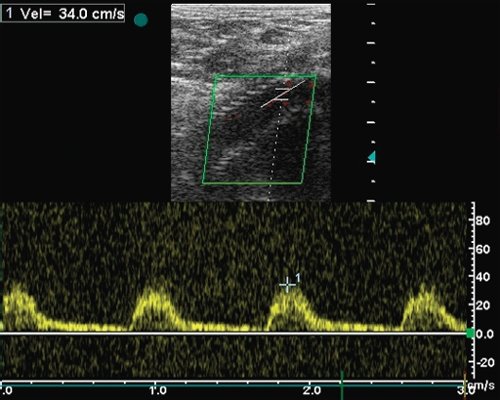
а) Допплерограмма кровотока из шунта на 3-5 см выше уровня дистального анастомоза (Vps - 34 см/с).
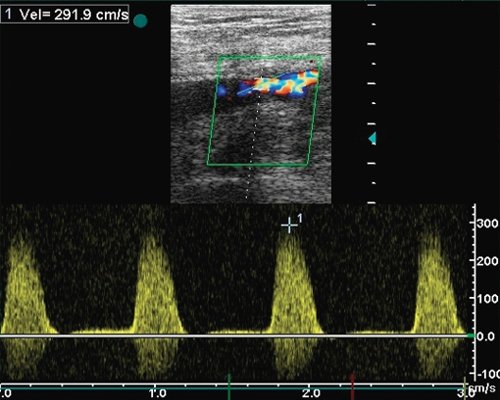
б) Допплерограмма кровотока из зоны стеноза (Vps - 292 см/с).
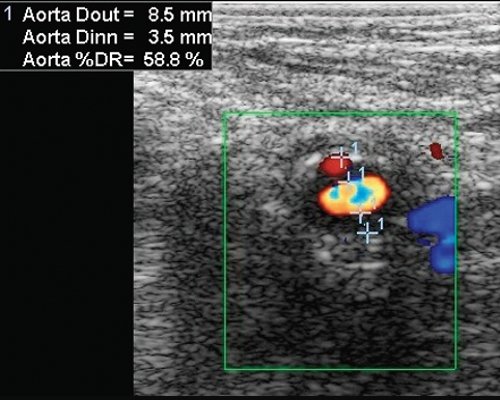
в) Поперечное сечение поверхностной бедренной артерии в области дистального анастомоза, планиметрическая оценка степени стеноза "по диаметру", стеноз 59%.
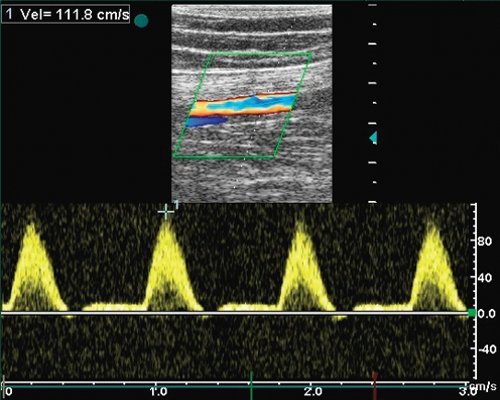
г) Магистральный кровоток в поверхностной бедренной артерии в средней 1/3 бедра (Vps - 111 см/с). Нормальные характеристики кровотока ниже дистального анастомоза позволяют исключить стеноз более 75% и подтверждают результаты планиметрической оценки "по диаметру".
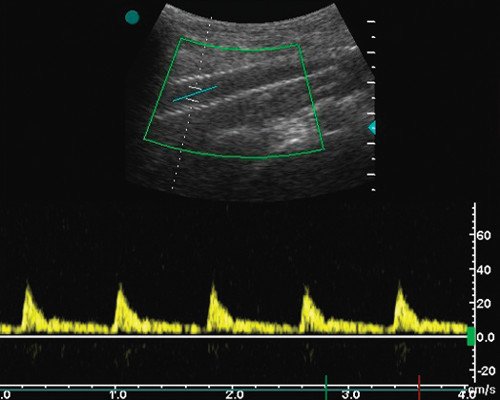
Допплерограмма кровотока из средней 1/3 протеза (Vps - 30 см/с), значимые сужения проксимальных и дистальных сегментов сосудистого русла не обнаружены.
В протоколе ультразвукового исследования аорты и артерий нижних конечностей после шунтирующих операций особое внимание уделяется описанию структурно-анатомических изменений приносящих сосудов и характеристике кровотока в них, характеристике кровотока и оценке состояния проксимального, дистального анастомозов и шунтирующего сосуда на всем протяжении, а также описанию структурно-анатомических изменений выносящих сосудов и характеристике кровотока в них [10].
При исследовании шунтирующего сосуда делаются акценты на анализе Vps и расчете отношения пиковой скорости кровотока в зоне ее локального увеличения (в зоне стеноза) к пиковой скорости кровотока, зарегистрированной проксимальнее стеноза (Vps-ratio). Кроме того, протокол ультразвукового исследования требует максимально полного описания планиметрических характеристик стенозированного сегмента шунта, а в случае аутовенозного шунтирования - оценки диаметра шунтирующей вены в поперечном сечении над и ниже стеноза, протяженности стеноза и четкого указания анатомической локализации стеноза.
Допплерографическая градация степени стеноза и группы риска тромбоза шунта
Существует допплерографическая градация степени стеноза аутовенозных шунтов, которая базируется на оценке Vps в зоне стеноза и Vps-ratio [19], разработанная на основании сопоставления данных дуплексного сканирования с результатами ангиографии (табл.).
| Степень стеноза,% | Vps в зоне стеноза, см/с | Vps-ratio, у.е. |
|---|---|---|
| < 20 | < 125 | < 1,4 |
| 20-50 | < 180 | 1,5-2,4 |
| 50-75 | > 180 | 2,5-4,0 |
| > 75 | > 300 | > 4,0 |
Однако наибольшей прогностической эффективностью обладает оценка степени риска тромбоза аутовенозного шунта на основе комбинации таких показателей, как Vps в зоне стеноза, Vps-ratio, средняя Vps в шунте (среднее значение пиковой систолической скорости кровотока из 3-4 равноудаленных зон шунта вне области стеноза) и лодыжечно-плечевой индекс давления (ЛИД). Низкая скорость кровотока по шунту увеличивает риск тромбоза [20]. Риск тромбоза аутовенозного шунта ниже по сравнению с искусственным протезом [10], а профилактическое назначение антикоагулянтной и дезагрегантной терапии снижает риск развития тромбоза низкоскоростных шунтов [6-7].
К группе наивысшего риска (I степень) с угрозой тромбоза в ближайшее время относятся шунты, стенозированные более чем на 70% с Vps в зоне стеноза > 300 см/с, Vps-ratio > 3,5 у.е., с низкоскоростным кровотоком по шунту (средняя Vps < 45 см/с) вне области стеноза и уменьшением ЛИД (по сравнению с предшествующей оценкой) более чем на 0,15 у.е. (см. рис. 6).
К группе высокого риска тромбоза (II степень) относятся шунты, стенозированные более чем на 70% с Vps в зоне стеноза > 300 см/с, Vps-ratio > 3,5 у.е., с нормальной скоростью кровотока по шунту вне области стеноза (средняя Vps > 45 см/с) и уменьшением ЛИД (по сравнению с предшествующей оценкой) менее чем на 0,15 у.е.
Группы наивысшего и высокого риска тромбоза (I и II степень) требуют ревизии шунта и хирургического восстановления его проходимости. Вероятность прогрессирования стеноза или развития тромбоза в этих группах в течение 3-6 месяцев составляет 40-50%. Для группы наивысшего риска (I степень) рекомендуется немедленное восстановление проходимости шунта, в то время как для группы высокого риска (II степень) возможно восстановление в плановом порядке в течение 1-2 нед.
К группе умеренного риска тромбоза (III степень) относятся шунты, стенозированные на 50-70% с Vps в зоне стеноза 180-300 см/с, Vps-ratio > 2 у.е., с нормальной скоростью кровотока по шунту вне области стеноза (средняя Vps > 45 см/с) и уменьшением ЛИД (по сравнению с предшествующей оценкой) менее чем на 0,15 у.е.
К группе низкого риска тромбоза (IV степень) относятся шунты, не стенозированные или стенозированные < 50% с Vps в зоне стеноза < 180 см/с, Vps-ratio < 2 у.е., с нормальной скоростью кровотока по шунту вне области стеноза (средняя Vps > 45 см/с) и уменьшением ЛИД (по сравнению с предшествующей оценкой) менее чем на 0,15 у.е. (см. рис. 7).
В группах риска III и IV степени поражения шунта, обнаруженные в первые 3 мес. от момента шунтирования, в 20-30% случаев регрессируют, в 10-20% случаев остаются стабильными, а в 40-50% случаев прогрессируют до стеноза более 70%.
Для группы умеренного риска рекомендуется динамическое наблюдение с интервалом в 4-6 нед для подтверждения или исключения прогрессирования стеноза. При динамическом исследовании прогрессирование стеноза подтверждается увеличением Vps в зоне стеноза, уменьшением среднего значения Vps по шунту вне области стеноза и снижением ЛИД > 0,15 у.е. и, соответственно, переходом в группу высокого или наивысшего риска [10].
В сравнении с аутовенозным шунтированием исследования, посвященные роли дуплексного сканирования в наблюдении протезных шунтов и определении показаний к хирургическому вмешательству на измененных протезах, не так многочисленны. Однако было показано, что после протезного шунтирования включение в программу наблюдения дуплексного сканирования и выполнение реконструктивного вмешательства на шунтирующих сосудах на основании его результатов сопровождается 5-летней проходимостью шунтов около 88% и превосходит таковые показатели без динамического дуплексного наблюдения [7]. При бедренно-бедренном протезном шунтировании ультразвуковыми предвестниками тромбоза шунта являются Vps в приносящей подвздошной артерии более 300 см/с, наличие стеноза протеза с локальным увеличением Vps более 300 см/с и средним значением Vps в протезе менее 60 см/с [7]. Детальная допплерографическая градация степени стеноза и степени риска тромбоза для синтетических и биологических протезов отсутствует. В связи с этим допустимо использование ультразвуковых критериев степени стеноза и степени риска тромбоза аутовенозных шунтов для синтетических и биологических протезов (рис. 12).
В качестве прогностического критерия риска тромбоза протезного шунта может быть использовано среднее значение Vps в протезе менее 45 см/с [8]. Однако низкая скорость кровотока по шунту (рис. 13) прежде всего предполагает тщательное исследование проксимальных и дистальных сегментов сосудистого русла с целью исключения/подтверждения значимых сужений. Самостоятельное значение низкой скорости кровотока по шунту до конца не определено, однако требует в протоколе ультразвукового исследования указания: "снижение скоростных показателей кровотока по шунту".
Одним из предрасполагающих факторов к развитию тромбоза является перегиб (перекрут) шунта/протеза (рис. 14), сопровождающийся сужением функционирующего просвета и локальными нарушениями кровотока в виде увеличения Vps.
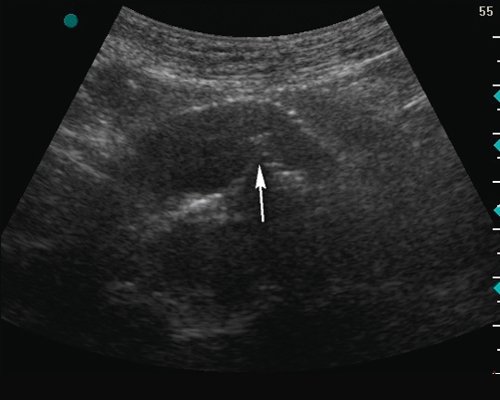
а) Продольное сечение протеза на 2-4 см ниже уровня проксимального анастомоза, стрелкой показан перегиб протеза.
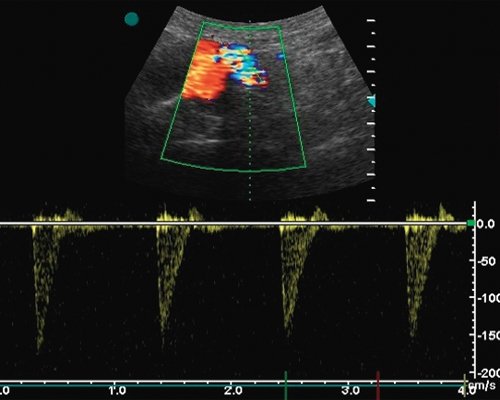
б) Допплерограмма кровотока из области перегиба, Vps локально увеличена до 150 см/с.
Диагностика осложнений шунтирующих операций
Дуплексное сканирование обладает высокой точностью в диагностике таких осложнений шунтирующих операций, как аневризма сосудов в области проксимального (центрального) и/или дистального анастомозов (рис. 15), аневризма протеза на протяжении (более характерно для биологических протезов, рис. 10), диагностике пульсирующей гематомы (рис. 16), ложной аневризмы в области проксимального или дистального анастомозов (рис. 17), а также в диагностике артериовенозных фистул (рис. 18, 19).
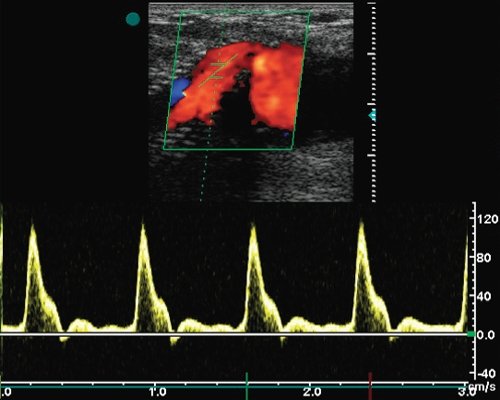
а) Допплерограмма кровотока из шунта на 1-2 см выше уровня дистального анастомоза (Vps - 120 см/с).
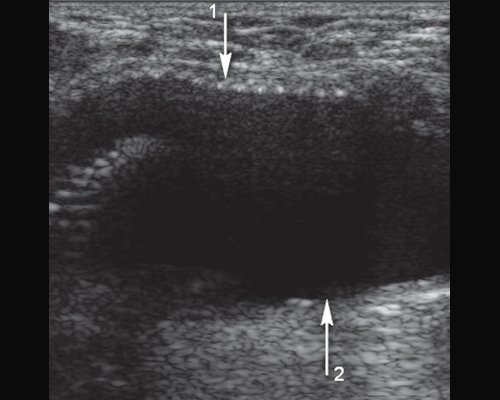
б) Зона дистального анастомоза, стрелка 1 - протез, стрелка 2 - расширенная общая бедренная артерия (диаметр - 17 мм).
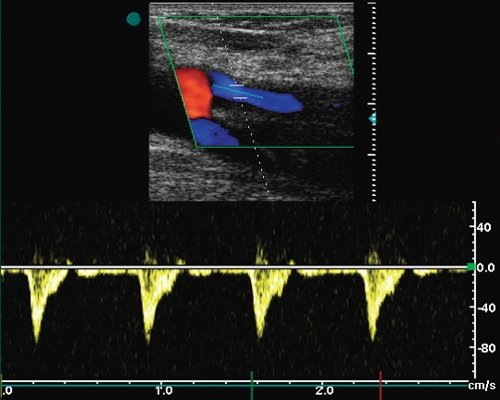
в) Магистральный кровоток в поверхностной бедренной артерии на 1-2 см ниже уровня дистального анастомоза (Vps - 70 см/с).
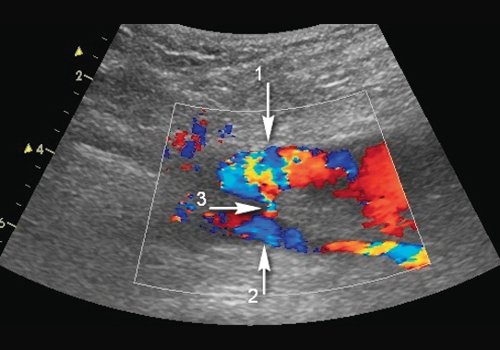
а) Продольное сечение. Стрелка 1 - полость гематомы, стрелка 2 - общая бедренная артерия, стрелка 3 - канал между общей бедренной артерией и полостью гематомы, диаметр канала - 3-3,5 мм.
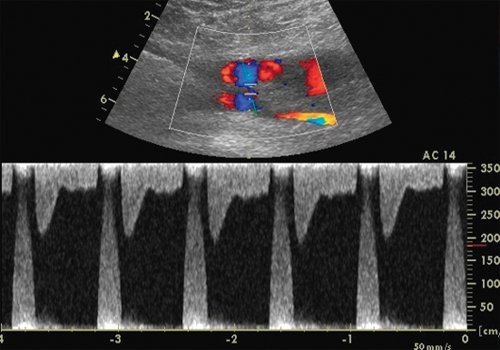
б) Допплерограмма кровотока из канала, Vps локально увеличена до 320 см/с.
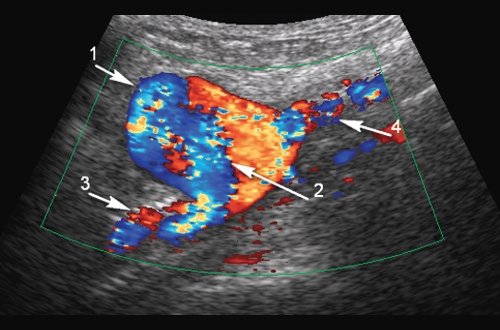
а) Продольное сечение. Стрелка 1 - аневризматический мешок, стрелка 2 - широкое основание аневризматического мешка, стрелка 3 - синтетический протез, стрелка 4 - поверхностная бедренная артерия.
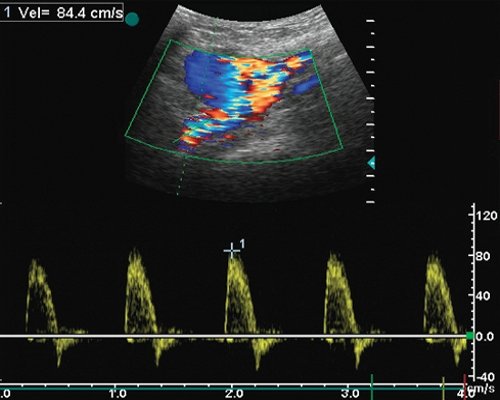
б) Допплерограмма из шунта перед областью аневризматического мешка, магистральный кровоток, Vps - 84 см/с.
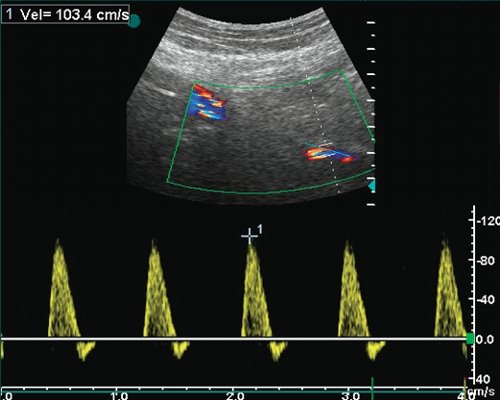
в) Допплерограмма из средней 1/3 поверхностной бедренной артерии, дистальнее аневризматического мешка, магистральный кровоток, Vps - 103 см/с.
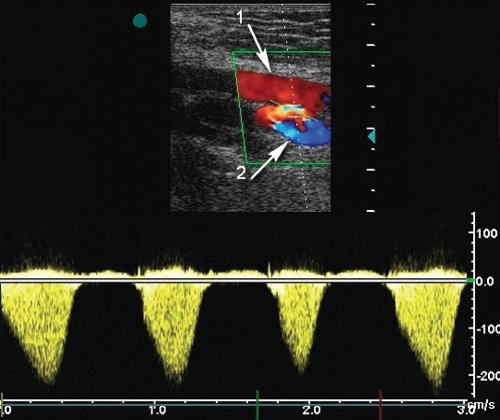
а) Допплерограмма кровотока из области фистулы, диаметр фистулы - 2,5-3 мм. Стрелка 1 - поверхностная бедреннартерия, стрелка 2 - поверхностная бедренная вена.
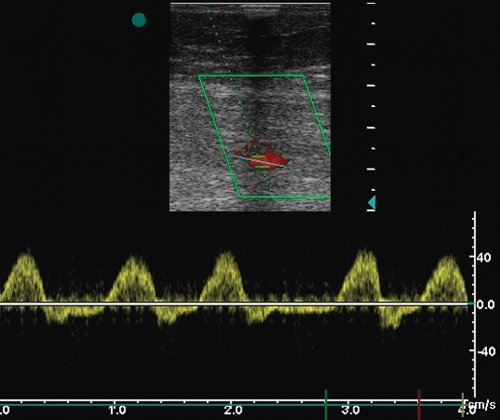
б) Допплерограмма из поверхностной бедренной вены на 3-5 см дистальнее фистулы, характер кровотока псевдоартериальный, Vps - 45 см/с.
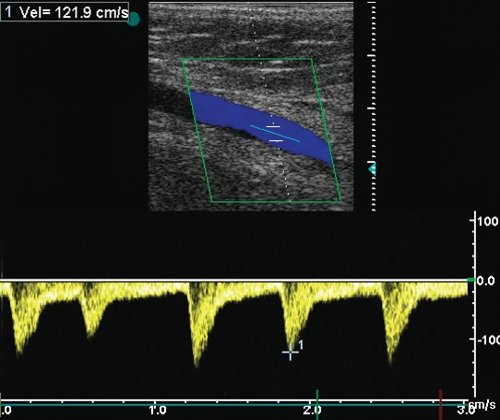
а) Допплерограмма кровотока из аутовенозного шунта на 4-5 см выше фистулы (притока аутовены), средняя 1/3 бедра, характер кровотока магистрально-измененный (низкорезистентный), Vps - 120-130 см/с, RI - 0,8 у.е.
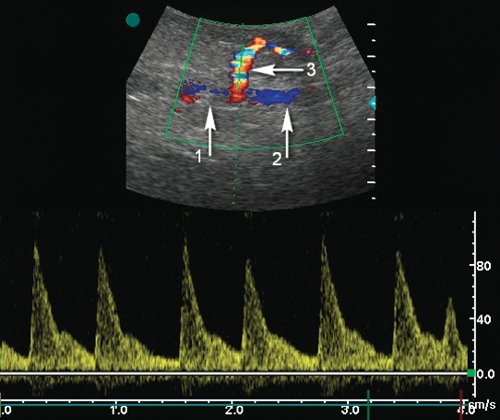
б) Допплерограмма из фистулы (притока аутовены), характер кровотока артериальный, Vps - 95 см/с.
Заключение
Очевидно, что дуплексное сканирование - это первичная диагностическая процедура при подозрении на нарушение функционирования шунта в любой период от момента проведения реконструктивной операции. Результаты дуплексного сканирования, проведенного опытным специалистом, могут рассматриваться в качестве показаний для проведения ангиографического исследования [9] или для превентивного хирургического вмешательства на шунтирующих сосудах [4].
Литература
- Hirsch A.T., Haskal Z.J., Hertzer N.R., et al. ACC/AHA 2005 Guidelines for the Management of Patients With Peripheral Arterial Disease (Lower Extremity, Renal, Mesenteric, and Abdominal Aortic): A Collaborative Report from the American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, and the ACC/AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Peripheral Arterial Disease) // J Am Coll Cardiol. 2006. N 47. P. e1-e192.
- Layden J., Michaels J., Bermingham S., et al. Diagnosis and management of lower limb peripheral arterial disease: summary of NICE guidance // BMJ. 2011. N 345. P. e4947.
- Rooke T.W., Hirsch A.T., Misra S., et al. ACCF/ AHA Focused Update of the Guideline for the Management of Patients With Peripheral Artery Disease (Updating the 2005 Guideline) // J Am Coll Cardiol. 2011. V. 58. N 19. P. 2020-2045.
- Национальные рекомендации по ведению пациентов с заболеваниями артерий нижних конечностей (Рос. об-во ангиологов и сосудистых хирургов, Ассоц. сердечн.-сосуд. хирургов России, Рос. науч. об-во рентгенэндоваскулярных хирургов и интервенционных радиологов, Всерос. науч. об-во кардиологов, Ассоц. флебологов России) // Ангиология и сосудистая хирургия. 2013. Т. 19. Приложение 2. С. 2-67.
- Tendera M., Aboyans V., Bartelink M.L., et al. ESC Guidelines on the diagnosis and treatment of peripheral artery diseases: Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries: the Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology (ESC) // Eur Heart J. 2011. V. 32. N 22. P. 2851-2906.
- Tinder C.N., Chavanpun J.P., Bandyk D.F., et al. Efficacy of duplex ultrasound surveillance after infrainguinal vein bypass may be enhanced by identification of characteristics predictive of graft stenosis development // J Vasc Surg. 2008. V. 48. P. 613-618.
- Stone P.A., Armstrong P.A., Bandyk D.F., et al. Duplex ultrasound criteria for femoral-femoral bypass revision // J Vasc Surg. 2006. V. 44. P. 496-502.
- Brumberg S.R., Back M.R., Armstrong P.A., et al. The relative importance of graft surveillance and warfarin therapy in infrainguinal prosthetic bypass failure // J Vasc Surg. 2007. V. 46. P. 1160-1166.
- Haimovici's vascular surgery. 6th edition / edited by Ascher Å., Veith F.J., Gloviczki P., et al. - Blackwell Publishing. 2012. 1317 pp.
- Rutherford's vascular surgery. 6th edition / edited by Cronenwett J.L., Johnston K.W. - Elsevier Health Sciences. 2014. 2688 pp.
- Bradbury A.W., Adam D.J., Bell J., et al. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) trial: Analysis of amputation free and overall survival by treatment received // Journal of Vascular Surgery. 2010. V. 51. P. 18S-31S.
- Conte M.S. Bypass versus Angioplasty in Severe Ischaemia of the Leg (BASIL) and the (hoped for) dawn of evidence-based treatment for advanced limb ischemia // Journal of Vascular Surgery. 2010. V. 51. P. 69S-75S.
- Szilagyi D.E., Elliott J.P., Smith R.F., et al. A thirty-year survey of the reconstructive surgical treatment of aortoiliac occlusive disease // J Vasc Surg. 1986. V. 3. N 3. P. 421-436.
- Nevelsteen A., Wouters L., Suy R., et al. Aortofemoral Dacron reconstruction for aorto-iliac occlusive disease: a 25-year survey // Eur J Vasc Surg. 1991. V. 5. P. 179-186.
- Барбараш Л.С., Иванов С.В., Журавлева И.Ю. и др. 12-летний опыт использования биопротезов для замещения инфраингвинальных артерий // Ангиология и сосудистая хирургия. 2006. Т. 3. № 12. С. 91-97.
- Журавлева И.Ю., Кудрявцева Ю.А., Иванов С.В. и др. Пути и перспективы совершенствования инфраингвинальных артериальных биопротезов // Патология кровообращения и кардиохирургия. 2005. № 1. С. 78-83.
- Mohler E.R., Gornik H.L., Gerhard-Herman M., et al. ACCF/ACR/AIUM/ASE/ASN/ICAVL/SCAI/ SCCT/SIR/SVM/SVS 2012 appropriate use criteria for peripheral vascular ultrasound and physiological testing, part 1: arterial ultrasound and physiological testing // J Am Coll Cardiol. 2012. V. 60. P. 242-276.
- Norgren L., Hiatt W.R., Dormandy J.A., et al. TASC II Working Group: Inter-Society consensus for the management of peripheral arterial disease (TASC II) // J Vasc Surg. 2007. V. 45. P. S5-S67.
- Jaff M., Mohler E., Roman M., et al. Guidelines for noninvasive vascular laboratory testing: a report from the American Society of Echocardiography and the Society for Vascular Medicine and Biology // Vasc Med. 2006. V. 11. N 3. P. 183-200.
- Bandyk D., Cato R., Towne J. A low velocity predicts failure of femoropoliteal and femorotibial bypass grafts // Surgery. 1985. V. 98. P. 799-809.

УЗ сканер Samsung HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Публикации по теме
- Аномалия Эбштейна (эхографические, клинические и патоморфологические сопоставления) - Делягин В.М.
- Клинико-инструментальная характеристика некомпактного миокарда левого желудочка - Малинин М.В.
- Цветовое дуплексное сканирование после шунтирующих операций на артериях нижних конечностей - Засорин С.В.
- Возможности трансторакальной эхокардиографии в диагностике расслаивающей аневризмы аорты. Клинический случай - Поветкин С.В.
- Новые возможности оценки функционального состояния сердца при артериальной гипертензии - Хадзегова А.Б.


