Новые возможности оценки функционального состояния сердца при артериальной гипертензии
Рубрика: Эхография в кардиологии
Артериальная гипертензия (АГ) - одна из наиболее значимых медикосоциальных проблем, что обусловлено большой распространенностью и высоким риском сердечно-сосудистых осложнений. По результатам эпидемиологических и когортных исследований последних лет, в России повышенное артериальное давление почти в 80% случаев ассоциируется с развитием хронической сердечной недостаточности [1]. Как известно, с хронической сердечной недостаточностью ассоциируется не только высокий уровень инвалидизации, но и высокий риск смертности, поэтому в настоящее время одной из актуальных проблем кардиологии остается проблема ранней диагностики и лечения последней.
В настоящее время бурное развитие современных ультразвуковых технологий привело к появлению совершенно иных подходов к оценке функционального состояния сердца, которые на очень ранних этапах заболевания позволяют выявлять минимальные нарушения функции сердца. Мы еще не успели должным образом изучить возможности тканевой допплерографии, как появилась еще одна методика, получившая в англоязычной литературе название - speckle tracking. В отличие от тканевой допплерографии, основанной на эффекте допплера, speckle tracking основан на определении скорости движения миокарда при помощи отслеживания перемещения естественных акустических маркеров - пятнистых структур, на стандартном эхокардиографическом изображении в В-режиме (рис. 1).
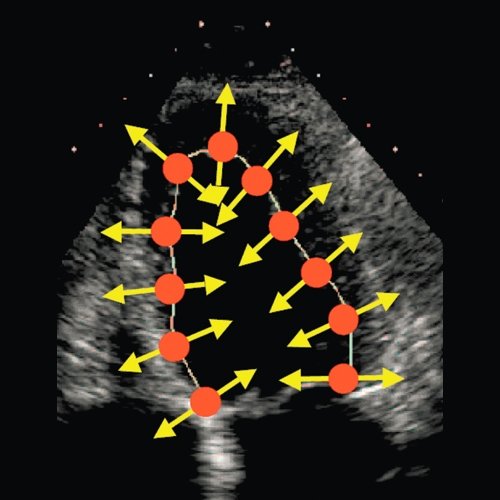
Рис. 1. Оценка скорости движения миокарда при помощи отслеживания перемещения естественных акустических маркеров - пятнистых структур, на стандартном эхокардиографическом изображении в В-режиме.
Суть метода заключается в том, что акустические маркеры случайным образом равномерно распределяются по всему миокарду. Размер каждого пятна составляет от 20 до 40 пикселей (точек). Положение каждого пятна определяется и точно прослеживается на последовательных кадрах. Таким образом, можно определить расстояние, на которое перемещается пятно от кадра к кадру. Зная частоту смены кадров, можно определить скорость движения пятна. С целью повышения качества отслеживания пятнистых структур применяется высокая частота смены кадров - 60-100 кадров в секунду. Особенности движения сердца, вращение в грудной клетке, а также дыхательная экскурсия грудной клетки могут приводить к смещению пятен из плоскости сканирования. Однако эти изменения не успевают произойти в значимом количестве между двумя последовательными кадрами. Таким образом, по движению пятнистых структур можно получить данные о скорости, деформации и скорости деформации всех участков миокарда. Техника вычисления деформации по двухмерному изображению значительно проще, чем при использовании тканевой допплерографии, так как при этом отсутствуют ограничения, связанные с параллельностью движения объекта и ультразвукового луча. Для последующих вычислений достаточно одного сердечного цикла (рис. 2). Обработка ультразвуковых изображений проводится в режиме offline [2].
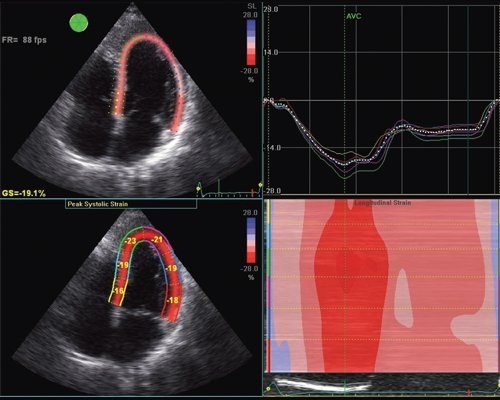
Рис. 2. Оценка продольной деформации левого желудочка с помощью ультразвуковой технологии speckle tracking в В-режиме.
С появлением ультразвуковой технологии speckle tracking стало возможным более детальное изучение регионарной систолической и диастолической функции не только продольных волокон, но и радиальных, окружностных, поскольку, новая технология лишена угловых ограничений, присущих тканевой допплерографии. Это делает возможным исследование продольной сократимости даже верхушечных сегментов левого желудочка. Благодаря технологии speckle tracking стало возможным изучение показателей апикальной и базальной ротации, скручивания и раскручивания сердца, что позволяет по-новому оценивать физиологию сокращения и расслабления миокарда.
Скручивание левого желудочка определяется как ротация верхушки сердца относительно основания и обусловлено сокращением косых спиральных волокон, что сводит к минимуму трансмуральный градиент деформации волокон и потребления кислорода. Как известно, волокна миокарда имеют сложную пространственную ориентацию, следуя вокруг полости по спирали [3]. Наружный (субэпикардиальный) слой миокарда представлен мышечными пучками косо ориентированных волокон, которые начинаясь от фиброзных колец, продолжаются вниз к верхушке сердца, где образуют завиток сердца и переходят во внутренний (субэндокардиальный) слой миокарда, пучки волокон которого расположены продольно. Наружный и внутренний слои миокарда являются общими для обоих желудочков, а расположенный между ними средний слой, образованный круговыми (циркулярными) пучками мышечных волокон, отдельный для каждого желудочка.
Во время систолы левый желудочек совершает движение с ротацией верхушки против часовой стрелки и с ротацией основания по часовой стрелке. После окончания систолы быстро происходит раскручивание, которое сопровождается противоположной ротацией по отношению к систоле. Раскручивание происходит преимущественно во время периода изоволюмического расслабления и ассоциируется с восстановлением сил, расходуемых во время систолы, что способствует диастолическому наполнению и представляет собой чувствительный параметр релаксации миокарда. Ротация против часовой стрелки, рассматриваемая с верхушки левого желудочка, выражается положительной величиной, тогда как ротация по часовой стрелке - величина отрицательная [3].
Особенности нарушения диастолической функции левого желудочка при артериальной гипертензии заключаются в том, что они имеются уже на ее ранних стадиях и определяются в первую очередь возрастающей постнагрузкой на левый желудочек. Наиболее характерным типом нарушения диастолической функции у больных АГ является тип с нарушенной релаксацией. И зачастую именно данный тип нарушения диастолической функции является единственной эхокардиографической находкой у таких больных. Концентрическая гипертрофия, развивающаяся при перегрузке левого желудочка давлением, еще больше усиливает уже имеющуюся диастолическую дисфункцию.
Таким образом, учитывая сложности анатомического строения и функциональной деятельности сердца, появление технологии speckle tracking, безусловно, является прорывом в оценке функционального состояния сердца, поскольку появляется уникальная возможность оценивать особенности систолической и диастолической функции отдельных слоев миокарда, что очень важно учитывать при комплексном обследовании больных АГ. Показатели апикальной и базальной ротации, скручивания и раскручивания сердца могут расширить наши представления о патофизиологических процессах, происходящих в сердце при артериальной гипертензии. Возможно, будут сформулированы новые подходы к оценке не только диастолической, но и систолической функции сердца с учетом не только показателей левого желудочка, но и состояния всех камер сердца.
До настоящего времени у больных АГ основным механизмом развития хронической сердечной недостаточности традиционно считалась изолированная диастолическая дисфункция левого желудочка с сохранением систолической функции. Появление тканевой допплерографии дало возможность определить, что у больных АГ с симптомами хронической сердечной недостаточности, несмотря на нормальные значения фракции выброса левого желудочка, имеют место регионарные нарушения продольной систолической функции левого желудочка [4, 5]. С накоплением данных об особенностях нарушения продольной систолической функции левого желудочка появилось понятие о диастолической сердечной недостаточности с сохраненной фракцией выброса левого желудочка.
Использование технологии speckle tracking при артериальной гипертензии полностью подтвердило нарушение при нормальной фракции выброса продольной систолической функции левого желудочка.
В исследовании Y. Liu и соавт. [6] показано, что у пациентов с диастолической сердечной недостаточностью скрытые нарушения систолической функции левого желудочка могут проявляться снижением глобальной пиковой продольной деформации (-14±5% против -20±3% в контрольной группе, p<0,0001), что позволяет использовать технологию speckle tracking для выявления доклинических нарушений систолической функции левого желудочка.
Y. Mizuguchi и соавт. [7] у 70 пациентов с сердечно-сосудистыми факторами риска и нормальной фракцией выброса левого желудочка оценивали систолическую и диастолическую функцию продольных, радиальных и окружностных волокон левого желудочка с последующим вычислением деформации миокарда. На основании данного анализа ими был сделан вывод о том, что наиболее ранним и надежным маркером доклинических нарушений сократимости и релаксации левого желудочка является изменение продольной деформации миокарда, поскольку из 3 направлений движения миокарда нарушения прежде всего выявляются в продольном направлении. Эти данные согласуются с результатами других исследований. По данным некоторых авторов [8, 9], при артериальной гипертензии продольная систолическая функция левого желудочка прогрессивно ухудшается в соответствии с функциональным классом хронической сердечной недостаточности. Так, при I функциональном классе хронической сердечной недостаточности данные нарушения выявляются только в базальном сегменте межжелудочковой перегородки, что, по мнению авторов, связано исключительно с фиброзом миокарда данной области. В последующем, при прогрессировании хронической сердечной недостаточности, т.е. при III и IV функциональном классе, данные нарушения уже выявляются практически во всех сегментах левого желудочка. При этом важно отметить, что радиальная и окружностная систолическая функция левого желудочка значительно дольше остается нормальной, компенсируя тем самым раннее нарушение продольной систолической функции миокарда. Значимое нарушение радиальной или окружностной систолической функции левого желудочка выявляется только на стадии формирования у пациентов с хронической сердечной недостаточностью III или IV функциональном классе.
При артериальной гипертензии выявление гипертрофии левого желудочка и оценка ее влияния на прогноз заболевания остается важной клинической задачей. J. Chen и соавт. [10] показали, что при гипертрофии левого желудочка локальные нарушения систолической функции выявляются рано, несмотря на нормальные показатели глобальной фракции выброса. Так, при обследовании 20 пациентов с артериальной гипертензией выявлено снижение пиковых сегментарных скоростей систолической деформации в позициях по длинной и короткой оси левого желудочка в сравнении с соответствующими сегментами в контрольной группе.
Исследование B. Goebel и соавт. [11] проводилось с целью изучения влияния степени гипертрофии левого желудочка на регионарную и глобальную функцию миокарда. У пациентов со значительной гипертрофией левого желудочка (индекс массы миокарда левого желудочка больше 149 г/м² - у мужчин и 122 г/м² - у женщин) отмечается более выраженное снижение систолической функции продольных и радиальных волокон миокарда, чем при незначительной и умеренной гипертрофии левого желудочка. Однако не выявлено влияния степени гипертрофии левого желудочка на величину его систолического скручивания.
Имеются данные и об использовании ультразвуковой технологии speckle tracking в дифференциальной диагностике патологической и физиологической гипертрофии левого желудочка. В своем исследовании L. Toncelli с соавт. [12] показали, что у больных АГ в сравнении со спортсменами, более высокие показатели скручивания левого желудочка (23,7±5,2° и 15,2±4,6°, соответственно, p=0,0001), базальной (-9,2±3,3° и -6,6±2,5°, соответственно, p<0,001) и особенно апикальной (14,4±5,4° и 8,6±4,1°, соответственно, p=0,001) ротации, тогда как продольная и окружностная деформации левого желудочка были схожи в обеих группах.
A. D'Andrea и соавт. [13] использовали технологию speckle tracking для сравнительной оценки функции левого предсердия при артериальной гипертензии и у спортсменов. Так, обследовав 40 пациентов с артериальной гипертензией, 45 сопоставимых по возрасту спортсменов (>40 лет) и 25 здоровых добровольцев авторы установили, что при патологической гипертрофии левого желудочка пиковая систолическая деформация по всем проанализированным сегментам левого предсердия значительно (p<0,0001) снижена.
В настоящее время технология speckle tracking в основном используется для оценки систолической функции левого желудочка, и очень мало работ по оценке диастолической функции. В работе M. Takeuchi и соавт. [14] показано, что замедление и снижение диастолического раскручивания левого желудочка во время периода изоволюмического расслабления у больных АГ с гипертрофией миокарда свидетельствует о нарушении релаксации. В аналогичном исследовании S. Park и соавт. [15], у пациентов с сохраненной фракцией выброса замедление раскручивания левого желудочка сопровождалось увеличением систолического скручивания за счет апикальной и базальной ротации. По мнению авторов, при нарушении релаксации левого желудочка усиление скручивания миокарда является компенсаторным механизмом.
Как известно, возрастные изменения миокарда также ассоциируются с нарушением диастолической функции левого желудочка. Механизмы, лежащие в их основе до конца не изучены, хотя одной из причин считают снижение содержания кальция в саркоплазматическом ретикулуме, что приводит к увеличению продолжительности релаксации миокарда. В исследовании M. Takeuchi и соавт. [3], выполненном у 113 здоровых добровольцев, разделенных на 3 группы в соответствии с возрастом,показано, что пиковое значение скручивания левого желудочка с возрастом увеличивается, а раскручивание левого желудочка, напротив, снижается и замедляется. Среднее значение пикового скручивания составляет 7,7±3,5°. Скручивание увеличивается в результате преобладания сокращения субэпикардиальных волокон над сокращением субэндокардиальных. Поэтому с возрастом субэндокардиальный фиброз, как и субэндокардиальная ишемия или фиброз вследствие гипертрофии миокарда, приводят к увеличению систолического скручивания левого желудочка. Также, при концентрической гипертрофии левого желудочка в результате утолщения стенок с сохранением или уменьшением размера полости, влияние субэпикардиальных волокон усиливается относительно субэндокардиальных [16]. Таким образом, увеличение систолического скручивания является неспецифическим признаком, ассоциируемым как с возрастными изменениями миокарда, так и с гипертрофией миокарда левого желудочка. В ряде аналогичных работ также было показано возрастное увеличение систолического скручивания левого желудочка за счет усиления базальной ротации [17, 18]. По мнению M. Yilmazer и соавт. [19], концентрическая гипертрофия левого желудочка является главной причиной увеличения показателей апикальной ротации и скручивания левого желудочка в покое и их снижение при физической нагрузке может свидетельствовать о ранних нарушениях сократительной функции миокарда. Однако, по результатам исследований J. Wang и соавт. [20, 21], механизм скручивания и раскручивания левого желудочка у пациентов с диастолической сердечной недостаточностью не зависит от релаксации миокарда. В их исследованиях показано, что у пациентов с диастолической сердечной недостаточностью снижены только продольная и радиальная деформации при сохранении показателей окружностной деформации, скручивания и раскручивания левого желудочка. Безусловно, такое разногласие должно быть улажено, что требует дальнейшего изучения роли скручивания и раскручивания левого желудочка у пациентов с диастолической дисфункцией с применением технологии speckle tracking.
Известно, что при артериальной гипертензии отмечается нарушение структурно-функционального состояния обоих желудочков сердца. С появлением технологии speckle tracking, позволяющей неинвазивно оценивать глобальную и сегментарную систолическую и диастолическую функции правого желудочка наравне с левым, значительно возрос интерес исследователей к изучению его функционального состояния. Так, E. Ogawa и соавт. [22], используя технологию speckle tracking, оценивали деформацию и скорость деформации правого желудочка из четырехкамерной апикальной позиции у 30 больных АГ с гипертрофией левого желудочка. Средний возраст больных составил 59±15 лет, величина фракции выброса левого желудочка - 64±5%. Согласно представленным данным, при гипертрофии левого желудочка имеет место ухудшение как систолической, так и диастолической функции правого желудочка, что проявляется значительным, по сравнению с сопоставимой по возрасту контрольной группой, снижением величины систолической деформации (-20±4% против -23±4% в контрольной группе, p<0,05) и скорости пиковой релаксации (0,96±0,23 1/с против 1,21±0,32 1/с в контрольной группе, p<0,05).
Таким образом, появление новых подходов к оценке функционального состояния миокарда с использованием современных ультразвуковых технологий, в частности технологии speckle tracking, может помочь в ранней диагностике систолической и диастолической дисфункции сердца при артериальной гипертензии. Использование технологии speckle tracking особенно полезно в тех случаях, когда функциональные нарушения носят не глобальный, а регионарный характер, для выявления которых недостаточно традиционной оценки фракции выброса, трансмитрального или транстрикуспидального потоков. Особый интерес представляет использование технологии speckle tracking для оценки функционального состояния предсердий. Практически неизученным остается использование данной методики для оценки диастолической функции левого желудочка.
Литература
- Кардиология: национальное руководство / Под ред. Беленкова Ю.Н., Оганова Р.Г. М.:ГЭОТАР-Медиа, 2008.
- Perk G., Tunick P.A., Kronzon I. Non-doppler twodimensional strain imaging by echocardiography - from technical considerations to clinical applications // J Am Soc Echocardiogr. 2007. V. 20. P. 234-243.
- Takeuchi M., Nakai H., Kokumai M. et al. Age-related changes in left ventricular twist assessed by two-dimensional speckle-tracking imaging // J Am Soc Echocardiogr. 2006. V. 19. P. 1077-1084.
- Никитин Н.П. Применение тканевой миокардиальнойдопплерэхокардиографии в кардиологии // Кардиология. 2002. N3. С. 66-79.
- Васюк Ю.А., Хадзегова А.Б., Иванова С.В. и др. Тканевая допплерография в ранней диагностике функциональных нарушений миокарда при артериальной гипертензии // Рациональная фармакотерапия в кардиологии. 2008. N1. C. 39-43.
- Liu Y., Tsai W.C., Lin C. et al. Evidence of subtle left ventricular systolic dysfunction detected by automatic function imaging in patients with diastolic heart failure // Abstracts of EUROECHO the twelfth. 2008. M963, p.S120.
- Mizuguchi Y., Oishi Y., Miyoshi H. et al. The functional role of longitudinal, circumferential and radial myocardial deformation for regulating the early impairment of left ventricular contraction and relaxation in patients with cardiovascular risk factors: a study with two-dimensional strain imaging // J Am Soc Echocardiogr. 2008. V. 21. P. 1138-1144.
- Kosmala W., Plaksej R.,Strotmann J. et al. Progression of left ventricular functional abnormalities in hypertensive patients with heart failure: an ultrasonic two-dimensional speckle tracking study // J Am Soc Echocardiogr. 2008. V. 21. P. 1309-1317.
- Plaksej R., Strottman J., Kosmala W. et al. Non-homogenous progression of left ventricular systolic dysfunction in essential hypertension: potential impact of myocardial fibrosis and radial compensatory // Abstracts of EUROECHO the twelfth. 2008. P1248, p.S177.
- Chen J., Cao T., Duan Y. et al. Velocity vector imaging in assessing myocardial systolic function of hypertensive patients with left ventricular hypertrophy // Can J Cardiol. 2007. V. 23. N 12. P. 957-961.
- Goebel B., Gjesdal O., Kottke D. et al. Regional and global myocardial function in patients with hypertensive heart disease: a two-dimensional ultrasound speckle tracking study // Circulation. 2008. 118:S_991-S_992.
- Toncelli L.T., Cappelli F.C., Vono MCRV et al. Left ventricular rotation and torsion in different type of left ventricular hypertrophy // Abstracts of EUROECHO the twelfth. 2008. P1241; p.S175.
- D'Andrea A., De Corato G., Scarafile R. et al. Left atril myocardial function in either physiological or pathological left ventricular hypertrophy: a two-dimensional speckle strain study // Br J Sports Med. 2008. V. 42. N 8. P. 696-702.
- Takeuchi M., Borden W., Nakai H. et al. Reduced and delayed untwisting of the left ventricle in patients with hypertension and left ventricular hypertrophy: a study using two-dimensional speckle tracking imaging // European Heart J. 2007. V. 28. P. 2756-2762.
- Park S., Miyazaki C., Bruce C. et al. Left ventricular torsion by two-dimensional speckle tracking echocardiography in patients with diastolic dysfunction and normal ejection fraction // J AM Soc. Echocardiogr. 2008. V. 21. P. 1129- 1137.
- Borg A.N., Ray S.G. А unifying framework for understanding heart failure? Response to "Left ventricular torsion by twodimensional speckle tracking echocardiography in patients with diastolic dysfunction and normal ejection fraction" by Park SJ et al // J Am Soc Echocardiogr. 2009. V. 22. P. 318-320.
- Jung B-C. Age-related changes in left ventricular torsion assessed by two-dimensional speckle-tracking imaging // Abstracts of EUROECHO the twelfth 2008, O935, p.S116.
- Phan T.T., Shivu G.N., Abozguia K. et al. Left ventricular torsion and strain patterns in heart failure with normal ejection fraction are similar to age-related changes // European J Echocardiogr. 2009. V. 10. P. 793-800.
- Yilmazer M.S., Aydin A., Gurol T. et al. The effect of exercise on left ventricular rotation and twist features: concentric hypertrophy impairs exercise induced increase in rotation and twist // Abstracts of EUROECHO the twelfth. 2008. P268, p.S25.
- Wang J., Khoury DS, Yue Y. et al. Left ventricular untwisting rate by speckle tracking echocardiography // Circulation. 2007. V. 116. P. 2580-2586.
- Wang J., Khoury D.S., Yue Y. et al. Preserved left ventricular twist and circumferential deformation, but depressed longitudinal and radial deformation in patients with diastolic heart failure // European Heart J. 2008. V. 29. P. 1283-1289.
- Ogawa E., Dohi K., Onishi K. et al. Impaired right ventricular contraction and relaxation in patients with left ventricular hypertrophy and preserved left ventricular ejection fraction quantified by speckle-tracking strain and strain rate imaging // Circulation. 2008. V. 118. S-939.
УЗИ сканер Samsung W10
Аппарат экспертного/премиум класса поможет расширить возможности диагностики, благодаря интуитивно понятным алгоритмам обработки и точным инструментам анализа.
Публикации по теме
- Цветовое дуплексное сканирование после шунтирующих операций на артериях нижних конечностей - Засорин С.В.
- Возможности трансторакальной эхокардиографии в диагностике расслаивающей аневризмы аорты. Клинический случай - Поветкин С.В.
- Новые возможности оценки функционального состояния сердца при артериальной гипертензии - Хадзегова А.Б.
- Скорости потока в нисходящей коронарной артерии у больных с артериальной гипертонией и гипертрофией левого желудочка - E.Н. Павлюкова
- Состояние сердечной гемодинамики у больных с различными патогенетическими подтипами гипертонической энцефалопатии - Белова Л.А.


