Трехмерная эхография органов пищеварения (аналитический обзор)
Рубрика: Эхография брюшной полости

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Новейшие компьютерные технологии заложили основу революционного преобразования классического двухмерного сканирования (2D) в реальном масштабе времени. Результатом явилось создание трехмерной эхографии (3D).
С 1980-х годов некоторые научно-исследовательские лаборатории начали разработку новой методики, позволявшей получать трехмерную реконструкцию ультразвукового изображения в эхокардиографии [1] и эхоангиологии [2,3]. Впервые же трехмерное изображение было применено в компьютерной томографии для воспроизведения костных структур в черепно-лицевой хирургии [4]. Пионером 3D является компания Kretztechnic AG (контрольный пакет ее акций принадлежат корпорации Medison), создавшая в 1989 г. первый коммерческий прибор Сombison 330, производящий мультиплановую реконструкцию данных в трех оргтогональных проекциях при использовании специальных 3D-датчиков для трансабдоминального и трансректального сканирования.
К достоинствам 3D УЗИ, выгодно отличающим ее от КТ и МРТ, следует отнести отсутствие ионизирующего излучения, безопасность, неинвазивность и относительно низкую цену. Наибольшие преимущества трехмерного УЗИ состоят в возможности получения ультразвуковых срезов, которые невозможно увидеть при рутинном сканировании, и в точном измерении объема с использованием специальных программ и объемных датчиков. Помимо этого методика позволяет интерактивно манипулировать данными по объему, используя превращение, ротацию и увеличение лоцированных структур, воссоздавая истинную анатомию органов в прямой проекции [5]. Однако сегодня нет однозначного ответа на вопрос: какую роль играет эта методика в диагностике и какую информацию она может дать в дополнение к 2D?
За рубежом 3D ультрасонография получила самое широкое распространение в клинике акушерства и гинекологии, особенно для исследования плода [6, 7, 8]; накапливается первый опыт и в нашей стране [9]. Свое применение 3D ультрасонография нашла также в диагностике заболеваний органов пищеварения.
Печень
В развитых странах методики КТ, МРТ и УЗИ, взаимодополняя одна другую, а подчас и конкурируя, стали обязательными визуальными методами, применяющимися в гепатологии. При этом эхография, являясь самым распространенным методом, имеет определенные ограничения: меньше возможности давать общее панорамное изображение больших структур, выше чувствительность к артефактам, возникающим при прохождении луча через газ, кость или жир [10].
Алгоритм ультразвукового исследования печени требует сканирования с различных позиций, в трех плоскостях и в различные фазы дыхания, поскольку печень слишком велика, чтобы провести адекватное обследование всех ее долей из одной точки. В каждом случае исследователю необходимо точно представлять, какая часть органа осмотрена из определенного местоположения датчика. Именно поэтому совершенная 3D-система должна четко документировать, сканирование какой части печени было проведено и, таким образом, облегчить последующий анализ [11].
В клиническом контексте измерения объема органа проводятся для диагностики и последующего динамического наблюдения пациентов с различными заболеваниями. Простейшая 2D-методика расчета объема, основанная на умножении трех взаимно перпендикулярных диаметров, нередко сопряжена с ошибками. Поэтому измерение объема органа на основе 3D позволяет повысить точность и правильность результата [12].
В ряде клинических ситуаций знание истинного объема печени чрезвычайно важно. Известно, что как собственная, так и трансплантированная ткань печени способна регенерировать, поэтому визуальный метод постепенно входит в арсенал средств мониторинга этого процесса [13]. Хотя сегодня с этой целью ччаще всего используются МРТ и волюметрическая КТ [13, 14], 3D ультрасонография имеет хороший потенциал, позволяющий в будущем заменить эти архидорогие, сложные и связанные с ионизирующим излучением (КТ) методики. Это было бы весьма желательно, так как обследовать пациента после, например, трансплантации печени можно было бы многократно [15].
S. Wagner и соавт. [11], проведя 2D и 3D обследование 93 пациентов с хроническими диффузными заболеваниями печени, сравнили результаты, полученные благодаря использованию обоих методов. 3D превосходила рутинное ультразвуковое исследование в определении анатомического хода сосудов печени и желчных протоков. Данные 3D УЗИ оказались более информативными для диагностики синдрома Бадда-Киари, первичного склерозирующего холангита, но не давали дополнительной информации для дифференциальной диагностики хронических диффузных заболеваний печени.
По мнению G. Esmot [16], 3D УЗИ является превосходным методом, позволяющим осмотреть неровную бугристую поверхность печени при циррозе; получаемое изображение при этом весьма сходно с изображением при лапароскопии. Возможно также лоцирование серповидной связки (рис.1) и большого сальника (рис. 2).
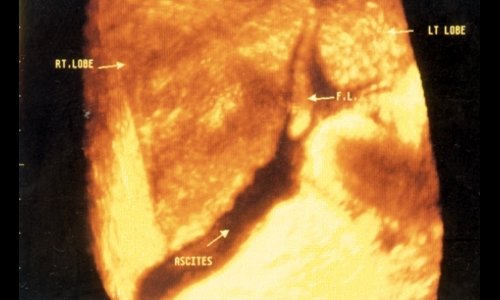
Рис. 1. Цирроз печени (неровный край печени, асцит) - круглая связка печени (F.L.) визуализируется между левой и правой долями.
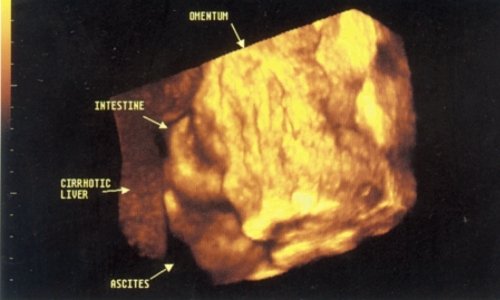
Рис. 2. Сальниковая поверхность печени, видимая у больного циррозом, осложненным асцитом.
К наиболее значимым достижениям методик, позволяющих визуализировать очаговые изменения печени, относится разработка 3D. H. Leiss и соавт. [17] доказали, что 3D дает в последовательных исследованиях более точные и повторяемые результаты измерений фокальных поражений печени, чем 2D и даже КТ. Это чрезвычайно важно, поскольку уровень планируемого лечения зависит от размера (объема) участка поражения. Так, количество спирта, необходимого для облитерации гепатоцеллюлярной карциномы у пациентов с циррозом печени, прямо пропорционально объему опухоли [18]. Поскольку результаты измерения объема при 3D сопоставимы с результатами при КТ, трехмерное УЗИ может применяться для динамического наблюдения пациентов (рис. 3) как альтернативная КТ диагностическая процедура [19]. 3D окажется полезным в наблюдении за больными с неоперабельными опухолями или, наоборот, при планировании объема резекции печени, определении топографии опухоли, больших печеночных структур, объема здоровой печеночной паренхимы, остающейся после резекции [20]. С помощью 3D можно определить направление иглы (проводника) при интервенционных процедурах, включая биопсию, аспирацию, введение терапевтических агентов [16]. Метод позволяет не только диагностировать, но и получать точные параметры объема эхинококковой кисты (рис. 4), производить ее аспирацию, алкоголизацию, а при необходимости, оценив эффект лечения, реаспирацию.
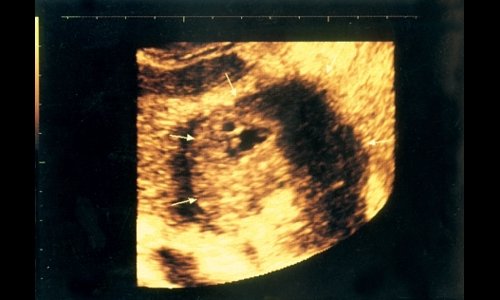
Рис. 3. Солидный очаг поражения в печени (гепатоцеллюлярная карцинома - стрелки) с центральной зоной распада.
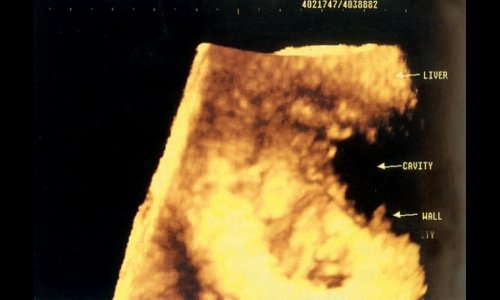
Рис. 4. Неровная стенка эхинококковой кисты печени.
Особой ценностью отличается возможность получать четкое изображение сосудов печени, в том числе опухолевых (характер васкуляризации опухоли является критерием ее роста и инвазивности, поэтому информация такого рода подчас становится определяющей). Альтернативной КТ-методикой, позволяющей добиться качественного изображения сосудистых структур без неблагоприятных воздействий на пациента, считается ультразвуковая ангиография [9]. Трехмерная силовая допплеровская ультрасонография воротной вены дает соответствующее четкое изображение портальной системы, если используется volume-rendered mode. Кроме того, оценки состояния шунтов портальной системы, в первую очередь трансъюгулярно-внутрипеченочнопортосистемного шунта, могут быть представлены в 3D-изображении более элегантно, особенно с применением 3D силового режима. Использование эхоконтрастного усиления при трехмерном сканировании опухолей предполагает многообещающие результаты, хотя до настоящего времени этот вопрос остается открытым [21].
Как показали G. Eamat и М. El Raziky [22], 3D-допплеровское исследование приносит неоценимую пользу диагностике причин хронических заболеваний печени у пациентов с асцитом в связи с веноокклюзионными заболеваниями, при которых наблюдается облитерация печеночной вены и минимальный нерегулярный ток крови. Таким образом, 3D исследование кровотока улучшает понимание геометрии и гемодинамики тока крови, а получаемые данные мало зависят от опыта оператора.
Селезенка
Спленомегалия - наиболее часто диагностируемое патологическое состояние селезенки. Очаговые ее поражения, обусловленные злокачественной или доброкачественной опухолью, а также кисты (рис. 5) легко распознаются с помощью 3D УЗИ [23]. Объем селезенки можно мгновенно автоматически рассчитать после получения серийных срезов, хотя, что очень важно, каждый срез имеет свою зону обзора вокруг органа, позволяя определить состояние прилежащих структур.
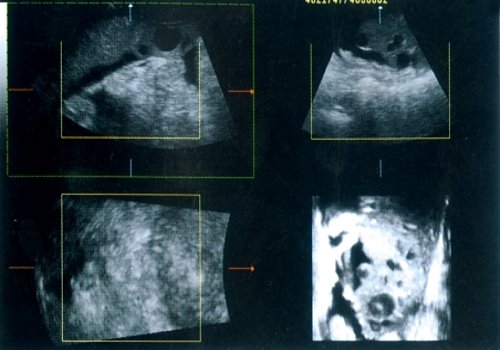
Рис. 5. Мультиплановый вид и интерактивное трехмерное изображение множественных кист селезенки в случае ее сосудистой аномалии.
3D УЗИ превосходит 2D при обследовании подобных селезенке органов, имеющих не ровную линейную форму, а округлую, позволяя определить все размеры и, в первую очередь, объем, наиболее достоверно [24]. Легко воспроизводимое высококачественное 3D-изображение селезенки в режиме силового допплера помогает правильной и быстрой диагностике ее инфаркта или травмы [21].
Поджелудочная железа
М. Sackmann и соавт. [25], применив 3D для обследования пациентов с неопластическими поражениями поджелудочной железы и калькулезным панкреатитом, пришли к заключению, что метод чрезвычайно полезен для определения степени распространенности опухоли и инвазии ей окружающих тканей (рис. 6). Камни поджелудочной железы также хорошо визуализируются.
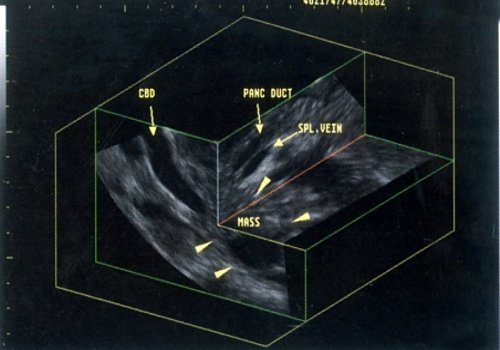
Рис. 6. Расширенные вследствие объемного образования в головке поджелудочной железы панкреатический (PANC DUCT) и общий желчный (CBD) протоки.
Трехмерное УЗИ помогает в решении вопроса о наличии перипанкреатической кисты вследствие формирования псевдокисты (что важно для динамического наблюдения за данной категорией пациентов) или опухоли, а также в прецизионном измерении внутрипанкреатических очагов поражения [16].
F. Selner и E. Machacek [26] сообщили о целесообразности определения объема опухоли для решения вопроса о возможности выполнения радикальной операции при периампулярном раке. Однако вопрос, дает ли 3D УЗИ более точные результаты измерений, чем КТ или ЭНДОУЗИ для данной категории пациентов, остается открытым.
Желчевыделительная система
Точное знание местоположения желчного пузыря необходимо в преддверии хирургического или радиологического лечения (рис. 7). В редких случаях аномалии расположения пузыря (левостороннее или внутрипеченочное) могут сделать лапароскопическую холецистэктомию трудновыполнимой. Подобные аномалии лучше диагностируются именно при 3D, создающей панорамное изображение желчного пузыря и окружающих органов и тканей.
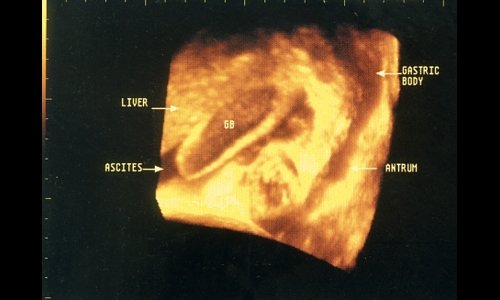
Рис. 7. Анатомические взаимоотношения между печенью, желчным пузырем (GB) и желудком у больного с асцитом.
Получение четкого изображения перипузырной области необходимо для определения наиболее подходящего оперативного доступа к пузырю при его карциноме или метастатическом поражении [23]. 3D УЗИ воспроизводит точные показатели объема пузыря, его сократительной активности (опорожнения), давая значительно меньшую, по сравнению с другими методами, погрешность при оценке объема [27] и при распознавании вида дискинезии (рис. 8).
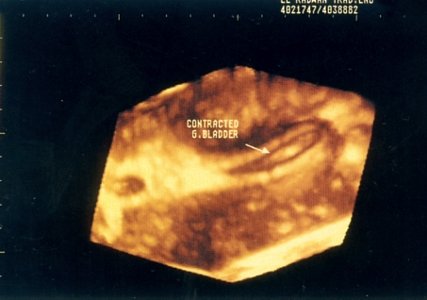
Рис. 8. Сократившийся желчный пузырь с утолщенной стенкой.
М. Sackmann и соавт. [25] доказали целесообразность применения 3D для изучения состояния стенок желчного пузыря, диагностики холестероза. Кроме того, в случаях портальной гипертензии (рис. 9) портосистемные коллатерали, расположенные в ложе пузыря, распознаются безошибочно [16].
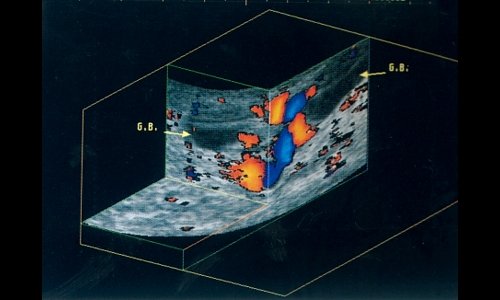
Рис. 9. Портальная гипертензия - коллатерали в стенке желчного пузыря.
S. Wagner и соавт. [11] считают 3D перспективной методикой для выявления патогномоничных изменений билиарного дерева в случаях первичного склерозирующего холангита.
В целом, следует подчеркнуть, что 3D-УЗИ полностью воспроизводит анатомо-топографические взаимоотношения общего печеночного протока и желчного пузыря, воротной вены, печеночной артерии и нижней полой вены (рис. 10).
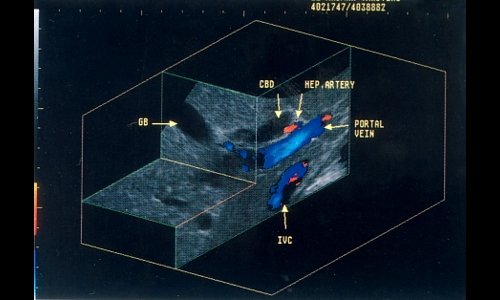
Рис. 10. Расширенный общий желчный проток (CBD) и его взаимоотношения с желчным пузырем (GB), портальной веной, печеночной артерией и НПВ (IVC). Цветной допплер.
Желудочно-кишечный тракт
Трансабдоминальная, а особенно эндоскопическая ультрасонография позволяют детально исследовать стенку желудочнокишечного тракта, близко расположенные органы и структуры. 3D-УЗИ, улучшая визуализацию, способствует установлению истинных топографических взаимоотношений, природы патологических образований. Она представляется клинически значимой методикой для диагностики локальных опухолевых поражений, а также диффузных изменений стенки желудка и кишечника, выявления внутрипросветной патологии [23].
Гидроколоносонография с применением трехмерной реконструкции может стать особо значимой процедурой для диагностики патологии полых органов. Было показано [22], что данный способ точнее, чем 2D-ультрасонография, так как позволяет получать множественные, пространственно строго ориентированные срезы. 3D помогает при определении совокупного объема опухоли и измерении ее протяженности (к примеру, расстояния от края опухоли прямой кишки до наружного сфинктера, что в конечном итоге влияет на выбор объема и способа выполнения предстоящего оперативного пособия) [23].
3D сделало технически возможным применение ультрасонографии для диагностики поражений пищевода, дополнив потенциальные возможности метода в установлении стадии рака [28]. Трехмерная реконструкция привносит неоценимый вклад в интерпретацию и количественный анализ ситуации, требующей установления стента при раке пищевода [29]. J. Lin и B. Goldberg [30] в предварительном исследовании продемонстрировали возможность трехмерной реконструкции данных, полученных при использовании ультратонких датчиков; при этом внутрипросветная 3D оказалась столь же точна, как и спиральная КТ при расчете объема опухоли пищевода.
В изучении моторики желудка и скорости его опорожнения 3D продемонстрировала in vitro высокую диагностическую ценность, позволяя рассчитывать уровень опорожнения точнее, чем 2D и давая возможность изучить внутрижелудочное распределение жидкой пищи в процессе исследования [31].
В клинической практике [16] 3D-гидрография желудка позволила, например, диагностировать малигнизированную язву на большой кривизне желудка и доказать вовлечение региональных лимфатических узлов (рис. 11).
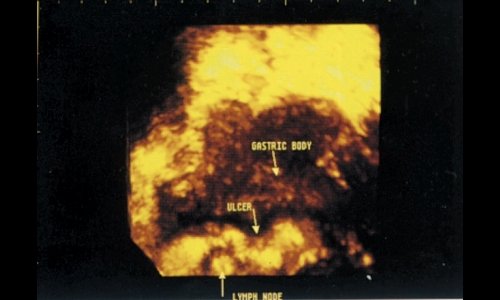
Рис. 11. Трехмерная гидросонография - язва большой кривизны желудка с вовлечением лимфатических узлов.
При прогрессировании неопластического процесса и развитии асцита петли тонкого кишечника, висцеральная брюшина, большой и малый сальник могут быть успешно визуализированы (рис.12).
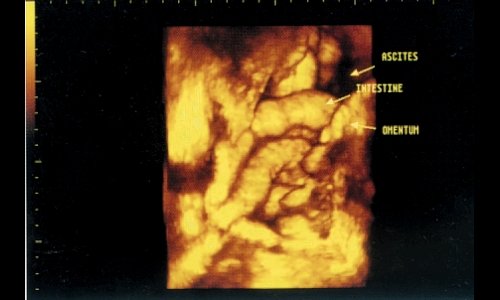
Рис. 12. Ровная поверхность кишечных петель у пациента с циррозом печени, осложненным асцитом.
N. Hunerbein и соавт. [31], изучив роль 3D-эндосонографии в процессе обследования 100 пациентов с раком прямой кишки, пришли к убеждению, что метод позволяет визуализировать участки поражения в различных проекциях, на разнообразных срезах, что практически невыполнимо при традиционной двухмерной эхографии.
Асцит
Как и в случае 2D наилучшие 3D-срезы были получены от анатомических или патологических структур с жидкостным содержимым или структур, окруженных жидкостью (гидроцеле, асцит).
G. Esmat и М. El Raziky (22), проанализировав результаты обследования 39 пациентов с асцитом, пришли к заключению, что свободная жидкость "помогала" в проведении 3D-сканирования, так как содействовала визуализации поверхности петель кишечника и париетальной брюшины. Кроме того, авторы предприняли попытку определить этиологию асцита. Так, им удалось описать патогномоничные признаки туберкулезного асцита, при котором практически во всех случаях визуализировались увеличенные внутрибрюшные лимфатические узлы. 3D позволила в 80% случаев провести дифференциальный диагноз между туберкулезной и злокачественной природой лимфоаденопатии (рис. 13, 14, 15).
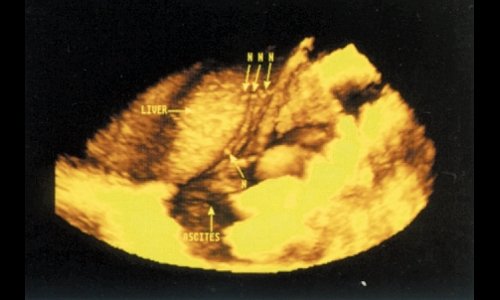
Рис. 13. Печень, покрытая туберкулезными узелками (N) при туберкулезном асците.
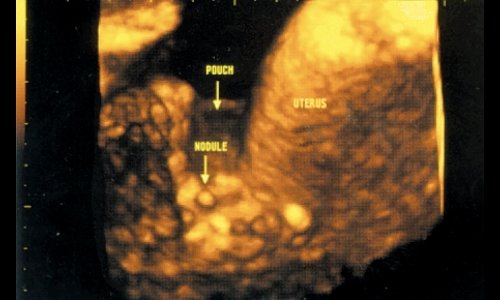
Рис. 14. Туберкулезные узелки в пространстве Дугласа. Узелки имеют характерный гипоэхогенный контур.
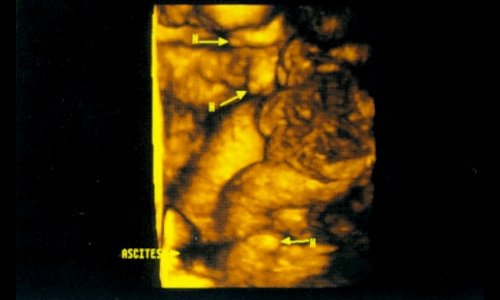
Рис. 15. Множественные различного размера узелки на висцеральной брюшине при злокачественном асците.
Необходимо подчеркнуть, что сфера клинического применения 3D-УЗИ неуклонно расширяется, поскольку метод обеспечивает анатомическую реконструкцию зоны интереса (органа, структуры), получение точнейших результатов при измерении объема, проведение анализа таких ультразвуковых срезов, визуализация которых невозможна при рутинном сканировании. При сохранении информации в полном объеме возможно ее многократное воспроизведение без ограничений во времени и в отсутствие пациента (он не испытывает дискомфорта и излишнего беспокойства).
Сомнительные, неоднозначные результаты сканирования можно повторно тщательно анализироваить и изучать с привлечением специалистов, дающих независимую интерпретацию сохраненного объемного изображения.
Перспективным представляется применение 3D-УЗИ, в первую очередь, в онкологии, поскольку совершенствование компьютерных программ вычисления объема, внедрение трехмерного силового допплеровского анализа васкуляризации опухоли, визуализация ее поверхности в трех измерениях, а в дальнейшем - повышение разрешающей способности метода в связи с разработкой новых эхоконтрастов, дающих большую продолжительность перфузии, улучшат не только первичную диагностику неопластических поражений, но и наконец, позволят проводить дифференциальную диагностику между злокачественной и доброкачественной природой образований.
Введение трехмерной реконструкции при ЭНДОУЗИ, особенно при применении высокочастотных ультратонких датчиков, способно дать морфологическую оценку состояния стенки пищеварительного тракта.
3D-УЗИ имеет потенциал для использования не только в крупных региональных центрах, но и на ранних этапах оказания медицинской помощи. Появление нового оборудования будет стимулировать и расширять области применения 3D. Свидетельство тому - прорыв, совершенный компанией "Медисон" в 2000 г. На рынок выпущен ультразвуковой сканер SA-9900, создающий трехмерную реконструкцию в реальном масштабе времени.
Литература
- Levine R.A., Weyman A.C., Handschmacher M.D. Three-dimensional echocardiography: techniques and applications // Am. J. Cardiol, 1992; 69: 121-134.
- Kitney R., Moura L., Straughan K. 3-D visualisation of arterial structures using ultrasound and voxel modeling // Int. J. Card Imaging, 1989; 4: 135-143.
- Schrank E., Phillips D.J., Morritz W.E. A triangulation method for the quantitative measurement of arterial blood velocity magnitude and direction in humans // Ultrasound Med. Biol., 1990; 16: 499-599.
- Kossoff G. Three-dimensional ultrasound - technology push or market pull? // Ultrasound Obstet Gynecol, 1995; 5: 217-218.
- Thomas R., Dolores H. Interactive acquisition, analysis and visualisation of sonographic volume data // Int. J. Imaging Technol, 1997; 35: 40-47.
- Kurjak A., Kupesic S., Anic T., Kosuta D. Threedimensional ultrasound and power Doppler improve the diagnosis of ovarian lesions // Gynecol Oncol, 2000; 76: 28-32.
- Kurjak A., Kos M. Three-dimensional ultrasonography in prenatal diagnosis / In: Chervenak F.A., Kurjak A., eds. Fetal Medicine, Carnforth, UK: Parthenon Publishing, 1999: 102-108.
- Nelson T.R. Three-dimensional imaging // Ultrasound Med. Biol. 2000, 26, Supplement 1, p. 35-38.
- Гажонова В.Е., Сокольская Е.В., Зубарев А.В. Трехмерная эхография в оценке полости матки после различных внутриматочных вмешательств // Эхография, 2000. - Т. 1. - N 3. - С. 248-252.
- Cosgrove D. Why do we need contrast agents for ultrasound? // Clin. Radiol., 1996, 51 Supplement 1: 1-4.
- Wagner S., Gebel V., Bleck J., Manns M. Clinical application of three-dimensional sonography in hepatobiliary diseases // Bildgebung, 1994; 61: 104109.
- Gilja O., Hausken T., Perstand A., Odegaard S. Measurements of organ volumes by ultrasonography // Proc. Inst. Mech. Eng. 1999; 213: 247-259.
- Chari R., Baker M., Sue S., Meyers W. Regeneration of a transplanted liver after right hepatic lobectomy // Liver Transpl. Surg. 1996; 2: 233-234.
- Caldwell S., de Lange E., Gaffey M. Accuracy and significance of pretransplant liver volume measured by magnetic resonance energy // Liver Transpl. Surg. 1996; 2: 438-442.
- Henderson J., Macky G., Kutner M., Noe B. Volumetric and functional liver blood flow are both increased in the human transplanted liver // J. Hepatol 1993; 17: 204-208.
- Esmat G. Three-dimensional ultrasonography in hepatogastroenterology // In: Kurjiak A., Kupesic S., eds. Clinical application of 3D sonography, NewYork - London, Parthenon Publ. Group, 2000: 235241.
- Liess H., Roth C., Umgelter A., Zoller W. Improvements in volumetric quantification of circumscribed hepatic lesions by 3D-US // Z Gastroenterol 1994; 32: 488-492.
- Alexander D., Unger E., Seeger S. Estimation of volumes of distribution and intra-tumoral ethanol concentrations by CT scanning after percutaneous ethanol injection // Acad Radiol 1996; 3: 49-56.
- Lang H., Wolf G., Prokop M., Nuber B., Weiman A. 3-D sonography for volume determination of liver tumor - report of initial experiences // Chirurgie 1999; 70: 246-250.
- Lang H., Wolf G., Procop M., Nuber B., Weimann A. Volumetry of circumscribed liver changes with 3D US in comparison with 3D CT // Langenbecks Arch. Chir. Suppl. Kongressbd, 1998; 115: 1478-1480.
- Downey D., Fenster A. Vascular imaging with a 3D power Doppler system // Am J Roentgenol, 1995; 156: 665-668.
- Eamat G., El Raziky M. Etiological diagnosis of ascites by 3D ultrasonography // Medical Imaging International, 2000; 10: 18-19.
- Nelson T., Downey D., Pretorius D., Fenester A. Abdomen. Three-dimensional Ultrasonography. Philadelphia, PA: Lippincott Williams and Wilkins, 1999: 151-167.
- De Odoricio I., Spaulding K., Pretorius D. Normal splenic volumes estimated using 3D ultrasonography // J. Ultrasound Med. 1999; 18: 231-236.
- Sachmann M., Pauletzki J., Zwiebel F., Holl J. Three-dimensional ultrasopnography in hepatobiliary and pancreatic diseases // Bildgebung 1994; 61: 100-103.
- Sellner F., E. Machacek. The importance of tumor volume in the prognosis of radically treated periampullary carcinomas // Eur. J. Surg. 1993; 159: 95-100.
- Pauletzki J., Sackmann M., Holl J., Paumgartner G. Evaluation of gallbladder volume and emptying with a novel three-dimensional ultrasound system: comparison with the sum-of-cylinders and the ellipsoid methods // J. Clin. Ultrasound 1996; 24: 277-285.
- Kallimans G., Garra B., Tio T. The feasibility of three-dimensional endoscopic ultrasonography: a preliminary report // Gastrointest Endosc 1995; 41: 235-239.
- Molin S. Usefullness of three- dimensional reconstruction for interpretation and quantitative analysis during stent depolyment in esophageal cancer / Presented at the 8th International Congress of International Ultrasound, Copenhagen, September 1, 1999: 56.
- Lin J., Goldberg B. 2-D and 3-D endoluminal ultrasound: vascular and nonvascular applications // Ultrasound Med Biol 199; 25: 159-173.
- Gilja O., Detmer P., Jong J. Intragastric distribution and gastric emptying assessed by three-dimensional ultrasonography // Gastroenterology 1997; 113: 3839.
- Hunerbein N., Dohmoto M., Haensch W., Schlag P. Evaluation and biopsy of recurrent rectal cancer using 3D endosonography // Dis Colon Rectum 1996; 39: 1378-1378.
- Cesarani F., Isolato G., Capello S., Pianchi S. Tridimensional ultrasonography / First clinical experience with dedicated devices and review of the literature // Radiol Med (Toronto) 1999; 97: 256-264.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Публикации по теме
- Ультразвуковая диагностика фитобезоаров желудка. Клиническое наблюдение - Бурков С.Г.
- Ультразвуковая диагностика псевдоопухолевой формы актиномикоза печени - Дергачев А.И.
- Трехмерная эхография органов пищеварения (аналитический обзор) - Бурков С.Г.
- Методологические основы применения ультразвуковой томографии в малоинвазивном лечении очаговых поражений селезенки - Борсуков А.В.
- Пролиферирующая фибролипома паренхимы почки в сочетании с множественными доброкачественными образованиями печени - Буйлов В.М.

