Клиническая трактовка результатов ультразвуковых исследований печени
Рубрика: Эхография в педиатрии

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
Ультразвуковые исследования (УЗИ) - часто первые в ряду диагностических поисков при подозрении на патологию печени, определяя выбор других методик. Совершенствование ультразвуковых диагностических технологий привело к тому, что в ряде случаев стало возможным отказаться от других радиологических исследований. Но это же повышает ответственность специалиста, требует клинически интерпретировать полученные результаты, не сводя описание к фиксации "эхопозитивных" и "эхонегативных" образований. Основная доля УЗИ в поликлинических условиях приходится на органы брюшной полости. И печень - первое, что в этом случае пытается визуализировать специалист. Заболевания печени могут быть заподозрены по предъявляемым жалобам, клинической картине, лабораторным данным, но нередко они выявляются случайно. Последнее относится, прежде всего, к детям, у которых доля врожденной патологии выше, чем у взрослых. Резервные возможности печени невероятны, поэтому задача врача - выявить патологию, прежде чем она станет клинически значимой.
Общие положения
Эмбриогенез печени и ее сосудов, анатомия. В раннем онтогенезе печень, желчный пузырь и желчный проток возникают как единый вырост (печеночный дивертикул) в каудальном отделе переднего отдела протокишки. Это образование растет вентрально в septum transversum, представляющую собой мезодерму между развивающимся сердцем и средним отделом кишки. Зачаток печени растет очень быстро, в первые 10 нед занимая бoльшую часть брюшной полости. В этот период размеры правой и левой долей печени одинаковые, но за счет оксигенированной крови из печеночной вены правая доля быстро обгоняет в размерах и массе левую. С 6-й недели печень является органом кроветворения, а с 12-й недели синтезирует желчь. Маленький каудально расположенный отросток на печеночном дивертикуле дает начало желчному пузырю, а его ножка - пузырному протоку. Из тяжика, идущего от печеночного и пузырного протока к двенадцатиперстной кишке, формируется общий желчный проток. В эмбриональный период кровь поступает в печень по пупочной вене, проходящей по свободному краю ligamentum falciforum в левую ветвь воротной вены. Эта часть v. portae соединяется с печеночной веной через ductus venosus, далее кровь поступает в правое предсердие. Таким образом, ductus venosus представляет собой большой венозный шунт в обход печени, благодаря которому основная часть крови из плаценты поступает непосредственно в сердце. Это единственный путь, по которому может быть проведен катетер. Если катетер при зондировании пупочной вены попадает в правую ветвь воротной вены, развиваются тромбоз, облитерация и портальная гипертензия. После рождения ребенка пупочная вена облитерируется и превращается в круглую связку печени (ligamentum teres). Ductus venosus трансформируется в ligamentum venosum. В первые часы после рождения эти структуры можно визуализировать как каналикулярные. Позднее ligamentum teres видна как плотная структура, распространяющаяся от левой части воротной вены. Если возрастает внутрипеченочное давление (при циррозе), круглая связка печени реканализируется. Портальная кровь начинает оттекать от печени к пупку, в результате чего варикозно расширяются околопупочные вены (caput medusae). Возможны аномалии нижней полой вены, но они крайне редки. Среди этих редких пороков чаще встречается леворасположенная нижняя полая вена, самостоятельно впадающая в правое предсердие через коронарный синус. Возможно недоразвитие печеночного сегмента нижней полой вены с дренажом крови через систему vv. azygos et hemiazygos. Печеночная вена самостоятельно дренируется в правое предсердие. Возможно удвоение нижней полой вены, при этом левая вена значительно меньше по диаметру, чем правая. Знание этих особенностей особенно важно в детской практике, так как существенная часть педиатрической патологии является врожденной.
Особенности локации (автор выражает благодарность компании Medison за предоставленную аппаратуру. Рис. 2-4 также предоставлены этой компанией). Начиная рабочий день, проверьте состояние аппаратуры. Убедитесь, что набор датчиков позволяет вам выполнить все исследования. Добейтесь, чтобы в направлении были приведены показания к проведению исследования, сформулированы цель и задачи, представлены основные клинические, лабораторные и инструментальные результаты. В беседе с родителями и ребенком (если он может формулировать свои проблемы) уточните все неясные моменты. Посмотрите на пациента как врач, а не как исполнитель при аппарате. Критически оцените прежние данные, сформулируйте свои показания. Имейте четкий план работы: период, в течение которого ребенок спокоен и позволяет выполнять процедуры, недолог.
Для УЗИ печени, селезенки, верхней части живота наиболее приемлем конвексный датчик. Угол обзора при этом большой, а деформация ближнего поля минимальная. Линейный датчик применим для визуализации мелких структур. Допплерография необходима при подозрении на сосудистые аномалии, гемангиомы.
Сканирование лучше проводить в положении ребенка на спине при максимальном вдохе или выдохе (в зависимости от особенностей ребенка). При вдохе легкие оттесняют печень, желчный пузырь и селезенку ниже реберной дуги, смещают толстую кишку, увеличивая акустическое окно. У детей старшего возраста иногда требуется осмотр через межреберные промежутки или в боковой проекции. Межкостальный доступ является оптимальным при расположении печени глубоко в подреберье. Чтобы избежать ложных заключений при нестандартных доступах, исследователь должен помнить об изменяющейся топографии органа, нарушениях обычного соотношения с ним почек, нижней полой вены, кишечника. Если в процессе осмотра печени возникли сомнения относительно состояния желчного пузыря или желчевыводящих путей, а ребенок подготовлен недостаточно, лучше закончить исследование и повторить его после подготовки. Важнейшее преимущество УЗИ перед другими методами неинвазивной визуализации (рентгенография, магнитнорезонансная - МРТ или компьютерная томография - КТ, ретроградная холангиопанкреатография - РХПГ) состоит в возможности повторять исследование так часто, как это диктуется клиникой.
Эхографическая картина нормальной печени. В норме печень ребенка гомогенна. Характер обработки сигнала выбирают в зависимости от цели исследования (рис. 1а, 1б). Капсула печени тонкая, эхогенная. Эхогенность паренхимы печени выше, чем паренхимы коры почек. Медуллярная ткань почек темнее паренхимы печени. Вентральный край печени тонкий, острый. При увеличении размеров печени он закругляется. Частым показанием к проведению УЗИ является подозрение на увеличение размеров печени. Существует много формул для расчета размеров печени, в том числе волюметрические. Последние используются в основном в научных целях или в специализированных клиниках. Размеры и конфигурация печени достаточно вариабельны. При рутинных исследованиях размеры печени можно оценивать качественно. Правая доля печени распространяется до нижнего полюса почки, но если существует риделевская долька (вариант нормы), то несколько ниже. У детей 1 года жизни левая доля при поперечном сканировании распространяется за срединную линию, у старших детей - до аорты. При гепатомегалии левая доля простирается вплоть до селезенки, сдвигая ее вниз. Смещение селезенки может служить причиной ошибочного заключения о спленомегалии. Таким образом, печень состоит из правой и левой долей. Кроме того, имеется и хвостатая доля. Доли печени делятся на сегменты. Упрощенно - правая доля имеет передний и задний сегменты (граница - правая печеночная вена). Левая доля состоит из медиального и латерального сегментов (граница - левая печеночная вена). Каждый сегмент имеет свое кровоснабжение. Поэтому при синдроме Бадда-Хиари (обструкция печеночных вен) сегменты увеличиваются в размерах, их эхогенность возрастает. Знание сегментов печени важно и для точной локализации объемных образований.
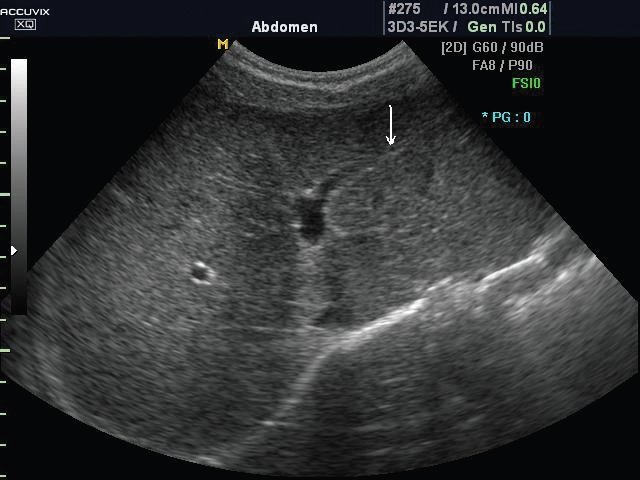
а) Эхограмма печени 12-летнего подростка в обычном режиме. Обратите внимание, что даже в 12-летнем возрасте круглая связка печени (стрелка), отходящая от левой части воротной вены, имеет каналикулярный вид (просвет внутри).
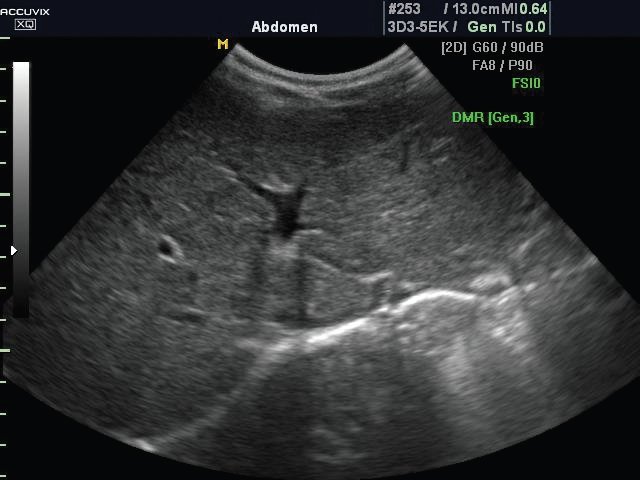
б) Эхограмма печени этого же подростка в режиме МРТ. Множественные мелкие эхосигналы, происходящие, вероятнее всего, от соединительной ткани, убраны. Хорошо визуализируются собственно паренхима и сосуды.
Печеночные вены уносят кровь из печени в нижнюю полую вену и правое предсердие. Допплерографическая кривая трехфазная. В диастолу волна направлена к печени, в систолу две короткие невысокие волны имеют обратное направление. Факторы определяющие амплитуду волн:
- повышение плотности печени снижает амплитуду;
- нормальная флюктуация изменяется при сердечной недостаточности, расширении нижней полой вены;
- внепеченочные образования и асцит, сдавливая печень и вены, изменяют колебания допплеровской кривой.
Воротная вена приносит кровь от кишечника и селезенки. В воротах печени она делится на правую и левую ветви. Общий диаметр вены варьирует в зависимости от возраста, положения тела (стоя или лежа), глубины дыхания. Для практических целей можно считать, что у детей до 10 лет диаметр v. portae составляет около 8 мм, после 10 лет - 10 мм (см. таблицу). Стенки их внутрипеченочных отделов высокоэхогенны и хорошо выделяются на фоне паренхимы. Плотность стенок используется как стандарт для оценки плотности паренхимы печени. При хронической патологии печени ее плотность приближается к плотности стенок внутрипеченочных ветвей портальной вены. Допплерографическая волна монофазная, колебания определяются дыханием и объемом сердечного выброса. Из аномалий воротной вены известны ее агенезия, удвоение и предуоденальная портальная вена. Последняя нередко сочетается с обратным расположением внутренних органов, кольцевидной поджелудочной железой, стенозом двенадцатиперстной кишки или другими аномалиями.
| Возраст, годы | 1 | 3 | 5 | 7 | 9 | 11 | 13 | 15 |
|---|---|---|---|---|---|---|---|---|
| Медиана, мм | 3,3 | 4,5 | 5,8 | 7,7 | 8,0 | 8,2 | 8,7 | 8,9 |
| Пределы колебаний, мм | 2,9-5,7 | 3,5-6,9 | 4,3-7,6 | 4,5-8,5 | 4,9-9,4 | 5,1-10,0 | 5,6-10,1 | 5,7-10,6 |
Печеночная артерия несет оксигенированную кровь от аорты. Пульсация допплерографической кривой соответствует сердечному циклу.
Частные проблемы
Изменения печени у новорожденных и детей 1-го года жизни аналогичны ее изменениям у детей более старшего возраста, но их спектр несколько различен. Гепатомегалия - самая частая причина эхографических исследований у новорожденных.
Причины и эхографическая картина.
- Метаболические заболевания печени (гликогенозы и т.д.). Печень увеличена в размерах, эхогенность ее повышена.
- Застойная сердечная недостаточность. Эхогенность печени повышена. Вены печени и нижняя полая вена расширены.
- Врожденные гепатиты. К моменту рождения печень обычно имеет повышенную эхогенность.
- Гемангиомы и гемангиоэндотелиомы - самые частые локальные образования в печени у детей 1 года, в 80% случаев они манифестируют в первые 6 мес жизни. Образования могут быть единичными, множественными или диффузными. Множественные мелкие гемангиомы гипоэхогенны, солитарные гемангиомы обычно гиперэхогенны, как и у взрослых. Одновременно очаги могут обнаруживаться в селезенке. В 13-17% случаев отмечается кальцификация. Кавернозные гемангиомы могут выглядеть как грубые, неправильной формы кистозные образования. Требуется тщательный допплерографический анализ для выявления питающих и отводящих сосудов, артериовенозных шунтов.
- Нейробластома (4S нейробастома). На нее приходится до 50% всех случаев опухолей новорожденных. Медиана возраста к моменту установления диагноза - 22 мес. До 80% всех случаев выявляются в период отдаленных метастазов. Эхографически увеличенная печень выглядит как инфильтрированная метастазами, причем первичный очаг в надпочечниках выявляется всего в 40-50% случаев.
Диффузные изменения печени у детей могут быть вызваны как системными, так и локальными патологическими процессами. Эхографическая картина в большинстве случаев не специфична, сочетаясь с гепатомегалией и нередко желтухой. Диффузные изменения печени обычно протекают в сочетании с гепатомегалией. Исключение составляет цирроз печени, который в далеко зашедших стадиях приводит к уменьшению размеров печени. Кроме того, диффузные изменения печени обычно сочетаются с ее гиперэхогенностью. Исключения представляют острый отек печени и острый гепатит. На фоне гипоэхогенной паренхимы печени особенно четко прорисовываются стенки вен портальной системы.
При диффузном изменении печени требуется определить ее размеры, характер поверхности (ровный, бугристый) и края (острый, закругленный), состояние селезенки, поджелудочной железы, почек, сосудов печени, лимфатических узлов.
Жировая инфильтрация печени - результат накопления жира в гепатоцитах. Эхогенность паренхимы возрастает, рисунок вен портальной системы стерт. Контраст между паренхимой печени и почкой резкий. Выраженность изменений зависит от степени жировой инфильтрации. Жировая инфильтрация наблюдается в исходе химио- и стероидной терапии, при мальнутриции, ожирении, муковисцидозе, тирозинемии, болезни Вильсона - Коновалова, гликогенозах и т.д. Жировая инфильтрация может быть и очаговой. Очаг жировой инфильтрации может быть любых размеров и формы, что симулирует опухоль.
Цирроз - не самостоятельное заболевание, а исход многих заболеваний печени, на фоне которого возможно развитие гепатоцеллюлярной карциномы. При остром процессе вначале фиксируется жировая инфильтрация. Позднее появляется зернистость паренхимы. Процесс может быть микронодулярным, при котором изменяется вся паренхима печени, и макронодулярным, при котором в измененной паренхиме видны узлы диаметром 1 см и более. Паренхима гетерогенна за счет гипоэхогенных очагов регенерации. Фиброз формируется как тяжи соединительной ткани, поэтому аттенуация луча меньше, чем при жировой инфильтрации. Печень уменьшается в размерах, компенсаторно увеличиваются левая и хвостатая доли. При макронодулярном типе цирроза край печени становится неровным. Повышенная плотность печени приводит к ее ригидности и нарушению кровотока. Обычная трехфазная волна по печеночным венам может превратиться в флюктуирующую или монофазную. В качестве дополнительного признака цирроза указывают на асцит (рис. 2).
Муковисцидоз передается по аутосомно-рецессивному типу и регистрируется среди европеоидов с частотой 1:3000-1:2500 живорожденных. Причина заболевания - нарушение транспорта ионов из эпителиальных клеток экзокринных желез с формированием густого секрета, обструкции полых органов, присоединением инфекции и развитием склероза. Поражение печени характеризуется крупноочаговым фиброзом.
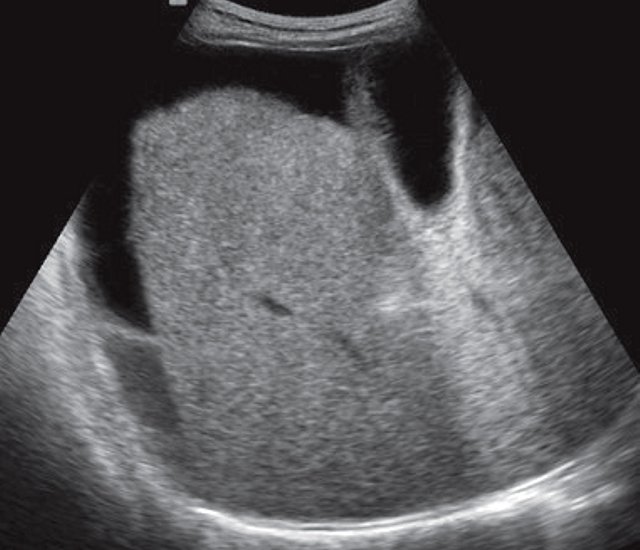
Рис. 2. Эхограмма печени при циррозе.
Портальная гипертензия - неспособность портальной системы свободно проносить кровь в печень или из печени. Возникающее избыточное давление приводит к увеличению селезенки и появлению варикоза вен портальной системы, открытию коллатералей. Базис диагностики - выявление спленомегалии, варикоза вен, коллатералей. Выделяют три варианта портальной гипертензии:
- подпеченочная - самый частый вариант в детском возрасте. Может быть идиопатической, результатом катетеризации пупочной вены, восходящей инфекции (омфалит; аппендицит с флебитом верхней брыжеечной артерии, впадающей в v. portae, и тромбозом последней);
- внутрипеченочная. Цирроз с обструкцией внутрипеченочных ветвей v. portae;
- надпеченочная. Вено-окклюзивная болезнь - частичная или полная окклюзия малых печеночных вен, обычно являющихся резервными для больших вен, с блокадой кровотока через печень. У детей обычно возникает после трансплантации гематопоэтических стволовых клеток (костного мозга), радио- или химиотерапии. Как синоним часто используется термин "синдром Бадда-Хиари", хотя это и не совсем верно. Под термином "синдром Бадда-Хиари" принято понимать блокаду кровотока по печеночным венам при гиперкоагуляции. Поэтому термин вено-окклюзивная болезнь более универсальный. Окклюзия сосудов обычно начинается с внутрипеченочных венул. Вены, впадающие в нижнюю полую вену, какое-то время могут быть еще сохранены, что может послужить причиной ложноотрицательного диагноза. Эхографическая диагностика затруднена. Определяются асцит, утолщенные стенки желчного пузыря, атипичный поток крови по воротной вене. При тяжелой вено-окклюзивной болезни печеночные вены имеют малый диаметр, плохо визуализируются.
Эхографическая картина зависит от уровня обструкции. При подпеченочной портальной гипертензии v. portae практически не визуализируется, зато хорошо видна ее кавернозная трансформация (портальная кавернома). Кавернозная трансформация - множество мелких коллатералей в обход тромбированной v. portae. Она развивается в ближайшие 1-3 нед после тромбоза. По данным допплерографии, портальный кровоток угнетен, он может быть обратным. Открываются коллатеральные каналы. Всего описано не менее 20 таких каналов, но имеют клиническое значение и легко опредеяляются при УЗИ следующие.
- Пищеводные и желудочные вены выявляются легко и чаще всего. При лонгитудинальном сканировании тут же слева от аорты располагается гастроэзофагеальный переход. При цветном допплеровском сканировании обнаруживается варикозное расширение вен вокруг нижней части пищевода и по нижней поверхности печени. Часть вен находится в стенке пищевода, другие - по ее поверхности. Последние служат источником кровотечений и хорошо выявляются при эзофагогастроскопии.
- Спленоренальные коллатерали формируются от ворот селезенки и проводят кровь в левую почечную вену. Эхографически выглядят как дополнительный сосуд между селезенкой и левой почкой в сочетании с расширенной почечной веной. Это оптимальный шунт: кровотечений из него не бывает.
- Параумбиликальные коллатерали у детей обнаруживаются редко и только в случаях цирроза. Они берут начало от левой ветви воротной вены и простираются к пупку. Отводят кровь через вены эпигастрия в наружную подвздошную. Именно эти вены и формируют caput medusae. Другим признаком открытия параумбиликальных коллатералей является утолщение малого сальника. Для выявления этого феномена проводят лонгитудинальное сканирование на уровне чревной артерии. В норме расстояние от чревной артерии до нижней поверхности печени (толщина малого сальника) составляет 1-1,5 диаметра аорты. При наличии коллатералей в малом сальнике его толщина составляет 1,7 и более диаметра аорты.
- Артериопортальный шунт соединяет печеночную артерию и систему воротной вены. Его гемодинамическая значимость сильно варьирует. При большом сбросе возникают портальная гипертензия и сердечная недостаточность за счет большого ударного объема левого желудочка (резкое сокращение времени возврата крови в сердце). Возникает при опухолях, сосудистых аномалиях, как исход травмы при неудачной пункции печени.
Очаговые изменения печени могут быть доброкачественными и злокачественными. К доброкачественным очаговым поражениям печени относят кисты, абсцессы (гнойные, грибковые), гидатидную болезнь (эхино-, альвеококкоз), гематомы, мезенхиальную гамартому, гемангиому.
Кисты истинные в детском возрасте встречаются редко. Они могут быть при поликистозной болезни, поэтому при обнаружении кисты в печени, а тем более множественных кист необходимо обследование всех паренхиматозных органов. Истинная киста анэхогенна, стенка ее не визуализируется, хорошо виден феномен усиления звука за кистой. Кисты обычно выявляются случайно, они бессимптомны, пока не достигают больших размеров, не смещают и не сдавливают структуры печени. Мелкие кисты пасполагаются по периферии печени и значительно лучше выявляются при КТ, чем с помощью УЗИ. Вторичные кисты формируются в исходе гематомы или абсцесса. Такие кисты имеют неоднородное содержимое и толстую стенку.
Абсцессы пиогенные, грибковые, амебные имеют общие эхографические проявления. Пиогенные и грибковые абсцессы типичны для детей с первичным иммунодефицитом (особенно хронической гранулематозной болезнью), ВИЧ-инфекцией, на фоне химиотерапии. Абсцессы обычно локализуются в задней части правой доли, могут быть множественными или единичными. Эхографически могут выглядеть как:
- мелкие эхонегативные образования;
- феномен "бычьего глаза", т.е. круглое эхонегативное образование с эхоплотным центром;
- мишеневидная печень. Так как абсцессы могут быть очень мелкими, требуется использовать датчики с высокой частотой излучения.
Гидатидная болезнь печени - эхинои альвеококкоз. Заболеваемость среди детей увеличилась в 2,9 раза ("Распределение паразитарной заболеваемости по территории РФ" на сайте www.rusmedserv.com). Эхографически при эхинококкозе обнаруживают кисту с отчетливой стенкой и очень тонким эхонегативным ободком вокруг нее. Дочерние гидатиды внутри определяются как мелкие эхопозитивные плавающие образования. Капсула старого эхинококкового пузыря может кальцинироваться. (Наиболее частую локализацию эхинококка в печени пытаются объяснить несоответствием размеров паразита и диаметра сосудов, представляя печень как сито. На самом деле эхинококк избирательно фиксируется в печени потому, что его капсула построена из пятичленных сахаров, а пентозный цикл интенсивнее всего идет в печени, т.е. эхинококк фиксируется там, где есть оптимальные условия для его развития. И то, что пентозный цикл интенсивнее всего идет в печени, тоже имеет большой биологический смысл: печень, являясь едва ли не основным депо гликогена (построенного из шестичленных сахаров, с ней конкурируют только мышцы), свой энергетический обмен обеспечивает пятичленными сахарами, не растрачивая углеводы, потребляемые другими органами. Точно так же эритроцит, переносящий кислород, сам живет за счет анаэробного обмена. Тромбоцит, чья задача погибнуть в нужный момент, не является живой клеткой, а только осколком клетки. Таких примеров много. И если после всех этих, казалось бы, узких медицинских знаний мы не приходим к мысли о высшей целесообразности, то как мы услышим голос, если не хотим слышать его.)
Гематома печени должна быть исключена при любой травме, особенно травме живота и автомобильной. В случаях недавней травмы гематома выглядит как солидное эхогенное образование. Постепенно за счет некроза формируется псевдокиста.
Гемангиома печени - самое частое доброкачественное опухолеподобное образование печени. Небольшая гемангиома за счет множества мелких кист и септ, создающих эффект отражения звука, выглядит как эхогенное образование (рис. 3). При больших гемангиомах возможны эпизоды их тромбирования с дефицитом тромбоцитов на периферии и склонностью к геморрагиям.
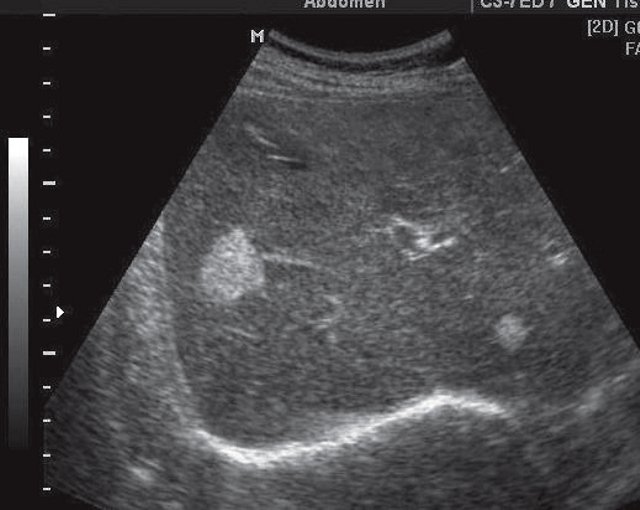
Рис. 3. Гемангиома печени.
Мезенхимальная гамартома обычно выявляется у детей первых 2 лет жизни и дебютирует как безболевое образование в брюшной полости. На нее приходится 7-8% всех опухолей печени у детей. Гамартома возникает из мезенхимы перипортального тракта, внутри опухоли обнаруживают гепатоциты, компоненты желчных ходов, кровеносных сосудов, мезенхимы, но без лимфатической ткани. За счет скопления жидкости в мезенхиме возникают кисты. Различное соотношение ткани и кист привело к выделению двух вариантов гамартомы: преимущественно стромальный и преимущественно кистозный. Эхографическая картина мезенхимальной гамартомы чрезвычайно вариабельна. Гамартома хорошо отграничена от печеночной ткани, обычно располагается в правой доле, большая по размерам, содержит множество септальных кист.
Аденомы печени у детей редки. Они встречаются у детей с гликогенозами (особенно I типа), дефицитом глюкозо-6-фосфатазы, галактоземией, анемией Фанкони, апластической анемией (в последнем случае - леченной андрогенами). Эхографически регистрируется солитарное гипоэхогенное образование, в ряде случаев - изоэхогенное.
Фокальная нодулярная гипертрофия - первичная опухоль печени без капсулы. Представляет собой гиперпластически регенерирующие узлы из гепатоцитов, Купферовских клеток, разделенных фиброзными тяжами. Характерным для фокальной нодулярной гипертрофии является наличие центрального звездчатого поля (рубца) с лучеобразно распространяющимися от него пролиферирующими желчными протоками и кровеносными сосудами. Фокальная нодулярная гипертрофия чаще выявляется у женщин, но может обнаруживаться и у детей любого возраста. Эстрогены ускоряют рост образования. Эхографически опухоль обнаруживается случайно, выглядит как хорошо ограниченное образование, которое может быть разной степени гиперэхогенным или изоэхогенным. В 50% случаев регистрируется гало. Образование может располагаться на ножке на краю печени.
Внутрипеченочные кальцинаты встречаются редко (рис. 4). Они типичны для инфекционного процесса, особенно гранулематозного (туберкулез, бруцеллез, гистоплазмоз, кокцидиомикоз), цитомегаловирусов, токсоплазм, пневмоцист, гидатидной болезни, гемангиомы, гемангиоэндотелиомы, злокачественных опухолей (кальцинаты по типу радиальных лучей характерны для гепатобластомы), травмы, кальцинации сосудов, болезни Кароли.
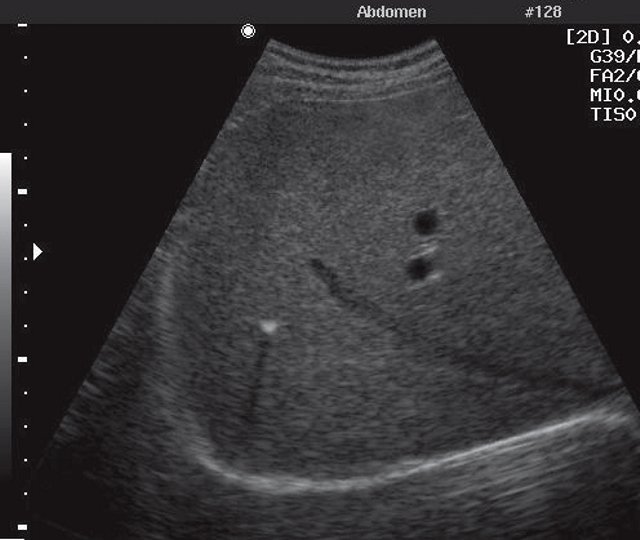
Рис. 4. Кальцинат в паренхиме печени с типичным феноменом акустической тени.
Злокачественные опухоли печени занимают по распространенности 3-е место после опухоли Вильмса и нейробластомы. На них приходится 5% всех злокачественных опухолей детского возраста. 65-70% опухолей печени у детей злокачественные. Все опухоли печени манифестируют как объемные образования брюшной полости. Роль эхографии - уточнить локализацию образования, представить данные для предварительного диагноза и создать условия для следующих этапов диагностики (МРТ, ангиография и т.д.).
Гепатобластома - самая частая опухоль печени. На нее приходится 47-50% всех злокачественных опухолей печени детского возраста. Происходит из фетальных гепатоцитов. Средний возраст пациентов на момент диагноза - 18 мес (пределы колебаний - от 0 до 3 лет). Девочки болеют чаще. Манифестирует с увеличения живота, гепатомегалии, нередко - с симптомов острого живота. Возможны остеопения с переломами костей, гипогликемия, гиперхолестеринемия. В 90% случаев повышен уровень α-фетопротеина. Эхографически опухоль выглядит как достаточно четко ограниченное образование, чаще массивное. Внутри опухоли могут быть очаги кальциноза и некрозов. По данным допплерографии, опухоль хорошо васкуляризирована. Гепатобластома быстро прорастает в печеночную артерию, нижнюю полую вену или охватывает их в виде плотной муфты (рис. 5, а, б).
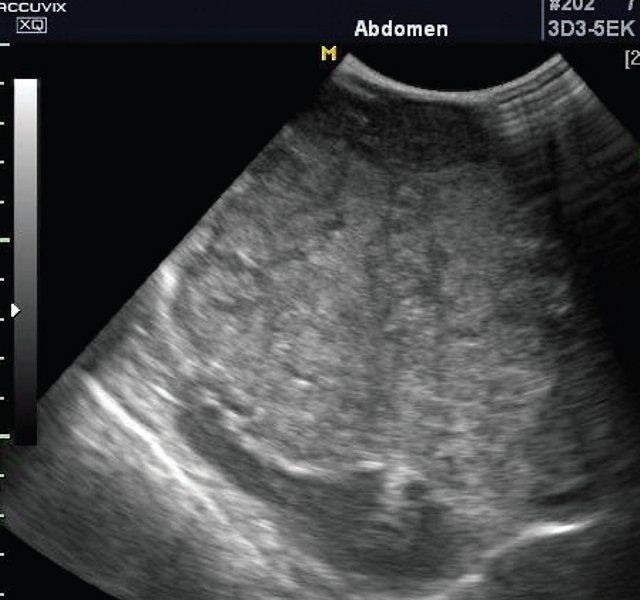
а) Эхограмма опухоли печени в обычном режиме. Опухоль визуализируется недостаточно четко.
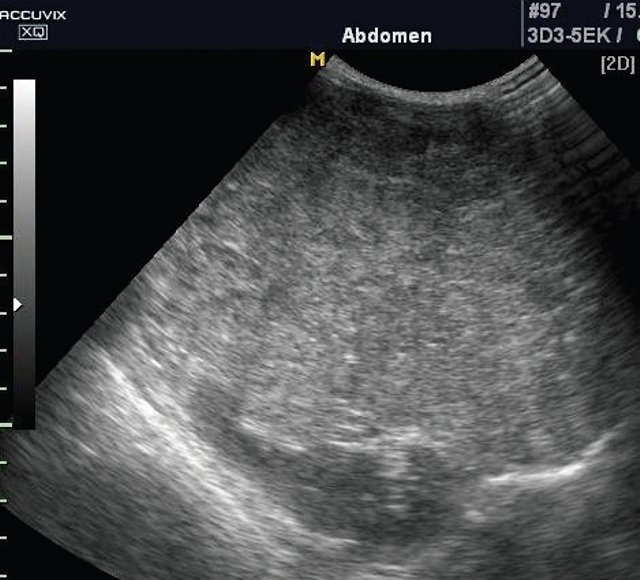
б) Эхограмма опухоли печени в режиме МРТ. Структура опухоли и ее границы видны достаточно четко.
Гепатоцеллюлярная карцинома у детей гистологически полностью аналогична таковой у взрослых. Клетки опухоли гистологически очень сходны с нормальными гепатоцитами, что затрудняет диагностику. Поражает детей в возрасте 10-12 лет. На нее приходится 20% всех злокачественных опухолей печени у детей. Предрасполагающими факторами являются билиарная атрезия, семейный холестаз, гепатит В, ожирение, гликогеноз I типа, наследственная тирозинемия. Манифестирует с гепатомегалии, желтухи, анорексии, существенного повышения уровня α-фетопротеина. Эхографически опухоль может быть гипо- или изоэхогенной, мультифокальной, солитарной (гигантских размеров), диффузной (поражающей всю печень). Иногда вокруг опухоли регистрируется тонкий эхонегативный ободок-гало, являющийся эхографическим отражением капсулы. Возможен центральный некроз опухоли с образованием ложных кист.
Недифференцированная эмбриональная саркома (злокачественная мезенхимома) - редкая опухоль, состоящая из недифференцированных веретеновидных клеток и поражающая в основном подростков. На нее приходится 5% всех злокачественных опухолей печени у детей. Проявляется, как и все опухоли печени, с объемного образования брюшной полости, лихорадки, истощения, при этом концентрация α-фетопротеина не изменяется. Эхографически опухоль может быть представлена как солидными массами с плотными кальцинатами и феноменом акустической тени, так и кистозными образованиями с множественными внутренними перегородками. Эти псевдокистозные полости образуются за счет кровоизлияний и некрозов. Ангиографически подтверждается гиперваскуляризация опухоли.
Метастазы. Печень в результате сложностей своего кровоснабжения как никакой другой орган предрасположена к появлению в ней метастазов. Опухолевые клетки заносятся обычно с потоком крови через портальную систему (например, от опухолей кишечника), через печеночную артерию (опухоли легких или молочной железы), по лимфатической системе. Реже метастазирование происходит по перитонеальной поверхности (рак яичников). В последнем случае первоначальный метастаз локализуется субсерозно. В противоположность этому при гематогенном метастазировании очаги располагаются центрально. Небольшие периферические очаги эхографически выявляются с большим трудом, так как они могут быть скрыты тенью ребра или артефактом ближнего поля. Метастазы могут быть гипер-, гипоэхогенными (наиболее гипоэхогенны метастазы лимфомы, они множественные, очень нежные), изогенными, неоднородными (за счет некроза или кровоизлияний). Но говорить о происхождении метастазов на основании их акустических свойств по данным УЗИ невозможно. Стадия заболевания должна уточняться по данным МРТ или КТ.
Метастазы при УЗИ обычно солидные, края очерчены нечетко. Большие метастазы могут содержать в центре жидкость (некроз) или муцин (метастаз рака яичников). В результате химиотерапии в метастазе могут появляться кальцинаты. В случаях изменения текстуры печени (расширение внутрипеченочных желчных ходов, последствия химиотерапии, цирроз как исход гепатита) выявление метастазов очень затруднено. По данным допплерографии сосудов, внутри метастазов нет. В больших метастазах по периферии могут появляться редкие мелкие сосуды. При наличии асцита в далеко зашедших стадиях онкологического заболевания удается выявить метастазы на поверхности сальника или брюшины.
Заключение
УЗИ используется для диагностики и мониторинга заболеваний печени, а также при лечении с применением инвазивных процедур под контролем ультразвука. Одновременно следует помнить, что печень изменяется при патологии многих других органов, например при заболеваниях почек, и установить причины изменения морфологии и функции печени без тщательного системного анализа невозможно. Для этого наряду с исследованием желчного пузыря, поджелудочной железы не забывайте сканировать ретроперитонеальное, поддиафрагмальное пространства и малый таз. Если Вы не будете работать рядом с аппаратом как врач, то при любых самых золотых звездах на погонах Вы не поднимитесь выше фельдшера.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Публикации по теме
- Эхография в дифференциальной диагностике поражения лимфатических узлов опухолевого и неопухолевого генеза - Делягин В.М.
- Ультразвуковые исследования малого таза у девочек и девушек-подростков - Делягин В.М.
- Клиническая трактовка результатов ультразвуковых исследований печени - Делягин В.М.
- Эхокардиография в исследовании центральной гемодинамики у детей, находящихся на программном гемодиализе - Нугманова А.М.
- Эхография селезенки у детей и подростков - Делягин В.М.


