Ангиомиолипомы почек
Рубрика: Эхография в урологии
Введение
Ангиомиолипома (АМЛ) является самой распространенной доброкачественной опухолью почек. Впервые была описана в 1902 г. W. Fischer. Согласно определению, АМЛ почки представляет собой высокоактивную сосудистую опухоль, как правило доброкачественную, состоящую из клеток эндотелия, гладких мышц и жировой ткани (рис. 1).
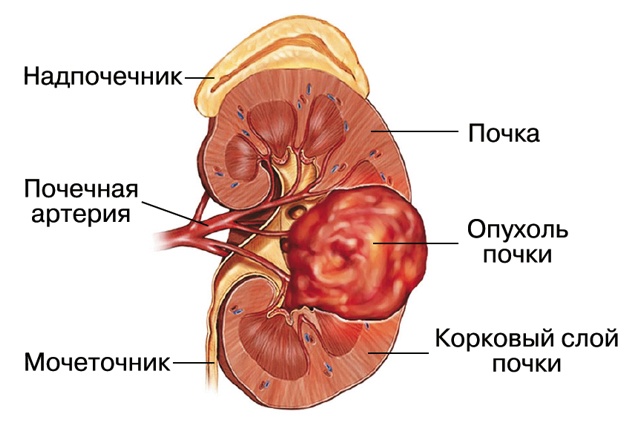
Рис. 1. Ангиомиолипома почки (графическое изображение).
В 80–90% случаев образования являются самостоятельным заболеванием. В остальных случаях ассоциированы с другой патологией, например туберозным склерозом или лимфангиолейомиоматозом.
Туберозный склероз – аутосомно-доминантное генетическое заболевание, приводящее к появлению доброкачественных опухолей (гамартом) во внутренних органах, повреждению кожи. Комплекс туберозного склероза (болезнь Бурневилля–Прингла) включает в себя ангиофибромы лица, околоногтевые фибромы, гамартому сетчатки, корковые туберы и субэпендимальные узлы, множественные АМЛ почки [5, 6].
Лимфангиолейомиоматоз – полисистемное заболевание, характеризующееся прогрессирующей кистозной деструкцией легочной ткани, поражением лимфатической системы и появлением опухолевидных образований (ангиомиолипом) органов брюшной полости с генетической основой [4].
Этиология и патогенез развития АМЛ до сих пор остаются малоизученными. К факторам, предрасполагающим к развитию спорадических АМЛ, причисляют женский пол, возраст, беременность, гормональные изменения (динамика роста АМЛ во время беременности могут свидетельствовать о гормонозависимой природе опухоли) [1–3].
Частота встречаемости АМЛ составляет от 12 до 30 случаев на 100 тыс. населения.
Общая распространенность в мире предположительно может составлять от 0,3 до 3,0% по данным разных авторов [1–3], у женщин АМЛ встречается в 2–3 раза чаще, чем у мужчин.
У пациентов, страдающих туберозным склерозом, в 90% случаев выявляются множественные двусторонние АМЛ почек. В свою очередь, до 20% всех выявляемых АМЛ сопровождают туберозный склероз [5, 6].
Более 90% АМЛ – асимптомные, а самым серьезным осложнением у таких пациентов является кровоизлияние, встречающееся менее чем в 2% случаев.
Классификация
Широкая распространенность АМЛ в клинической практике привела к многочисленным попыткам создать разнообразные классификации, среди которых были попытки систематизировать опухоль по чувствительности к гормонам, наличию признаков инвазии, дебюту заболевания и др.
В настоящее время в рутинной практике используется классификация по известному этиологическому фактору:
- Спорадический тип. Является наиболее распространенным, составляет 75–80% всех случаев заболевания. Образование обнаруживается при случайном ультразвуковом исследовании (УЗИ) органов мочевыделительной системы, характеризуется бессимптомным течением.
- Наследственный тип. Включает опухоли, сопровождающие генетические заболевания. Наиболее часто встречается синдром Бурневилля–Прингла (туберозный склероз) – аутосомно-генетическая патология из группы факоматозов. Она сопровождается множественными двусторонними АМЛ почек и обусловливает примерно 20% случаев таких образований.
- Тип с невыясненной этиологией. Диагностируется редко, не чаще 1–2% случаев. К данному типу относятся множественные спорадические новообразования, опухоли с инвазивным ростом.
Гистологическая классификация: типичная (трехфазная), атипичная (монофазная). Большинство АМЛ содержат все три компонента (расширенные кровеносные сосуды «-ангио»; гладкомышечные клетки «-мио» и зрелые адипоциты «-липо») и, таким образом, являются трехфазными опухолями. Однако в некоторых АМЛ превалирует какой-то один компонент (монофазные опухоли).
Радиологическая классификация. Согласно радиологической классификации, АМЛ почки может быть с большим содержанием жира, минимальным его содержанием и без выявляемого жира.
Клиническая картина заболевания
Как правило, спорадические АМЛ являются случайной находкой при УЗИ в возрасте от 30 лет и старше. Иногда рост опухоли может сопровождаться неинтенсивными болями со стороны поражения. Причем в отличие от других доброкачественных опухолей, при АМЛ болевой синдром не связан с давлением опухоли на ткань почки. Предполагают, что боль возникает в результате кровоизлияния внутри самой АМЛ.
Клинические проявления чаще всего связаны со спонтанным забрюшинным кровотечением, которое может привести к шоку у трети пациентов.
Диагностика
Лучший диагностический критерий – обнаружение солидного гетерогенного образования с макроскопическим жировым компонентом в коре почки у взрослых.
Обзорная рентгенография, экскреторная урография, сцинтиграфия, ангиография в настоящее время используются при подозрении на АМЛ чуть реже, поскольку имеют крайне низкую специфичность.
При экскреторной урографии небольшая АМЛ проявляется наличием рентгенопрозрачного дефекта, и если образование имеет большие размеры, то определяется деформация собирательной системы.
Ангиография может быть полезна при наличии в АМЛ увеличенного сосудистого компонента: выявляется гиперваскулярное образование с множественными хаотично расположенными извитыми сосудами и мешковатыми псевдоаневризмами.
Среди лучевых методов диагностики АМЛ почки УЗИ используют как базовый метод, включая дуплексное исследование, контрастное УЗИ, УЗ-эластографию.
Возможно ли обойтись лишь УЗИ у пациента с АМЛ почки, не проводя дополнительных исследований (МСКТ, МРТ, биопсии)? Согласно одному из метаанализов, чувствительность УЗИ составляет 99%, однако специфичность – лишь 43%. Необходимо учесть, что более чем в 50% случаев как АМЛ может выглядеть почечно-клеточный рак (ПКР). Поэтому КТ или МРТ обязательны для постановки диагноза АМЛ.
КТ с контрастированием и МРТ с контрастированием являются основными методами диагностики АМЛ. Биопсия используется в спорных случаях для определения тактики ведения и объема оперативного вмешательства и не является рутинным методом.
Одной из проблем диагностики АМЛ с низким содержанием жира является то, что лучевые характеристики образования могут не отличаться от ПКР. Это относится как к КТ, так и МРТ: ни динамическое контрастирование, ни изображения с химическим сдвигом, ни диффузионно-взвешенные изображения и карты коэффициента измеряемой диффузии не дают надежной информации.
Ультразвуковое исследование
При классической картине АМЛ в почке определяется гиперэхогенное (по отношению к паренхиме почки) образование с четкими контурами, не дающее акустической тени, округлой формы, акустическая плотность которого соответствует плотности жировой ткани, структура опухоли однородная во всех отделах (рис. 2, 3).
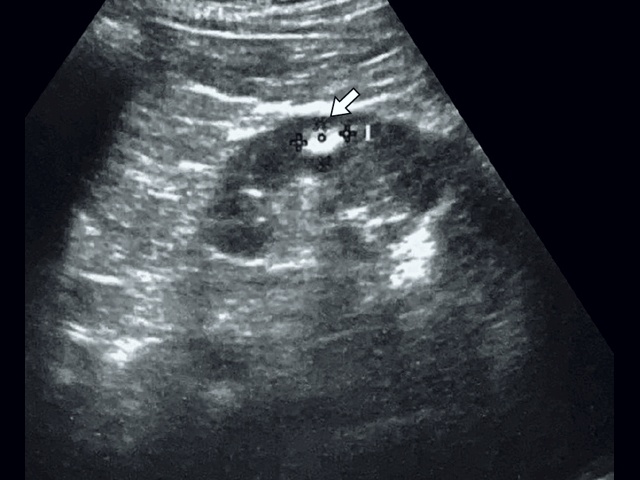
В паренхиме почки визуализируется гиперэхогенное образование с четкими контурами, небольшого размера, без акустической тени.
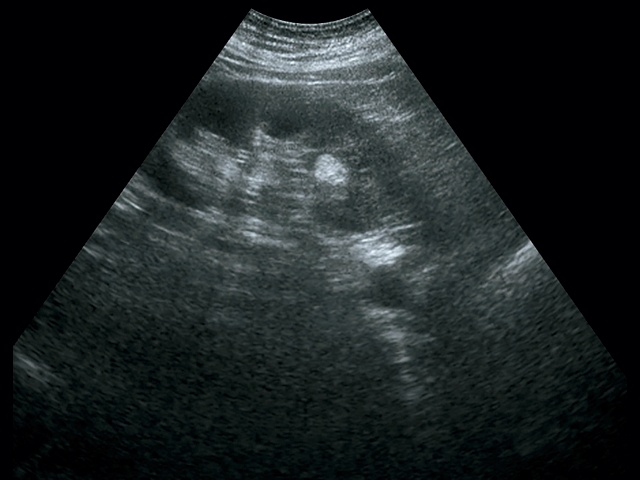
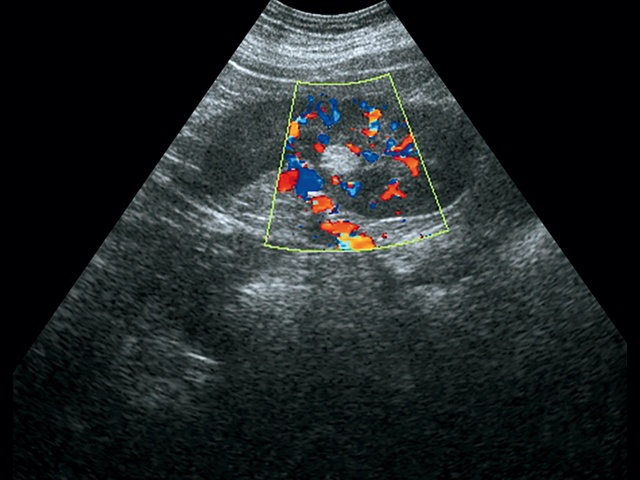
В паренхиме почки визуализируется гиперэхогенное образование с четкими контурами, небольшого размера, без акустической тени.
а – режим серой шкалы; б – режим ЦДК.
Цветовая допплерография при УЗИ направлена на обнаружение псевдоаневризм в виде овоидных или округлых структур, заполненных цветовым потоком, находящихся внутри или рядом с АМЛ. Энергетическая допплерография показывает, что большинство АМЛ обладает «внутриопухолевой очаговой картиной»: центральный внутренний поток, не распространяющийся к краям опухоли. Напротив, в большинстве случаев ПКР небольших размеров обладает смешанной периферической и проникающей картиной: поток определяют в центре опухоли с распространением к ее периферии.
Кроме того, АМЛ с минимальным содержанием жира обладает структурой от изо- до слегка гипоэхогенной, а ПКР, в свою очередь, при небольших размерах может быть гиперэхогенным.
При проведении дифференциальной диагностики будет иметь значение пол, возраст пациента, наличие травм в анамнезе.
Динамическое наблюдение требует контроля за изменением размеров образования, появлением регионарных лимфатических узлов.
Мультиспиральная компьютерная томография
При МСКТ без контрастного усиления определяется солидное гетероэхогенное образование с четкими контурами, растущее из коры почки, с макроскопическим содержанием жира (достоверный признак жира – плотность ткани составляет – 10 HU или ниже). Также патогномоничным признаком является наличие «желобка» – АМЛ представляет собой треугольный или прямоугольный желобовидный дефект в коре. Для типичных АМЛ характерна гипоаттенуация (недостаточное ослабление излучения при КТ) (рис. 4–6). В то же время для АМЛ с низким содержанием жира характерна гетерогенная изоаттенуация и гиператтенуация, для АМЛ практически без жировых компонентов – гомогенная гиператтенуация.
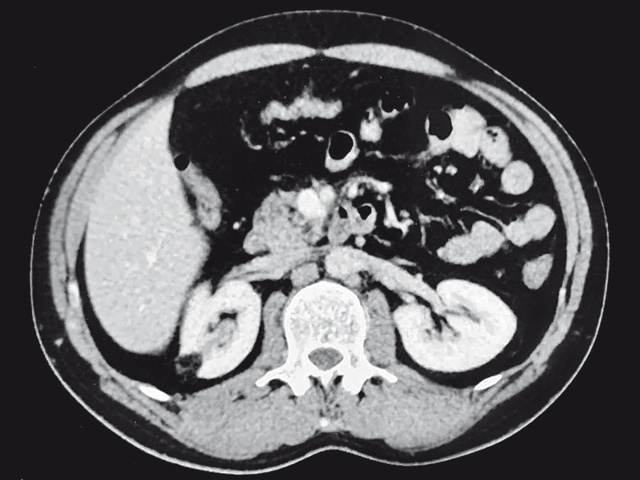
Определяется характерное образование, исходящее из коркового слоя почки, желобовидной формы, неоднородное, с макроскопическим присутствием жира, плотностью около – 53 HU.
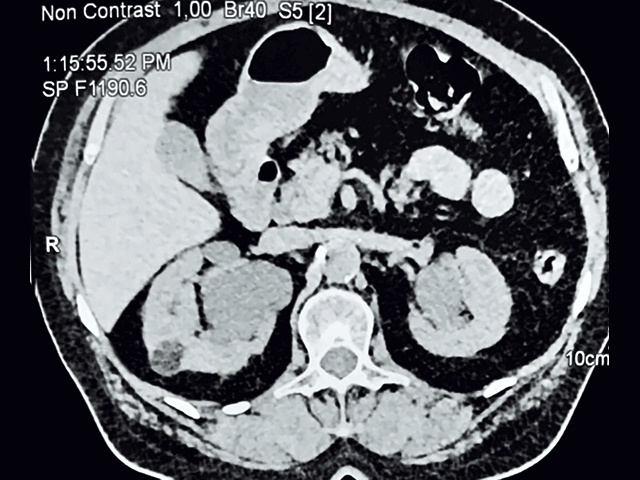
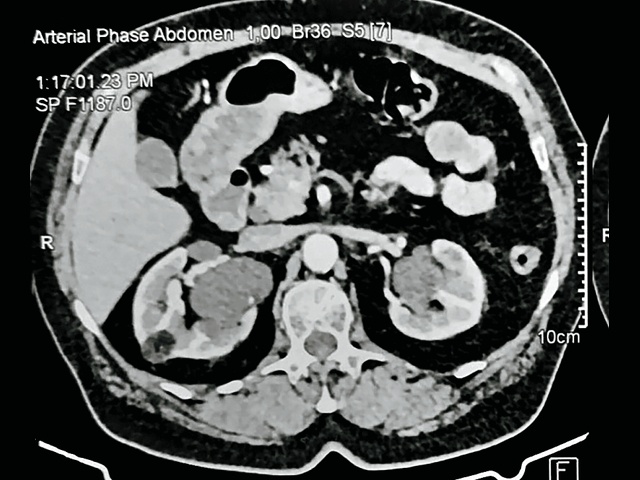
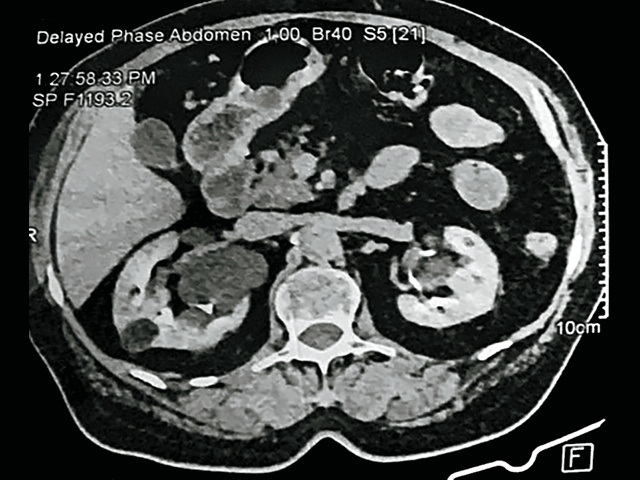
На границе верхней и средней трети по задней поверхности правой почки определяется очаговое образование овальной формы размерами 21 х 14 мм, частично выбухает за почечный синус, негомогенно жировой структу-ры, плотность – 70 HU, с усилением до – 30 HU в последующие фазы.
а – нативная фаза; б – артериальная фаза; в – отсроченная фаза.
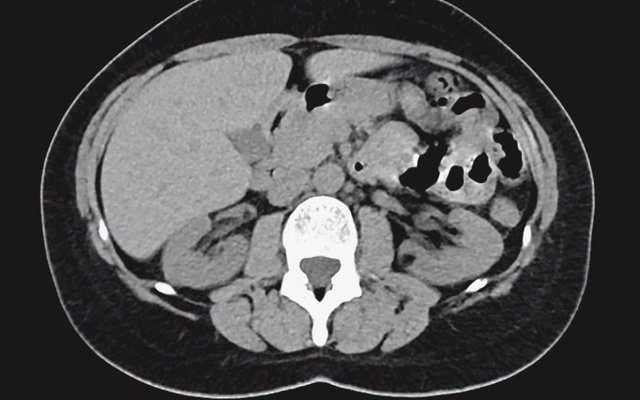
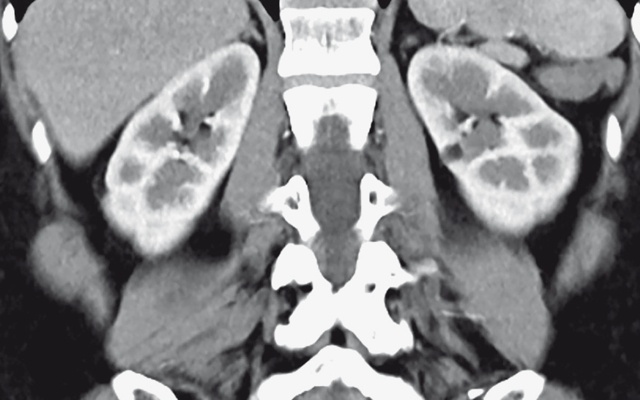
В среднем сегменте левой почки ближе к медиальной поверхности определяется образование размерами 11 х 12 мм, жировой плотности, без усиления – 110 HU.
а – нативная фаза; б – артериальная фаза; в – венозная фаза.
5% всех АМЛ содержит минимальное количество жира, гиперденсны и не могут быть достоверно распознаны на КТ.
В качестве иллюстрации приводим результаты обследования пациентки Д., 47 лет. При диспансерном осмотре при УЗИ выявлены множественные гиперэхогенные образования от 3 до 7 мм, по типу АМЛ (рис. 7)
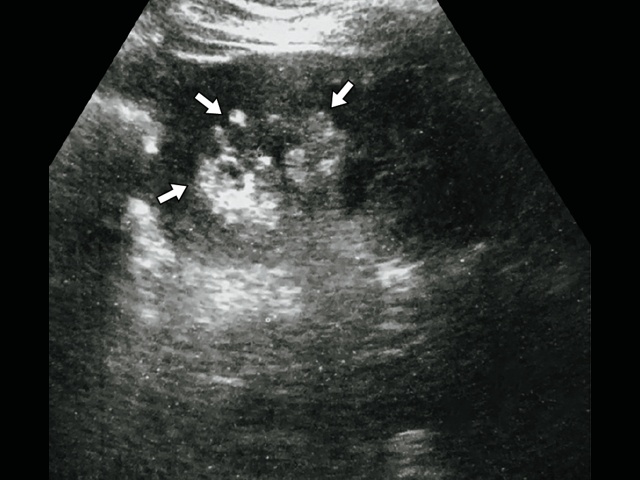
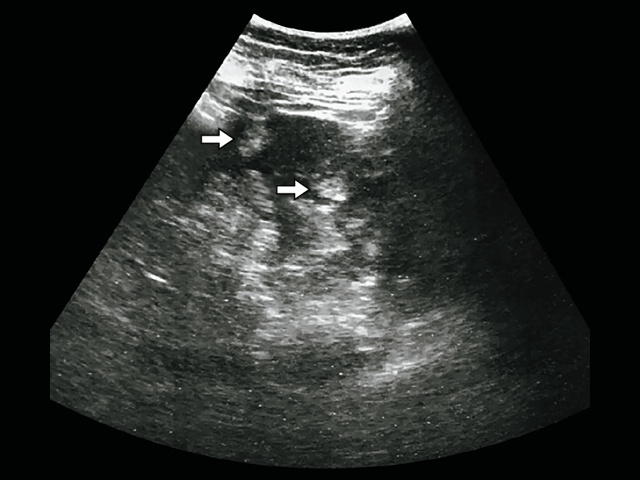
В обеих почках множественные гиперэхогенные образования различного диаметра с четкими контурами, без эффекта усиления.
Проведенная МСКТ полностью подтвердила полученные данные (рис. 8).
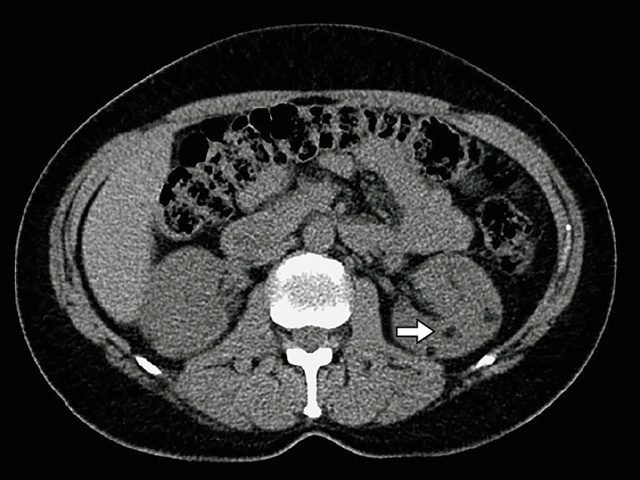
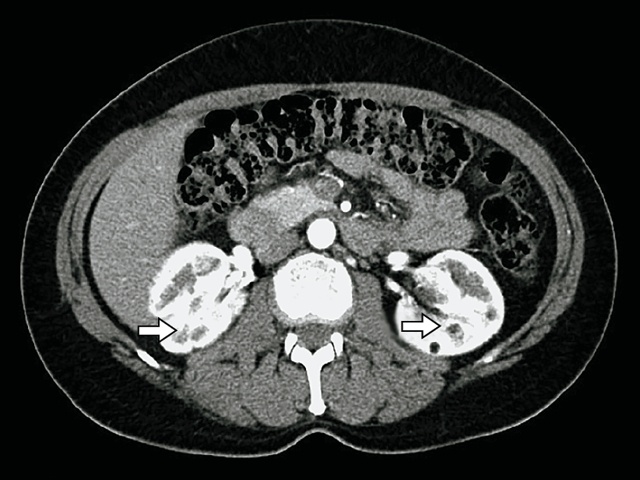
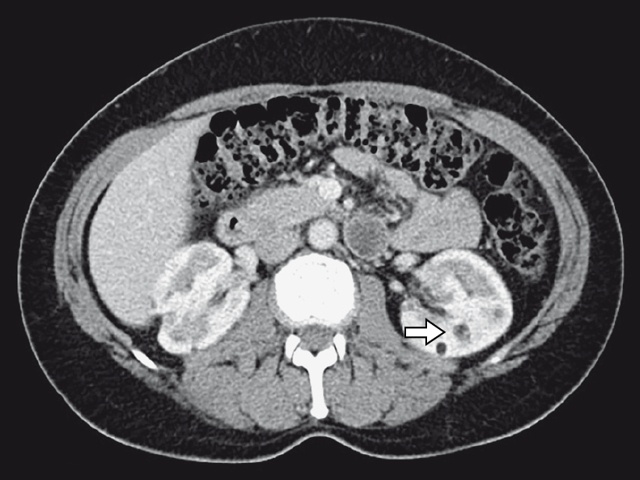
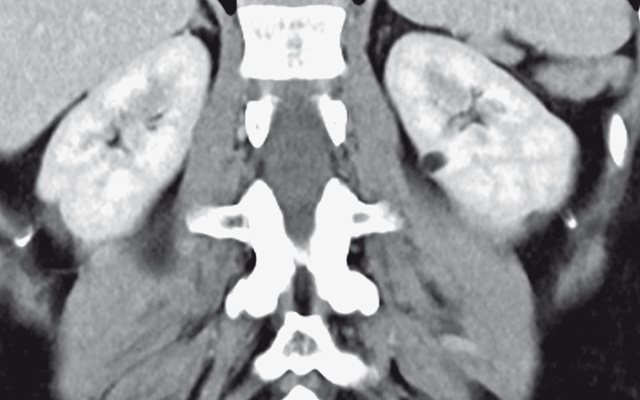
В обеих почках в корковом веществе определяются многочисленные образования с ровным контуром, размерами от 3 до 7 мм в диаметре, жировой плотности – 80 HU.
а – нативная фаза; б – артериальная фаза; в – венозная фаза.
Магнитно-резонансная томография
В диагностике АМЛ почек МРТ по точности эквивалентна МСКТ. АМЛ обладает гетерогенной картиной изменения сигнала: разнообразное соотношение сосудов, мышц и жира или макроскопическая картина скопления жира: Т1-гипоинтенсивность и Т1-гиперинтенсивность без подавления сигнала от жира. Однако эта Т1-гиперинтенсивность не явялется специфической характеристикой и может присутствовать в ПКР и геморрагических кистах.
Также возможно наличие артефакта химического сдвига и артефакта индийских чернил.
Артефакт химического сдвига обусловлен различиями между резонансными частотами жира и воды. Это приводит к чередованию высоких и низких сигналов в направлении частотного кодирования на противофазном изображении.
Этот внефазовый эффект отмены между жиром и водой приводит к появлению артефакта индийских чернил – искусственно созданная черная линия, расположенная на стыке жира и воды, приводящая к резкому очертанию мышечно-жировой границы, является специфичным признаком АМЛ.
В качестве иллюстрации приводим результаты обследования пациентки П., 39 лет, с диагнозом АМЛ почек.
Не менее 5 лет назад при случайном УЗИ выявлены АМЛ почек, было рекомендовано динамическое наблюдение. При обследовании в динамике установлено значительное увеличение размеров АМЛ слева. Учитывая высокую вероятность спонтанного разрыва опухоли, пациентка госпитализирована в отделение урологии в плановом порядке, где ей проведена селективная эмболизация левой почечной артерии (рис. 9).
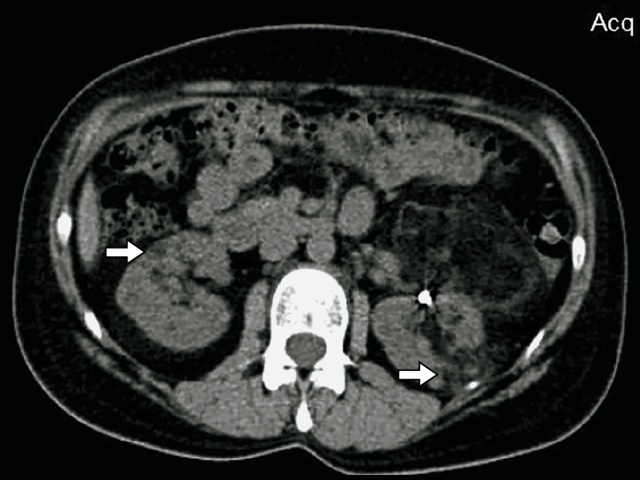
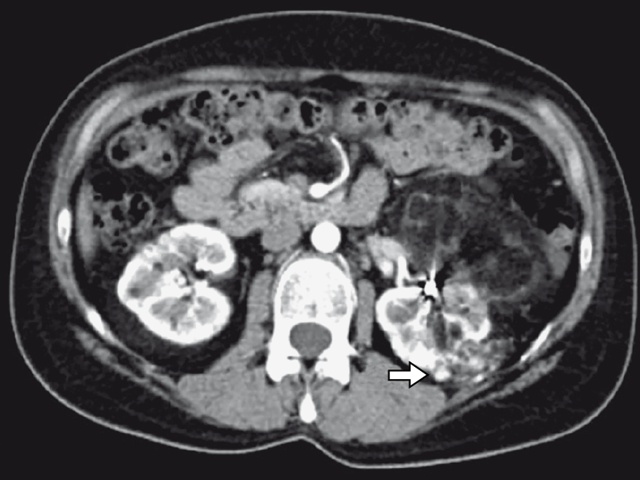
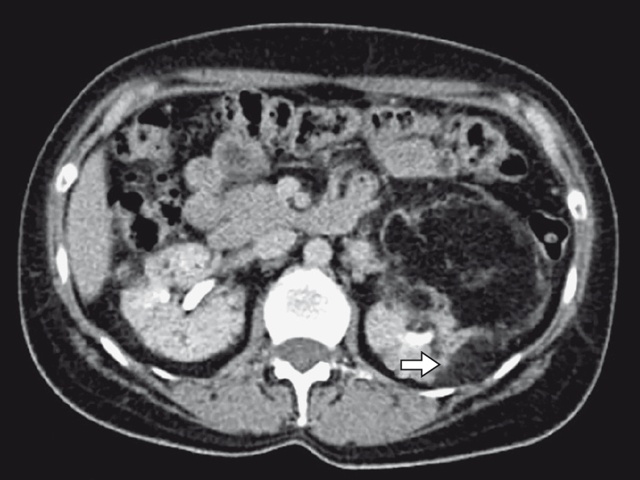
В верхнем сегменте левой почки определяется неоднородное образование с макроскопическим преобладанием жира, размерами до 10 см в диаметре. Состояние после селективной эмболизации артерии. а – нативная фаза; б – артериальная фаза; в – венозная фаза.
Дифференциальная диагностика АМЛ и ПКР
При дифференциальной диагностике будут иметь значение пол, возраст пациента, наличие травм в анамнезе. При динамическом наблюдении необходимо обратить внимание на изменение размеров образования, наличие регионарных лимфатических узлов.
При МСКТ почек с контрастированием на злокачественный характер опухоли будут указывать наличие «венчика» по периферии опухоли, быстрое вымывание контрастного вещества из опухоли. На АМЛ укажет отсутствие «венчика» по периферии опухоли и длительное сохранение контрастирования по периферии.
АМЛ с минимальным количеством жира обычно обладают гомогенным и длительным контрастированием в нефрографическую фазу по сравнению с ПКР.
Инвазия в почечную вену/нижнюю полую вену при АМЛ исключительно редка. АМЛ не имеет инфильтративного роста. Кальцинаты и некрозы в АМЛ встречаются крайне редко. Присутствие жира в сочетании с кальцинатами в образовании должно наводить на мысль о том, что это ПКР.
Прогноз
У пациентов с АМЛ в большинстве случаев прогноз благоприятный, не требует планового ее удаления, но обязывает проводить контроль функциональной способности почек.
Заключение
Таким образом, диагноз АМЛ по данным УЗИ должен быть подтвержден при КТ или МРТ с контрастированием. Обычно КТ позволяет поставить точный диагноз АМЛ с видимым или минимальным жиром. В большинстве сомнительных случаев МРТ позволяет подтвердить диагноз АМЛ или предложить альтернативный. Однако АМЛ без выявляемого жира могут быть неотличимыми по данным УЗИ, МРТ или КТ от рака почки. В таких случаях на усмотрение врача рекомендуется либо динамическое наблюдение, либо биопсия или резекция почки. Показания к оперативному лечению (резекция почки или селективная эмболизация артерии, питающей область расположения АМЛ) зависят от комплекса клинико-рентгенологических параметров, при этом размер АМЛ не является ведущим из них.
Литература
- Винаров А.З. Ангиомиолипома: что должен знать уролог // Урология сегодня. 2012; 4 (20): 1–3.
- Корчагин О.Ю., Нечипоренко Н.А. Тактика ведения больных с ангиомиолипомой почки. Журнал ГрГМУ. 2006; 2: 81–83.
- Матвеев В.Б., Сорокин К.В. Ангиомиолипома почка: диагностика и лечение // Онкоурология. 2006; 2: 14–20.
- Чикина С.Ю. Лимфангиолейомиоматоз – описание клинических случаев и обзор литературы // Практическая пульмонология. 2013; 2: 56–60.
- Ivanov D. Severe tuberous sclerosis with PKD: 5 years follow up. 17th IPNA Congress, New York (https://www.researchgate.net/publication/309187776_Severe_Tuberous_sclerosis_with_PKD_5_years_follow_up), 2016 г.
- Rabenou R.A., Charles H.W. Differentiation of sporadic versus tuberous sclerosis complex-associated angiomyolipoma // Am J Roentgenol. 2015; 205 (2): 292–301.

УЗ сканер Samsung HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Публикации по теме
- Ультразвуковые критерии изменений показателей артериоло-капиллярного русла почек у пациентов с хронической сердечной недостаточностью и кардиоренальным синдромом, полученные методом функционального нагрузочного тестирования - Слуцкая Н.В.
- Патология урахуса у взрослых в поликлинической практике - Бурков С.Г.
- Ангиомиолипомы почек - Курзанцева О.М.
- Современная лучевая диагностика абсцесса почки - Курзанцева О.М.
- Экстрофия мочевого пузыря - Одегова Н.О.


