Липолейомиома матки: опыт диагностики
Рубрика: Эхография в акушерстве
УЗ сканер Samsung HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Введение
Принято считать, что пальма первенства в описании липолейомиомы матки (ЛПМ) принадлежит V. Lobstaein, представленном в 1861 г. на страницах книги по патологической анатомии J.F. Meckel [1]. В последующие годы происходило фрагментарное накопление клинических случаев жировой трансформации гладкомышечных опухолей матки. Первый аналитически обзор 11 случаев ЛПМ был представлен в 1903 г. О. Saydel [2]. Дальнейшие обзоры на эту тему были опубликованы в 1923 г. (31 случай) [3], в 1943 г. (70 случаев) [4], в 1955 г. (96 случаев) [5] и 131 наблюдение ЛПМ было проанализировано в 1966 г. [6]. Нарастающая динамика аналитических исследований демонстрирует прогрессирующий научный интерес специалистов к проблеме ЛПМ.
Современные специалисты рассматривают ЛПМ в качестве редкого, но легко диагностируемого при патологоанатомическом исследовании доброкачественного варианта лейомиомы матки. Опухоль, состоящая из различного в пропорциях сочетания зрелых гладкомышечных клеток и адипоцитов, в большинстве случаев с преобладанием первого компонента, чаще всего обнаруживается в теле матки [7]. Морфологически выделяют липолейомиому, фибромиолипому, чистую липому, ангиомиолипому, липофиброму, липосаркому [8]. Ее следует дифференцировать с обнаруживаемыми в матке другими мезенхимальными опухолями, содержащими липоциты: фибромиолипомой, чистой липомой, ангиомиолипомой, липофибромой, липосаркомой [8].
С точки зрения S.S. Chandawale и соавт., причиной липолейомиомы является жировая доброкачественная метаморфоза гладкомышечных клеток опухоли, а не жировая дегенерация матки [9]. В то же самое время существовало мнение о злокачественной природе этой опухоли матки (цит. по [10]).
Итак, липолейомиома – редкая доброкачественная опухоль матки. Ее частота встречаемости варьирует от 0,03 до 0,2%, чаще всего будучи обнаруженной в период постменопаузы [10, 11]. Как правило, ЛПМ протекает бессимптомно.
Основным, но можно сказать и более категорично, единственным способом диагностики ЛПМ до времени начала активного использования в гинекологической практике эхографии был морфогистологический метод оценки удаленной опухоли.
Неинвазивная верификация «жировых опухолей» известна с 1978 г. M. Beham и E. Kazam [12] описали ультразвуковые характеристики жировых тканей и опухолей во многих участках тела. Авторы отметили, что в большинстве случаев жир обладает выраженной эхогенностью, сопровождаемой акустической тенью, препятствующей визуализации внутренней структуры опухоли, особенно ее дистальных отделов.
Пионеры лучевой диагностики ЛПМ – сотрудники отделения радиологии Pennsylvania Hospital L.M. Houser и соавт. [13]. Авторы описали у 59-летней пациентки с жалобами на тазовые боли «большую, твердую, неправильной формы тазовую массу, достигающую пупочного кольца». При В-сканировании в брюшной полости было обнаружено образование диаметром 16 см, центральная часть которого имела высокую эхогенность, а по периферии визуализировалась однородная гипоэхогенная ткань. Обнаруженная опухоль расценена как дермоидная кистома яичника. Диагноз ЛПМ у этой пациентки был верифицирован интра- и постоперационно при патологоанатомическом исследовании.
На страницах первой отечественной монографии по ультразвуковой диагностике в гинекологии в 1990 г. В.Н. Демидов и Б.И. Зыкин представили собственный опыт наблюдения миолипомы у трех пациенток [14]. С тех пор архив ультразвуковых диагнозов ЛПМ, как отечественных [15–19], так и зарубежных [11, 20–23], пополнялся, оставаясь по сравнению с «ультразвуковыми запасниками» иных гинекологических нозологий более скромным. При обращении к базе данных PubMed с запросом «Uterine lipoma, ultrasound diagnosis» ресурс предложил 83 источника цитирования в результатах поиска. На запрос же «Uterine mioma, fibroids, ultrasound diagnosis» – 5786 источников.
Редкую встречаемость ЛПМ, следовательно, скромный опыт особенно у начинающих специалистов, неоднозначность трактовок эхографических изображений ЛПМ можно рассматривать в ряду причин, снижающих диагностический потенциал эхографии в ультразвуковой верфикации этой опухоли. Трудности дифференциальной диагностики патологических образований миометрия, в частности ЛПМ, существовавшие в далекие 70-е годы XX столетия [13], сохранились спустя десятилетия [24].
С целью пополнения багажа знаний и портфеля морфологически верифицированных редких случаев онкогинекологии представляем собственный клинический опыт диагностики ЛПМ.
Клиническое наблюдение
Пациентка Л., 69 лет, 10.10.2022 обратилась с жалобами на периодически тянущие, часто беспокоящие боли внизу живота в течение последних 9 мес. В течение последних 2 мес боли усилились, стали постоянными.
Объективный статус: правильного телосложения, удовлетворительного питания (индекс массы тела 24, норма). Живот правильной формы, не увеличен. Из анамнеза выяснено, что перенесла ряд операций: в 1959 г. – аппендэктомия, в 1997 г. – правосторонняя мастэктомия по поводу «рака молочной железы» с последующими шестью курсами химиотерапии (медицинская документация по теме отсутствует), в 2007 г. – левосторонняя тиреоидэктомия, в 2010 г. – геморроидэктомия, в 2021 г. – удаление полипа уретры.
Менопауза 25 лет. В анамнезе двое неосложненных родов в срок, один артифициальный аборт. После мастэктомии к гинекологу не обращалась.
Локальный статус: наружные половые органы – без особенностей. Слизистая оболочка влагалища и шейки матки – без видимых патологических изменений. Выделения слизистые, скудные. Тело матки увеличено до 7–8 нед условной беременности, плотное, подвижное, чувствительное при пальпации. Яичники с обеих сторон не пальпируются, зона придатков безболезненна. Своды свободны.
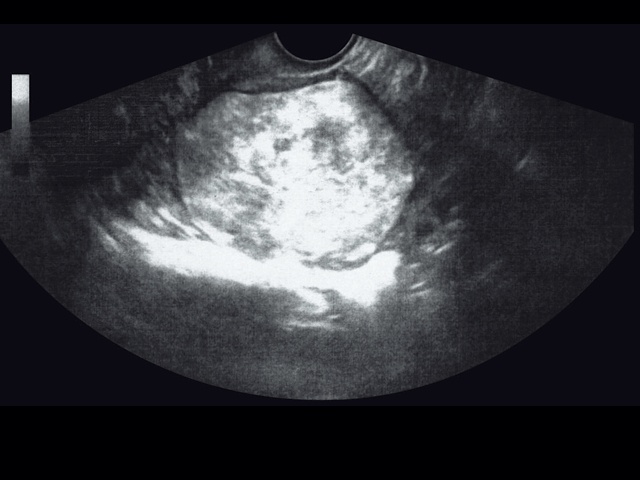
Рис. 1. Эхограмма (трансвагинальное сканирование) липолейомиомы.
01.07.2022 была выполнена трансвагинальная эхография (рис. 1): «… тело матки в anteflexio размерами 69 х 60 х 78 мм, контуры тела матки относительно ровные, форма шаровидная, миометрий умеренно неоднородный, лоцируется только передняя стенка толщиной 5 мм, задняя не дифференцируется, стенки матки четко не дифференцируются, все тело матки занимает гипоэхогенное гетерогенное образование с достаточно ровными четкими контурами, размерами 73 х 56,5 х 72 мм, с неактивным кровотоком по периферии, возможно расположенное в полости матки (субмукозная миома? дифференцировать с патологией эндометрия – гиперплазия?). Шейка матки обычной формы, размерами 25 х 24 х 29 мм, патологически не изменена. Яичники с обеих сторон не визуализированы. Стенки влагалища типичной структуры, не утолщены, васкуляризация не усилена, дополнительных образований не выявлено. Отмечается дилатация единичных вен тазового сплетения до 6,5 мм, вены проходимы, скоростные характеристики без особенностей, V = 4 см/с. Проба Вальсальвы отрицательная. Свободная жидкость в позадиматочном пространстве не определяется. Заключение: эхографические признаки миомы матки? Диф ференцировать с патологией эндометрия – гиперплазия? Suspicio Neo. Умеренные диффузные изменения миометрия, умеренная дилатация вен параметрального сплетения». Рекомендована консультация гинеколога, решение вопроса о целесообразности проведения МРТ, динамическое УЗИ.
05.07.2022 выполнена МРТ (рис. 2) нативно в T1, T2, DWI и STIR режимах в стандартных плоскостях: «… матка в положении retroflexio с правосторонней латерофлексией, в проекции матки (принадлежность матки трудно установить, вероятно, в полости) визуализируется образование округлой формы с четкими ровными контурами, с преимущественным содержанием жировой такни, наличием единичных септ размерами 57 х 61 х 61 мм, миометрий дифференцируется в виде тонкой полоски по периферии образования толщиной 7 мм в области передней стенки, по правому и заднему контурам образования небольшое количество жидкости. Яичники инволютивно изменены. Мочевой пузырь равномерно заполнен, содержимое однородно и соответствует жидкости, стенки не утолщены, паравезикальное пространство без особенностей. Лимфоузлы органов малого таза не увеличены, структура их не изменена. Сосуды малого таза обычно расположены. Костные структуры малого таза с признаками дистрофических изменений. Заключение: МРТ-картина жирсодержащего образования полости матки (возможна липомиома)». Пациентка была консультирована онкогинекологом, рекомендовано оперативное лечение.
12.10.2022 выполнена надвлагалищная ампутация матки без придатков. Макропрепарат: экстирпированное тело матки без придатков, длина полости по зонду 7 см, в центральной части передней стенки тела матки располагается крупный узел диаметром 7,5 см, состоящий из светло-желтого цвета жировой ткани, окружен тонкой плотной фиброзной капсулой, границы узла четкие (рис. 3). При гистологическом исследовании операционного материала диагностирована липолейомиома. Опухолевый узел состоял из беспорядочно расположенных зрелых липоцитов (унилокулярных клеток, содержащих одну жировую вакуоль) и мелких пучков гладкомышечных клеток (рис. 4). Между ними располагались капилляры и сосуды синусоидного типа. По периферии опухоли отмечалась атрофия гладкомышечных клеток (рис. 5).
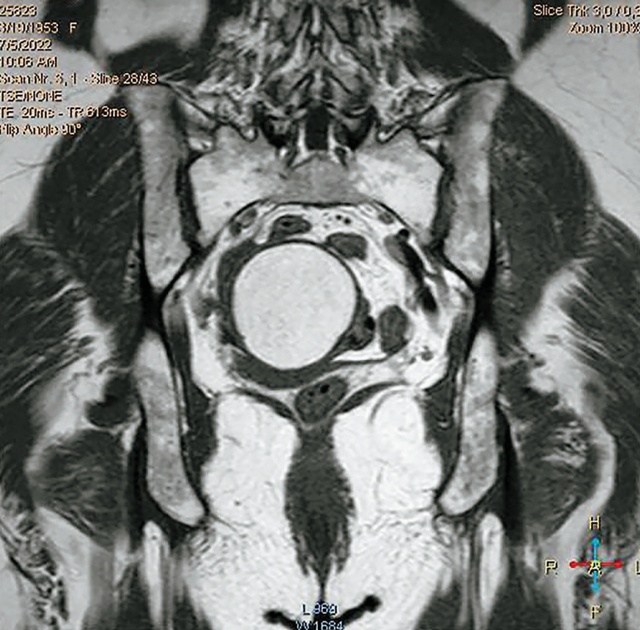
а) фронтальное сечение.
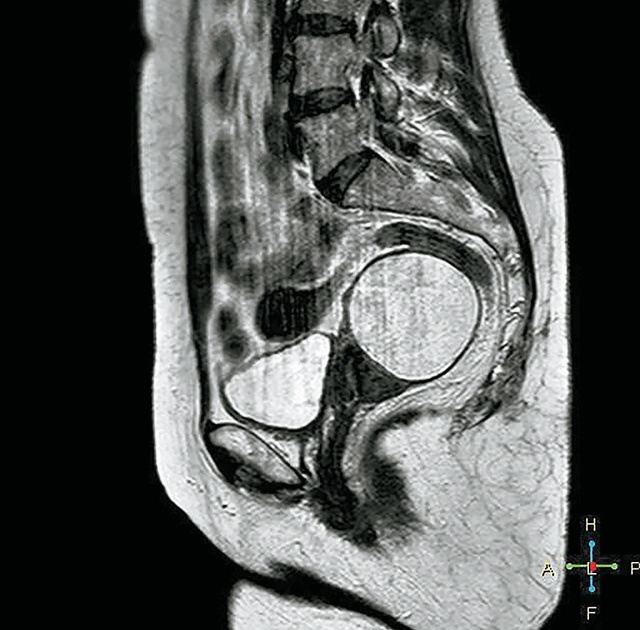
б) сагиттальное сечение.
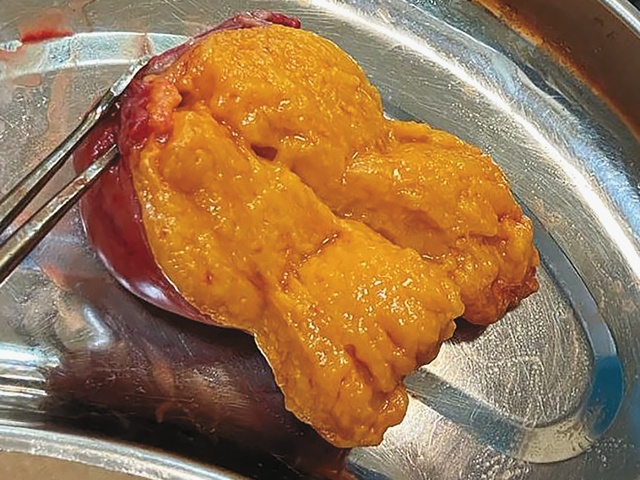
Рис. 3. Макропрепарат тела матки. На разрезе практически вся матка представлена однородной мягкой тканью желтого цвета, напоминающей жировую.
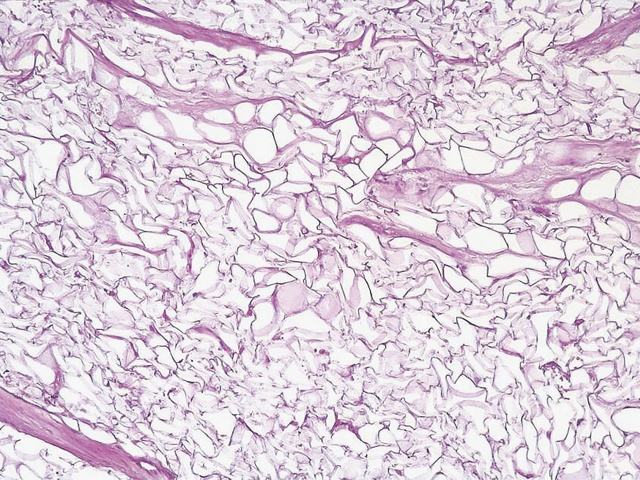
Рис. 4. Микропрепарат липолейомиомы (описание в тексте). Окраска гематоксилин-эозином. х100.
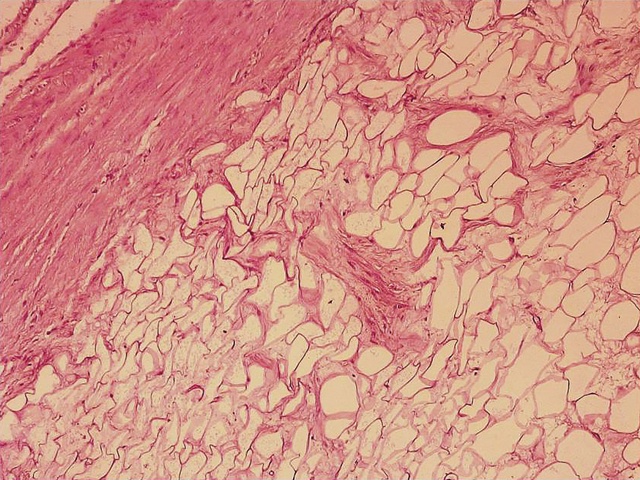
Рис. 5. Микропрепарат липолейомиомы (описание в тексте). Окраска гематоксилин-эозином. х100.
Послеоперационное течение гладкое. Пациентка в удовлетворительном состоянии выписана на 6-е сутки.
Обсуждение
На современном этапе развития визуализирующих ультразвуковых технологий, применяемых в гинекологической клинике, можно с абсолютной уверенностью утверждать, что эхография обладает 100% чувствительностью в дифференцировании патологических и анатомически неизмененных объектов малого таза. Однако показатель специфичности метода, как бы нам ни хотелось иного, остается невысок. Да, бесспорно, произошло значительное увеличение «правильных диагнозов» при формулировке ультразвукового заключения после внедрения в ежедневную практику диагностических критериев MUSA (Morphological Uterus Sonographic Assessment), IETA (International Endomertial Tumor Analysis group), IOTA (International Ovarian Tumor Analysis group) [18]. Однако гистологическая идентификация опухолей малого таза, хоть матки, хоть придатков, остается единственным инструментом в «присвоении имени» обнаруженной опухоли. Говоря об опыте диагностики, заявленном в названии настоящей статьи, считаем необходимым согласиться с мнением многих авторитетных авторов, говорящих о недопустимости формулировки ультразвукового заключения типа «миоматозный, саркоматозный, липоматозный узел» и т.д. В то же самое время, анализируя вышепредставленное ультразвуковое заключение, хочется поинтересоваться, какое состояние предполагается, что скрывается за формулировкой «умеренные диффузные изменения миометрия»?
Считаем, что весьма характерный ультразвуковой «внешний вид» (четкий, ровный наружный контур, правильная, округло-овальная форма, однородная аваскулярная структура и высокая эхогенность) обнаруженного маточного образования при сопоставлении с литературными данными [14–19] уже на этапе первичной эхографии позволял в дифференциальном ряду обсуждаемых состояний упомянуть «липому матки», причем на лидирующем месте.
МРТ, выполненная с использованием технологий идентификации жира, позволила верифицировать внутриопухолевый жир, практически «поставив точку» в формулировке предоперационного диагноза, подтвержденного в последующем морфологами.
Литература
- Lobstein V. In.: J.F. Meckel. Handbuch der pathologischen Anatomie // Reciam Leipzig, 1816; 2: 311.
- Saydel O. Lipomyofibroma myomatosum uteri // Ztschr Geburtsh Gynäk. 1903; 50: 274–292.
- Petersen A.J. Mixed tumours of the uterus // J Lab Clin Med. 1923; 8: 369–374.
- Kaseman W. Über heterologe benigne Fettgeschwülste des Uterus // Zentralbl Gynek. 1943; 67: 914–924.
- Brandfass R.J., Everts-Suarez E.A. Lipomatous tumours of the uterus// Am J Obstet Gynec. 1955; 70: 359–367.
- Barbanti-Silva C. Il lipoma dell' utero // Archivio de vecci per l'anatomia patologica. 1966; 47: 931–959.
- Akbulut M., Soysal M.E., Duzcan S.E. Giant lipoleiomyoma of the uterine corpus // Arch Gynecol Obstet. 2008; 278: 291–293. DOI: 10.1007/s00404-008-0580-0
- Чиссов В.И. Онкология: Национальное руководство. Краткое издание / Под ред. В.И. Чиссова, М.И. Давыдова. М.: ГЭОТАР-Медиа, 2017.
- Chandawale S.S., Karia K.M., Agrawal N.S. et al. Uterine Lipoleiomyoma and Lipoma: A Rare Unique Case Report with Review of Literature // Int J Appl Basic Med Res. 2018; 8 (3): 193–195. DOI: 10.4103/ijabmr. IJABMR_119_17
- Akbulut M., Gündoğan M., Yörükoğlu A. Clinical and pathological features of lipoleiomyoma of the uterine corpus: a review of 76 cases // Balkan Med J. 2014; 31 (3): 224–229. DOI: 10.5152/balkanmedj.2014.13079
- Wong F. Lipoleiomyoma: a rare uterine tumor // Wld J Advanc Res Rev. 2021; 09 (03): 269–271. DOI: 10.30574/wjarr.2021.9.3.0099
- Beham M., Kazam E. The echographic characteristics of fatty tissues and tumors // Radiology. 1978; 129: 143–151. DOI: 10.1148/129.1.143
- Houser L.M., Carassco C.H., Sheen Jr. Lipomatous tumour of the uterus: radiographic and ultrasonic appearance // Br J Radiol. 1979; 52 (624): 992–993. DOI: 10.1259/0007-1285-52-624-992
- Демидов В.Н., Зыкин Б.И. Ультразвуковая диагностика в гинекологии. М.: Медицина, 1990: 75.
- Громов А.И., Маканин М.А., Загвоздкин С.С., Иванова С.И. Липома матки в сочетании с высокодифференцированной аденокарциномой эндометрия // Ультразвуковая диагностика в акушерстве, гинекологии, педиатрии. 1999; 2 (7): 164–166.
- Озерская И.А. Эхография в гинекологии. 2-е изд., перераб. и доп. М.: Издательский дом Видар-М, 2013: 196–197.
- Буланов М.Н. Ультразвуковая гинекология: курс лекций в 3-х томах. Т.1. М.: Издательский дом Видар-М, 2010: 238–239.
- Буланов М.Н. Ультразвуковая диагностика в гинекологии: Руководство для врачей. М.: Издательский дом Видар-М, 2022: 192.
- Допплерография в гинекологии / Под ред. Б.И. Зыкина, М.В. Медведева. М.: Реальное время, 2000: 149.
- Prieto A., Crespo C., Pardo A. et al. Uterine lipoleiomyomas: US and CT findings // Abdom Imaging. 2000; 25 (6): 655–657. DOI: 10.1007/s002610000052
- Tsushima Y., Kita T., Yamamoto K. Uterine lipoleiomyoma: MRI, CT and ultrasonographic findings // Brit J Radiol. 1997; 70 (838): 1068–1070. DOI: 10.1259/bjr.70.838.9404215
- Kim Y.S., Lee J.H. A case report of pelviscopic resection of lipoleiomyoma originating from the uterine cervix in a postmenopausal woman // Medicine (Baltimore). 2022; 101 (39): e30665. DOI: 10.1097/ MD.0000000000030665
- Chan N., Vythianathan M. Uterine lipoma: a case report // Case Rep Womens Health. 2020; 13 (28): e00247. DOI: 10.1016/j.crwh.2020.e00247
- Давыдов А.И., Белоцерковцева Л.Д., Зайратьянц Г.О. Липома матки: сложности дифференциальной диагностики. Вопросы гинекологии, акушерства и перинатологии. 2017; 16 (6): 93–95. DOI: 10.20953/1726-1678-2017-6-93-95

УЗ сканер Samsung HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Публикации по теме
- Оценка ушной раковины плода как ключ к диагностике более серьезных изменений и синдромальной патологии. Два случая пренатальной диагностики - Мазырко М.А.
- Ультразвуковая навигация при планировании контактной лучевой терапии рака шейки матки - Дымовская Д.А.
- Липолейомиома матки: опыт диагностики - Волков А.Е.
- Особенности визуальной картины при различных молекулярных подтипах рака молочной железы у молодых пациенток: клинические наблюдения - Васильченко С.А.
- Ультразвуковая диагностика аномального прикрепления плаценты в I триместре беременности - Андрусенко И.В.



